人们等待着“科学权威”提供现成的答案,然而,“科学权威”们要么在沉默,要么在撒谎。
本文接续:连系新冠病毒与Ralph S. Baric的双纽带(上)
新冠病毒RBD决定ACE2结合能力,决定细胞进入(感染)能力,决定宿主范围的五个关键氨基酸是人为设计出来的,有人参照WIV1病毒的关键氨基酸,通过氨基酸重用和等价、等效替代,设计出了新冠病毒的关键氨基酸。人为设计的新冠病毒的关键氨基酸,与WIV1(rs3367)的关键氨基酸不仅高度关联,而且高度等价、等效。新冠病毒与WIV1(rs3367)病毒关键氨基酸的高度等价、等效性导致了以下三项貌似“巧合”的产生:
1)新冠病毒、WIV1(rs3367)病毒的跨物种感染能力都极其强大,难分伯仲。
2)新冠病毒、WIV1(rs3367)病毒不仅都具有极其广泛的宿主范围,而且它们的宿主范围还高度雷同(重合)。
3)新冠病毒、WIV1(rs3367)病毒的刺突蛋白都极其适合结合hACE2(human ACE2)。
前二项“巧合”在上一篇文章中已经作过详细说明。第3)项巧合的依据如下:
a)本文论文A-2(见后)以转基因小鼠(mACE2转基因为hACE2的小鼠)体内实验证明了WIV1病毒刺突蛋白的强大hACE2结合能力;
b)澳大利亚弗林德斯大学2021年6月24日正式发表于Nature Science的论文以模拟实验证明:
在14个研究物种中,与新冠病毒刺突蛋白结合能力最强的物种ACE2,就是hACE2。
https://www.nature.com/articles/s41598-021-92388-5
除上述三项巧合外,还有第四项“巧合”:新冠病毒、WIV1病毒都具有泛组织、器官感染能力。这一“巧合”的首因当然是ACE2的泛组织、器官存在性;但它很可能也与新冠病毒RBD关键氨基酸的人为设计有关,因为这一设计赋予了新冠病毒强大的hACE2结合能力,使它能够非常高效有力地结合人体各处的ACE2,非常高效有力地感染人体的各个组织、器官。
谁参照WIV1(rs3367)病毒,重用、替代其关键氨基酸,设计出了新冠病毒的关键氨基酸?
有没有什么人对WIV1(rs3367)病毒、对关键氨基酸,都做过深入的研究?
五个条件,Ralph S. Baric团队 vs 石正丽团队
有人对WIV1(rs3367)病毒,对冠状病毒RBD的关键氨基酸都做过深入的研究,并符合以下五个条件:
1)反复、深入研究过WIV1(rs3367);
2)“无数次”研究过冠状病毒RBD的关键氨基酸;
3)有着长期的,极为丰富的病毒改造、合成经验,功能增益研究经验,无数次人工合成自然病毒(克隆)、常规改造病毒、功能增益性改造病毒;
4)多次对关键氨基酸进行改造、替代,改造、培育出过多种可跨物种传播(如可感染人类和灵长类动物)的冠状病毒;
5)曾以WIV1(rs3367)为原材料,改造出有人类致病能力的危险病毒。
这个人是谁?就是Ralph S. Baric。Ralph S. Baric或其团队应该是唯一同时符合以上五个条件的人或团队。
Ralph S. Baric热衷于对冠状病毒进行功能增益性改造研究和实验,其理由是,功能增益研究、实验是在模拟病毒的自然突变,可以预测、预警未来可能出现的危险病毒,并提前研究、预备治疗手段。然而,功能增益研究、实验存在如下致命问题:冠状病毒自然演化史上从未出现过的高危突变,自然条件下再过一亿年也不会发生的高危突变(如将非冠状病毒的结构、功能嫁接、移植给冠状病毒),在实验室条件下几周甚至几天就可以设计、实现出来;功能增益性研究能够迅速、快捷地设计出无数一亿年也不会发生,甚至永远不会发生的自然突变,创造出无数可能永远不会自然产生的高危病毒,一旦它们中的任何一个从实验室意外溢出,或被人为地投放,就将给人类带来重大灾难。
WIV1、rs3367都是石正丽团队发现的,石正丽团队也多次研究过这两个病毒;而且,在SARS病毒溯源、蝙蝠冠状病毒跨物种传播研究中,石正丽团队也不只一次研究过冠状病毒的关键氨基酸。上述五个条件,石正丽团队是不是也符合?并不符合,具体原因如下:
1)石正丽团队的研究与Ralph S. Baric团队的研究有着本质的区别。
石正丽团队在发现、认知、解读天然蝙蝠冠状病毒既有的结构、既有的功能、既有的特性,包括跨物种感染、传播特性;而Ralph S. Baric团队则在每每制造蝙蝠冠状病毒及其它动物冠状病毒(如果子狸冠状病毒)的人为突变,人为增益、赋予冠状病毒新结构、新特性、新功能。
石正丽团队在各论文中所做的病毒改造都是常规改造,无一是功能增益改造;而Ralph S. Baric团队则对冠状病毒实施过大量的功能增益性改造,制造或培育出过多种有人类致病力的冠状病毒,及宿主更广的可跨物种传播的冠状病毒。
注:改造病毒是病毒研究的家常便饭和必要手段,在病毒研究中无可避免地需要对病毒进行常规改造,例如:制作危险病毒的去毒性假病毒需要改造、加工病毒;制造某些疫苗如腺病毒载体疫苗需要改造、加工病毒;将绿色荧光蛋白GFP(Green fluorescent protein)或红色荧光蛋白RFP嵌入到病毒中以便观察实验现象需要改造病毒;研究某个蛋白的功能时,需要从病毒中去除该蛋白或以其它蛋白替换该蛋白,通过对比改造前后病毒功能的变化来推断原蛋白的功能。
2)相比Ralph S. Baric团队,石正丽团队对关键氨基酸的研究有限得多,粗浅得多。
3)石正丽团队的功能增益研究、病毒功能增益改造经验为0。在病毒研究中,石正丽团队当然也需要对病毒进行常规改造,但他们没有对病毒实施过任何功能增益性改造,论文记录、文献记录表明,石正丽团队从未发表过功能增益研究论文,从未改造出过有人类致病能力的病毒,从未改造出过感染能力更强或宿主范围更广的病毒。
4)在冠状病毒关键氨基酸相关的研究中,石正丽团队没有制造过可跨物种传播的病毒,没有制造过可感染人类和灵长类动物的病毒。
5)石正丽团队从未将WIV1(rs3367)用于功能增益研究,从未以WIV1为原材料制造有人类致病能力的病毒。
Ralph S. Baric(团队)对WIV1(rs3367)的研究
Ralph S. Baric团队对跨物种感染能力极其强大的WIV1(rs3367)非常关注,2015年到2018年这四年间,该团队至少在4篇论文中研究了WIV1(rs3367),其中两篇论文是专门研究WIV1(rs3367)。
论文A-1
2015年11月9日,Ralph
S. Baric团队在《自然医学》(Nature Medicine)杂志发表了著名的嵌合病毒论文:A SARS-like cluster of
circulating bat coronaviruses shows potential for human
emergence(一个类似SARS的蝙蝠冠状病毒群显示了产生人类流行疫情的潜力)
https://www.nature.com/articles/nm.3985

我已经无数次介绍、提及过这篇论文。Ralph S. Baric是论文的两个通讯作者之一,另一通讯作者是论文的第一作者Vineet D. Menachery(维内特·德梅纳赫里),此人是Ralph S. Baric团队的重要人物,是该团队多篇论文的第一作者。
论文用SHC014(即rsSHC014)病毒的刺突蛋白和SARS-CoV-MA15病毒的骨干制造了一种高度危险的嵌合病毒SHC014-MA15(制造此类嵌合病毒都是首先设计嵌合的基因序列,而后基于设计好的基因序列,使用反向遗传系统合成嵌合病毒);
SHC014-MA15可使实验小鼠发病、体重大幅下降并死亡;
SHC014-MA15还能感染Vero E6细胞(非洲绿猴肾细胞系细胞)、人类气道上皮细胞(HAE细胞),在组织细胞内大量复制,复制滴度与SARS病毒感染相当;
SARS单克隆抗体和SARS疫苗都不能有效治疗SHC014-MA15的感染。
SARS-CoV-MA15是Ralph S. Baric团队在实验室环境下反复传代培育出的SARS病毒小鼠适应性变异体。
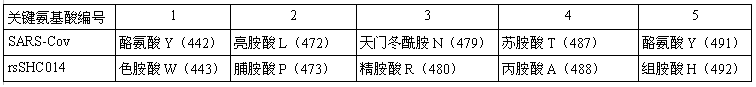
这篇论文的病毒主角是SHC014,WIV1在论文中是SHC014的对照病毒。论文指出:在刺突蛋白RBD决定ACE2结合能力、细胞进入能力及宿主范围的5个关键氨基酸(残基)中,WIV1病毒与SARS病毒虽然有三个关键氨基酸(1、2、4)不同,但其刺突蛋白仍能与hACE2(human ACE2)有效结合,与SARS一样,WIV1也具有人类细胞进入(感染)能力。
注:这一事实说明,与hACE2适配的关键氨基酸组合是不唯一的。
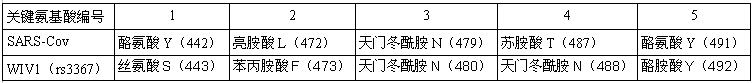
WIV1、SARS关键氨基酸对照表。二者的第3、5关键氨基酸相同,第1、2、4关键氨基酸不同。
WIV1具有人类细胞进入能力,其刺突蛋白可结合hACE2,这是石正丽团队2013年10月30日的nature论文已得出的结论,上述论文内容引用了这一结论。
https://www.nature.com/articles/nature12711
论文接着指出,相比WIV1,SHC014的关键氨基酸与SARS差异更大,无一相同。
SHC014、SARS关键氨基酸对照表。它们的5个关键氨基酸无一相同。
那么,SHC014的刺突蛋白能否结合hACE2?SHC014是否具有人类细胞进入能力呢?这是2015年论文要解决的核心问题之一。
上述问题是如何解决的?Baric等人用SHC014的刺突蛋白、SARS-CoV-MA15的骨干构建了嵌合病毒SHC014-MA15,通过SHC014-MA15对人气道上皮组织样本的感染实验证明,SHC014的刺突蛋白也能有效结合hACE2,进而间接证明,SHC014与WIV1一样,也是具有人体细胞进入(感染)能力的特殊蝙蝠冠状病毒。
注:SHC014也和WIV1一样,能进入(感染)人体细胞,但不会使人体产生疾病症状。
论文A-1是一篇功能增益研究论文,它以有人类感染能力,但无人类致病能力的SHC014病毒为原材料之一,改造出了有人类感染能力和高度致病危险(致病能力未经灵长类动物实验证实),在人体细胞中的感染、复制能力与SARS相当的高危病毒SHC014-MA15。
论文A-2
2016年3月14日,Ralph S. Baric团队在PNAS(美国国家科学院院刊)发表了如下论文:SARS-like WIV1-CoV poised for human emergence(类SARS冠状病毒WIV1-CoV对人类有潜在威胁)
https://www.pnas.org/content/113/11/3048
Ralph S. Baric仍是论文的通讯作者。
论文A-1中的对照病毒WIV1在这篇论文中晋升为病毒主角。论文有如下要点:
1)以WIV1刺突蛋白的基因序列替换SARS-CoV-MA15刺突蛋白的基因序列,设计了一个嵌合的基因序列,而后使用反向遗传平台,基于嵌合的基因序列,合成了嵌合病毒WIV1-MA15。合成WIV1-MA15、SHC014-MA15的原理、方法完全相同,区别只是换了一种刺突蛋白。
2)还使用反向遗传平台,基于WIV1的基因序列,合成了WIV1的病毒克隆,论文称之为WIV1-CoV。
3)小鼠体内实验证明,WIV1-MA15能有效感染实验小鼠,并能在小鼠气道和肺中复制;但与SAR-CoV的小鼠适应性变异体SARS-CoV-MA15相比,WIV1-MA15在小鼠肺中的复制滴度低10~100倍。
4)体外细胞实验证明,WIV1-MA15能强烈感染灵长类动物的Vero E6细胞(非洲绿猴肾细胞),强烈感染人气道上皮细胞(HAE细胞),它在这两种细胞中的复制滴度与SARS-CoV流行病毒株相当(SHC014-MA15亦是如此)。
体内实验、体外实验表明,人工改造病毒WIV1-MA15具有跨物种感染、传播能力,且其对人类、灵长类细胞的感染、复制能力与SARS病毒相当。
注:因为继承了WIV1的刺突蛋白,因此,WIV1-MA15也继承了WIV1强大的的跨物种感染能力,其跨物种感染、传播能力应该不逊色于新冠病毒。
5)实验证明,WIV1-MA15对普通实验小鼠的致病力明显弱于SARS-CoV-MA15,它只能使年轻的小鼠(10周龄)产生有限的疾病,不会使其体重显著下降(超过10%),更不会使其致死。
6)设计、培育了一种转基因小鼠,其肺、脑、肝、肾和胃肠道等部位的ACE2被转基因为hACE2。
7)如果将实验小鼠换成上述转基因小鼠,那么WIV1-MA15,甚至WIV-CoV自身的感染、复制能力、致病能力都将显著增强。相比普通小鼠,WIV1-MA15、WIV1-CoV在转基因小鼠细胞中的复制滴度提高了100倍;部分10-20周龄的被感染转基因小鼠体重减轻超过10%,这些小鼠还因病毒在大脑中的强劲复制而患上了脑炎。
注:这一实验结果表明,WIV1的刺突蛋白更适合结合hACE2,WIV1更适合感染人类细胞,在这两项特征上,新冠病毒与WIV1病毒完全一致;WIV1与新冠的区别是,它的病毒骨架没有人类毒性(致病力),它能感染人体细胞,但不能使人体发病。
8)实验证明,SARS单克隆抗体可有效治疗WIV1-MA15感染,但SARS疫苗对WIV1-MA15感染则没有什么疗效,并有显著的副作用。
Ralph S. Baric团队应该是唯一一支将WIV1(rs3367)用于功能增益研究,以之为原材料改造出人类致病性危险病毒的科学团队,我未发现其它团队、个人发表过相关论文。
下面还有意义更重大的内容。
论文Discussion部分指出:冠状病毒刺突蛋白RBD外其它区域的某些变化,如S2亚基的某些变化,S1亚基RBD外区域的某些变化,可能:
1)增强刺突蛋白与宿主蛋白酶(ACE2受体就是一种蛋白酶)作用的靶向性,
2)增进刺突蛋白的切割(酶切)特性,
3)增进刺突蛋白的扩展性,
从而使病毒获得更健全的感染能力。
这实际上是在预测、展望进一步的病毒改造方向。
注:Ralph S. Baric(团队)一直打着模拟、预测自然变异的旗号,自充造物主,对冠状病毒施以各种功能增益性改造,刻意制造人为突变,热衷于为冠状病毒引入、增加新结构、新特性、新功能,积极研究、借鉴各种对抗宿主免疫系统的功能、机制。
令人难以置信的是,论文中的三项预测,在3年半后出现的新冠病毒中全都神奇地应验、实现了!论文预言的刺突蛋白的扩展性、新的切割(酶切)特性、与宿主蛋白酶(如ACE2受体)作用的靶向性,分别对应着新冠病毒的以下三组结构、特性或功能:
1)刺突蛋白的扩展性对应着新冠刺突蛋白中可灵活屈直、伸缩、扭转的三关节式铰链结构,该结构使刺突蛋白前端的RBD能以多样的角度、姿态,更灵活、更有效地结合细胞表面的ACE2受体。
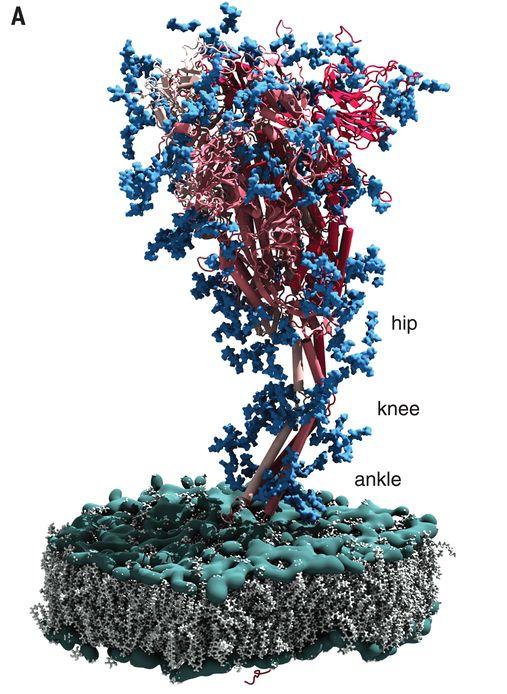
新冠病毒刺突蛋白三关节式绞链结构示意图
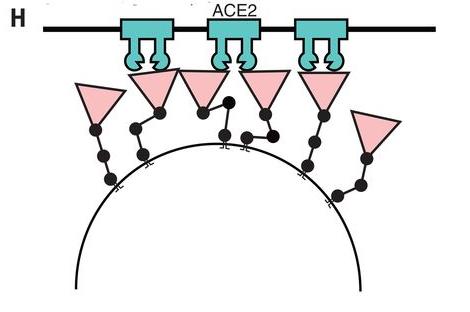
新冠病毒刺突蛋白以多样的角度、姿态灵活接触、结合ACE2示意图
2)新的切割(酶切)特性对应着新冠刺突蛋白S1亚基、S2亚基交界处功能强大的furin酶切位点结构(RRAR四氨基酸组合)。S1亚基与ACE2完成结合后,furin蛋白酶对furin酶切位点的切割使S1亚基脱落,使S2亚基、病毒包膜直接接触宿主细胞膜并与之发生膜融合,新冠病毒将在膜融合后直接将RNA释放到细胞中,立即开始病毒复制过程。
相比没有furin酶切位点,只能以胞吞方式“笨拙”进入宿主细胞、迟缓复制的SARS病毒,新冠病毒的感染、复制效率提高了100-1000倍!
furin酶切位点还赋予新冠病毒以膜融合的方式感染并杀死T淋巴细胞,破坏人体免疫系统的能力,这一能力也是SARS病毒所不具备的。
已知的所有蝙蝠冠状病毒都没有furin酶切位点。
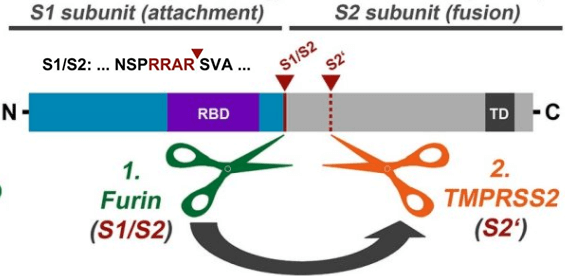
新冠病毒中的furin酶切位点、TMPRSS2(跨膜丝氨酸蛋白酶2)酶切位点示意图。SARS病毒只有TMPRSS2酶切位点。
3)与宿主蛋白酶(如ACE2受体)作用的靶向性对应着新冠病毒刺突蛋白与ACE2结合的针对性、目的性,以及隐蔽RBD,逃避抗体结合的特性,这组特性其实就是三关节式绞链结构所赋予的。
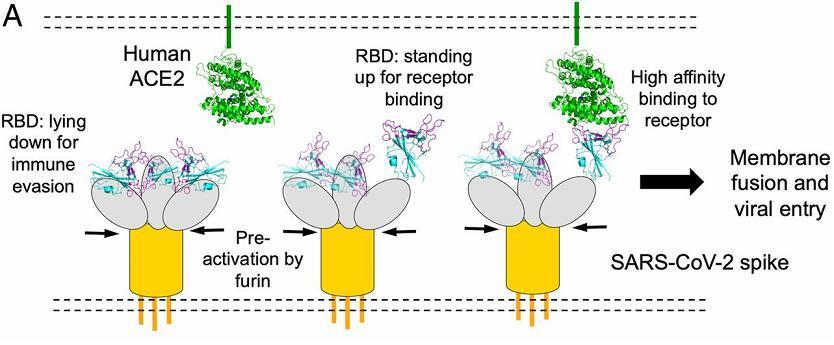
新冠病毒刺突蛋白起立、暴露RBD以结合ACE2,倒伏、隐藏RBD以逃避抗体结合示意图
关于论文中的三项预测及新冠病毒中的三项对应特性,还可参见:
出自科学疯子之手的病毒集大成者(二)
这篇2016年PNAS论文也是一篇功能增益论文,它以有人类感染能力,但无人类致病能力的WIV1为原材料之一,改造出了有人类感染能力和致病可能(致病能力未经灵长类动物实验证实),在人体细胞中的感染、复制能力与SARS相当的危病毒险WIV1-MA15。
需要特别指出的是,2015年11月的nature medicine论文、2016年3月的PNAS论文,相关研究都是奥巴马暂停令颁布后仍在进行的SARS相关的功能增益研究。
鉴于功能增益研究可能带来的难以预知的生物安全和生物安保风险,2014年10月17日,奥巴马政府颁布了一项“功能增益研究暂停令”,要求对功能增益研究进行严格的审议、监督,并暂停了对流感、SARS、MERS(中东呼吸综合症病毒)相关的功能增益研究的政府资金支持。
暂停令全文:
http://www.phe.gov/s3/dualuse/Documents/gain-of-function.pdf
奥巴马政府“功能增益研究暂停令”也被称为奥巴马功能增益研究禁令,简称奥巴马禁令。
暂停令颁布后,Ralph S. Baric深感不满,他给NIH(美国国立卫生研究院)写了一封长信,表示暂停令将严重影响冠状病毒研究,未来如果再爆发疫情,科学家将不能快速应变、控制疫情。Ralph S. Baric还提出,他的两项功能增益研究是在暂停令颁布前启动的,要求NIH允许继续完成这两项研究。NIH经过所谓“审查”,根据暂停令中的有关条款,特别批准了Baric的要求。完成了两项SARS相关的功能增益研究后,Ralph S. Baric团队分别发表了2015年11月9日的Nature Medicine论文和2016年3月14日的PNAS论文,即论文A-1、A-2。
以下是两篇论文“Biosafety and biosecurity”部分的图示,其中的:
US
Government Deliberative Process Research Funding Pause on Selected
Gain-of-Function Research Involving Influenza, MERS and SARS
Viruses(美国政府对选定的涉及流感、MERS和 SARS 病毒的功能获得性研究的审议过程研究资金暂停)
就是指奥巴马功能增益研究暂停令。

2015年11月Nature Medicine论文的Biosafety and Biosecurity

2016年3月PNAS论文的Biosafety and Biosecurity
功能增益研究,即功能获得性研究,英文为Gain-of-Function,缩写为G-o-F或GoF,指人为赋予病毒或病原体感染、致病、传播功能、特性,或人为增强其感染、致病、传播功能、特性的病毒、微生物改造研究。
美国国立卫生研究院(NIH)院长弗朗西斯·柯林斯(Francis S. Collins),NIH下属美国国立过敏和传染病研究所十几年的所长,白宫首席医学顾问安东尼·福奇(Anthony Fauci),是支持功能增益研究的两位重量级美国卫生官员。
Collins、Fauci支持的是武汉病毒研究所的功能增益研究吗?武汉病毒研究所根本未开展、从事任何功能增益研究,他们如何支持不存在的功能增益研究?他们支持的是美国本国病毒学家的功能增益研究,包括Ralph S. Baric团队的功能增益研究。
2017年12月19日,川普政府撤销了奥巴马暂停令,全面重启功能增益研究,并恢复了对该类研究的联邦资金支持。两年后,新冠病毒在武汉出现,疫情爆发。
弗朗西斯·柯林斯、安东尼·福奇也是川普共和党政府撤销奥巴马功能增益研究暂停令的重要推手。Fauci为什么一直谎称新冠病毒来自自然界?川普及其幕僚为什么一再捏造、散布卑鄙、下作的谎言,构陷、诬蔑武汉病毒研究所?川普为什么多次刻意淡化、贬低新冠病毒的危害?因为川普、Collins、Fauci都是新冠病毒产生的重大责任人。
论文A-3
2017年6月28日,Ralph S. Baric团队(北卡罗来纳大学教堂山分校流行病学系)、范德堡大学医学中心、波兰Jagiellonian University、吉利德科技等单位在《ScienceTranslational Medicine》杂志联合发表了一篇瑞德西韦研究论文:Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses(广谱抗病毒药物 GS-5734可抑制流行性人畜共患冠状病毒)
https://stm.sciencemag.org/content/9/396/eaal3653
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5567817/
论文指出:目前正在临床开发的用于治疗埃博拉病毒的GS-5734对多种冠状病毒,包括SARS-CoV和MERS-CoV都有明显的抑制疗效,GS-5734的预防性早期治疗显著降低了肺病毒载量,改善了临床症状以及呼吸功能。
论文中的GS-5734是瑞德西韦(Remdesivir)的研发编号。论文研究中,为检验瑞德西韦即GS-5734的广谱抗冠状病毒能力,Ralph S. Baric等人使用反向遗传平台,基于病毒的基因序列,人工合成了7种冠状病毒,其中之一是WIV1,其它六种病毒是:
SARS-CoV(SARS病毒)、
MERS-CoV(中东呼吸综合症病毒)、
HCoV-NL63(人类冠状病毒NL63)、
HKU3(蝙蝠冠状病毒HKU3)、
HKU5(伏翼蝠冠状病毒HKU5)、
SHC014(蝙蝠冠状病毒rsSHC014,论文A-1的病毒主角)。
注:伏翼蝙蝠是一种拇指大小、约重4克的蝙蝠,发现于2006年,可能是香港独有的物种。
论文比较了诸多冠状病毒(包括WIV1)与SARS病毒、MERS病毒在nsp12辅助蛋白、spike蛋白(刺突蛋白)两个部分上的A.A. identity,并将比较结果以不同颜色形象直观地展示为下图(蓝绿色代表一致度高,红黄色代表一致度低)。
注:A.A.指Amino Acid,A.A. identity即氨基酸序列一致性或相似度。
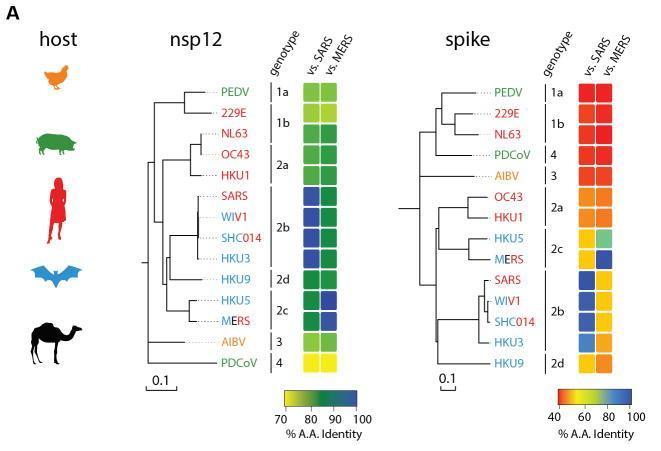
由图可见,不同冠状病毒刺突蛋白差异较大,而它们的nsp12蛋白则高度保守(一致程度高,变异程度低)。论文指出:nsp12蛋白是广谱抗冠状病毒药物的适宜靶点。
论文实验检测了GS-5734对两种冠状病毒MERS、SARS的抑制功效,实验结果以下图展示。
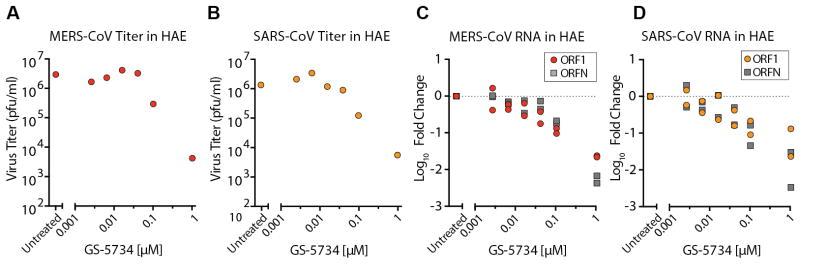
由图A、B可见,随着GS-5734使用浓度的增加,HAE细胞培养物中MERS、SARS病毒的滴度显著下降。
由图C、D可见,随着GS-5734使用浓度的增加,HAE细胞培养物中MERS、SARS病毒ORF1、ORFN两种辅助蛋白的检测值显著下降。
图A、B、C、D的横坐标都是GS-5734的单位使用剂量(浓度);
图A、B的纵坐标是病毒的滴度(每毫升培养物中含有的具有生物活性的病毒颗粒数);
图C、D的纵坐标分别是ORF1、ORFN两种辅助蛋白RT-PCR相对检测值的对数值。以C图为例,以未施用GS-5734时的检测值为一个基准单位,则当GS-5734施用浓度为1μM时,MERS病毒ORF1蛋白的检测值下降到约10^-2(10的负2次方)个单位(即施用前后检测值的比值约为10^-2),将相对检测值以10为底取对数,所得纵坐标值约为-2。
注:HAE细胞,即human airway epithelium cells,人气道上皮细胞。
论文接着又实验检测了GS-5734对另外五种冠状病毒(包括WIV1)的抑制能力。仍然使用HAE细胞培养各病毒,与上一组实验不同的是,每个病毒的HAE培养物都一式两份,实验结果见下图。

图B中各坐标子图的横坐标都是GS-5734的使用浓度。
上排五个坐标图的纵坐标都是HAE培养物中相应病毒的滴度。由图可见,随着GS-5734使用浓度的增加,培养物中各病毒的滴度显著下降。
下排各坐标图的纵坐标为HAE培养物中各病毒ORF1、ORFN蛋白RT-PCR相对检测值的对数值。由图可见,随着GS-5734的使用浓度的增加,各病毒ORF1、ORFN蛋白的检测值显著下降,当使用浓度为10μM时,相比未施用时,五病毒两辅助蛋白的检测值下降了100~100000倍。
Ralph S. Baric是该论文的两个通讯作者之一;论文的第一至第五作者,全都是北卡罗来纳大学教堂山分校的Baric团队成员,其中第四作者,就是论文A-1、A-2的第一作者,Ralph S. Baric团队的重要人物Vineet D. Menachery(维内特·德梅纳赫里),他也是论文A-4(见下)的第三作者。
2020年1月21日,新冠疫情发生不久,武汉病毒研究所抢先申报了一项专利《瑞德西韦抗2019新型冠状病毒的用途》,这是一项瑞德西韦用途专利,武汉所试图通过PCT(专利合作协定)途径将该专利从中国推及全球主要国家,使中国因此专利而受益。武汉病毒研究所凭什么判断瑞德西韦可能对治疗新冠病毒有效?因为新冠病毒出自他们之手吗?是他们未卜先知吗?当然都不是,原因很简单,因为他们知道Ralph S. Baric等人2017年6月发表的这篇论文,知道瑞德西韦的广谱抗冠状病毒功效。
论文A-4
2018年12月19日,Ralph S. Baric团队、国家过敏和传染病研究所(所长为安东尼·福奇)的两个下属机构(病毒学实验室、落基山兽医分会)在著名国际开源出版期刊MDPI(Multidisciplinary Digital Publishing Institute)联合发表了一篇论文: SARS-Like Coronavirus WIV1-CoV Does Not Replicate in Egyptian Fruit Bats(类SARS冠状病毒WIV1不会在埃及果蝠中复制)
https://www.mdpi.com/1999-4915/10/12/727/htm
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6316779/
注:埃及果蝠(Egyptian fruit bat,Rousettus aegyptiacus)是马尔堡病毒的天然宿主,也是所有丝状病毒的唯一已知宿主。
论文有以下要点:
1)WIV1病毒能有效利用埃及果福的ACE2进入果蝠细胞,感染果蝠的呼吸系统(鼻腔、肺)及胃、 肾脏和肠等器官,可观察到这些器官因感染而产生的明显的免疫反应;
注:新冠病毒也能感染人类的上述器官,WIV1与新冠的根本区别在于,WIV1的病毒骨架对人没有致病力,不会使人产生疾病症状。
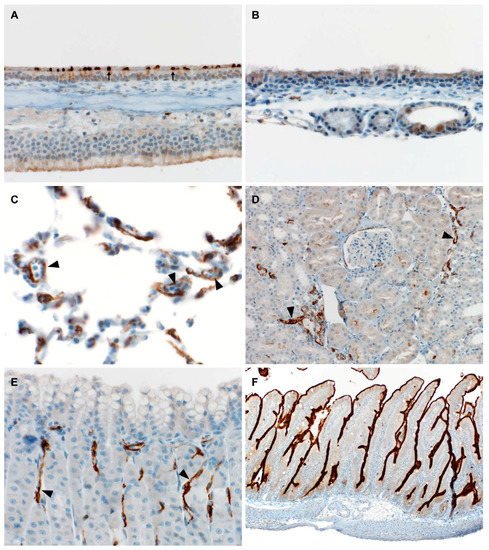
图示:WIV1感染使果蝠鼻甲(A)、气管(B)、肺(C)、肾(D)、胃(E)、肠(F)等器官、组织产生了不同程度、不同细节的免疫反应。
2)尽管WIV1可感染果蝠多处器官、组织,并引发免疫反应,但12只实验果蝠都没有表现出疾病迹象(如呼吸窘迫,厌食症或嗜睡),未检测到果蝠的体重减轻或体温变化。
3)在不同的感染后时段对实验果福实施安乐死,对以下诸多器官、组织进行病毒学和组织病理学分析:鼻甲、喉、咽、气管、肺、脑、眼、结膜、心、肝、脾、肾、膀胱、生殖器官、胃、近端和远端肠道、颈部淋巴结、肾上腺、皮肤和骨骼肌。
注:这表明,Ralph S. Baric团队认识到了WIV1病毒的泛器官、组织感染能力,新冠病毒也具有泛器官、组织感染能力。
4)感染后第三天,仅在果蝠咽部和鼻甲骨检测到了WIV1病毒的RNA,在其它各器官、组织中均未再检测到WIV1病毒的RNA(WIV1病毒感染了这些器官、组织,但在感染后,因为缺乏有效的持续复制、繁衍,它又从这些器官、组织中消失了)。
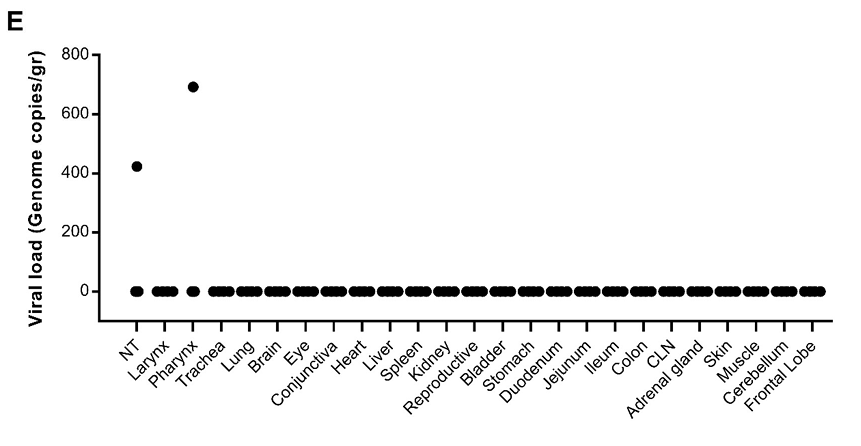
感染后第3天果蝠各器官、组织WIV病毒RNA载量统计图
5)实验表明,WIV1不会对果蝠造成强烈感染,不能引发可观察的临床症状;论文判断:WIV1在果蝠中可能只发生了一些低水平的病毒复制。
6)为对照WIV1的细胞感染能力,分别用SARS的刺突蛋白、MERS的刺突蛋白与VSV病毒的骨架,基于它们的基因序列,使用反向遗传平台合成了二种嵌合假病毒SARS-S、MERS-S;研究中使用的WIV1病毒毒株也是使用反向遗传平台,基于WIV1的基因序列人工合成、收获的。
注:VSV病毒,即vesicular stomatitis virus,水疱性口炎病毒。
7)使用三种转基因BHK细胞进行体外实验:表达人类ACE2的BHK细胞,表达埃及果福ACE2的BHK细胞,表达人类DPP4的BHK细胞。实验证明,WIV1及SARS-S都能感染前二种转基因BHK细胞,在感染后48小时能检测到细胞培养物中的病毒复制;而MERS-S则能感染表达DPP4的BHK细胞。实现结果见下图。
注:
BHK细胞,即Baby Hamster Syrian Kidney cells,叙利亚幼仓鼠肾细胞;
DPP4,即dipeptidyl peptidase IV,二肽基肽酶4,也称为CD26或腺苷脱氨酶复合蛋白-2,是一种丝氨酸外肽酶,调节多种肽(如生长因子、趋化因子和神经肽)的生物活性,在葡萄糖代谢中起主要作用。和ACE2一样,DPP4也是一种跨(细胞)膜糖蛋白,它是MERS病毒(中东呼吸综合症病毒)感染细胞时使用的受体。
图C:WIV1、SARS-S、MERS-S对四种BHK细胞的感染能力,每种BHK细胞培养物一式三份。
横坐标为四种BHK细胞:表达人类DPP4的BHK细胞、表达人类ACE2的BHK细胞、表达果蝠ACE2的BHK细胞、没有ACE2的BHK细胞;纵坐标为病毒复制滴度的对数值;
图C表明:WIV1、SARS-S可感染表达人或果蝠ACE2的转基因BHK细胞;MERS-S可感染表达人DPP4的转基因BHK细胞。
图D:WIV1对三种BHK细胞(表达人ACE2、表达果蝠ACE2,无ACE2)的感染情况,感染后0小时、48小时TCID(Tissue Culture Infective Dose,组织培养感染剂量)的对数值。图D亦说明,WIV1能有效感染两种转基因BHK细胞,并在感染后健壮复制。
Ralph S. Baric团队不仅对WIV1(rs3367)病毒做过反复、深入的研究,而且对另一纽带--冠状病毒刺突蛋白的关键氨基酸也做过极其频繁、极其深入、极其细致的研究。
(未完待续)























