(二)
是我在撒谎,还是他们在撒谎?
最危险的,不是自然界中的动物,而是那些在实验室中编辑、改造病毒基因,人为增强病原体致病能力、传播能力的人。能否树立这一常识,禁止或高度警惕、防范基因改造、病原体功能增益行为,并采取可靠、有效的措施(如严格的立法、完善的公民社会监督系统),关系到每一个人的安全,关系到我们子孙后代的安全、健康和幸福,关系到人类未来的命运。
我们需要真相。
接续:新冠,科学疯子设计的病毒集大成者(一)
展开后续内容之前,先贴一张冠状病毒结构示意图。
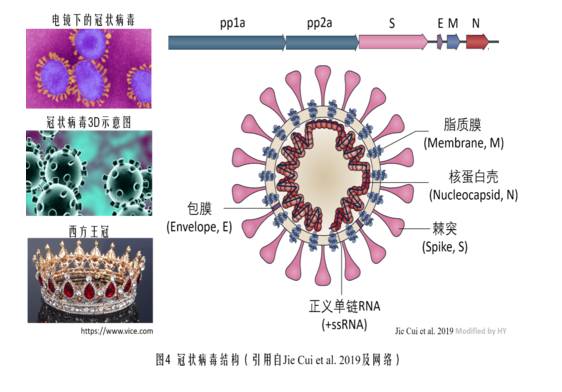
本文将聚焦新冠病毒的刺突蛋白三关节式组合铰链,介绍、展开论文依据,分析其人为设计性,并对相关设计嫌疑人进行初步探查。
II、刺突蛋白三关节式组合铰链设计
参考SARS-CoV、MERS-CoV(中东呼吸综合症冠状病毒)、 PEDV(猪流行性腹泻病毒)等病毒的简单铰链结构,为新冠刺突蛋白设计了非常精巧、灵活的(可能是前所未有、独一无二的)三关节式组合铰链结构,这组关节式铰链与人体髋、膝、踝三个关节的运动机制类似,它们有如下功能:
a) 当“关节”挺直时,刺突蛋白向上运动,RBD将暴露出来以便与宿主受体ACE2结合;
b) 当“关节”弯曲时,刺突蛋白向下运动,RBD将处于“躺卧”状态并隐藏在刺突蛋白三聚体头部之中,避免被宿主免疫系统或抗体药物搜索到。
c) 三个“关节”非同寻常的活动能力和自由度,使新冠刺突蛋白(及RBD)能够以不同高度、角度和姿态相当灵活地接触ACE2受体并与之结合,大大提高了感染宿主细胞的效率。
d) 新冠病毒逃避抗体药物结合的能力,以及逃避免疫系统搜索、打击的能力远超SARS病毒,重要原因之一,就是它有SARS所没有的,SARS的简单铰链所无法比拟的三关节式组合铰链。
上述“刺突蛋白三关节式组合铰链”结构及功能归纳自以下三篇论文。
论文一。
2020年3月13日,美国德克萨斯大学奥斯汀分校Jason S McLellan团队,及美国国家过敏和传染病研究所的研究人员在《Science》杂志上发表了一篇论文:Cryo-EM Structure of the 2019-nCoV Spike in the Prefusion Conformation(膜融合前构象中2019-nCoV刺突蛋白的冷冻电镜结构)
https://science.sciencemag.org/content/367/6483/1260
这篇论文在上篇文章中简单介绍过,当时是用来说明RBD5个关键氨基酸设计所取得的如下设计效果: 2019-nCoV(新冠,SARS-CoV-2的旧称)S蛋白与hACE2的结合亲和力,比SARS-CoV S蛋白与hACE2的结合亲和力高10-20倍。
注:S蛋白即Spike蛋白,即刺突蛋白或棘突蛋白。
这次,我们较全面地介绍一下该论文的要点(其中b、c两项与“三关节式组合铰链”有关):
a) 确定了(膜)融合前构象中2019-nCoV刺突蛋白三聚体的3.5埃分辨率冷冻电子显微镜结构;
b) 新冠刺突蛋白可通过铰链式构象运动,使S1亚基呈现出两种状态:向下构象与向上构象。向下构象对应着不可接近宿主细胞受体的状态(隐藏RBD的状态),向上构象则对应着可接近受体的状态(暴露RBD的状态)。刺突蛋白三聚体可通过向上旋转将向下构象转变为向上构象。通过两种构象的切换,新冠病毒可隐藏或暴露与ACE2结合的RBD部位。
c) 类似的铰链式构象运动在以下三种病毒的结构特征研究中也曾发现过:与新冠同谱系的β谱系冠状病毒SARS-CoV、MERS-CoV,关系较远的α谱系冠状病毒PEDV(Porcine epidemic diarrhea virus,猪流行性腹泻病毒) 。
d) 表面等离子体共振量化研究表明,新冠S蛋白(刺突蛋白)与ACE2的结合亲合力,比SARS-CoV S蛋白与ACE2的的结合亲和力高10至20倍;
e) 2019-nCoV刺突蛋白、ACE2结合后形成的复合物,与SARS-CoV刺突蛋白、ACE2结合后形成的复合物非常相似;
f) 对SARS-CoV有效(能代替ACE2强力结合SARS的RBD)的三种单克隆抗体(S230、m396 和 80R)对2019-nCoV都无效(不能有效结合新冠的RBD)。
论文二。
2020年10月9日,德国海德堡欧洲分子生物学实验室、法兰克福马克斯普朗克生物物理研究所、法兰克福歌德大学生物物理研究所等机构的一组德国科学家(Gerhard Hummer等)在《Science》杂志发表了一篇论文:In situ structural analysis of SARS-CoV-2 spike reveals flexibility mediated by three hinges(原位结构分析揭示了由三个铰链介导的新冠刺突蛋白的灵活性)
https://science.sciencemag.org/content/370/6513/203
论文部分要点归纳如下:
a) 新冠刺突蛋白刺突头部与病毒包膜之间的茎干部分似乎是动态的,电子断层扫描图像表明,头部之下、跨膜区域之上的刺突蛋白茎干中存在三个柔性铰链。
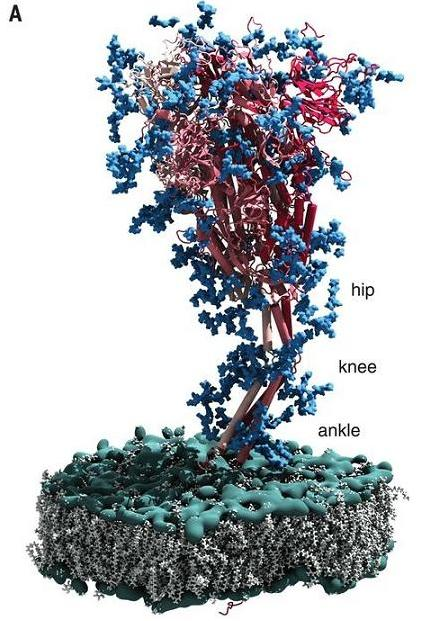
b) 这三个铰链与人类的髋、膝、踝三个关节类似,不妨称之为新冠刺突蛋白的髋关节、膝关节和踝关节。三个关节中,膝关节的可屈曲幅度最大,其次是踝关节,髋关节可屈曲幅度最小。通过三个关节的屈曲或挺直,刺突蛋白可侧移(横向位移)、倾斜、或直立,可调节其头部RBD的空间位置、高度和活动方向,甚至刺突蛋白的头部及RBD可贴近病毒包膜,处于倒伏的状态。
注:新冠刺突蛋白的踝关节位于S2蛋白的跨膜区域之上并贴近病毒包膜。论文没有明确指出另外两个关节的准确位置,结合论文有关内容,我的推测是:髋关节大致位于S1蛋白的三聚体头部之下,膝关节可能位于S1蛋白、S2蛋白的连接处附近。
c) 新冠刺突蛋白被相当庞大的聚糖链装饰,它的表面被这些广泛存在的N-糖基化位点所覆盖;髋、膝、踝三个关节处的N-糖基化覆盖、装饰情况尤为显著。这三个部位的N-糖基化装饰可能有助于保护功能重要的铰链免受抗体结合并保持它们的灵活性。
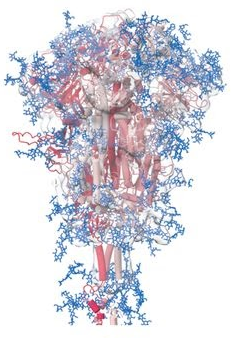
新冠刺突蛋白被N-糖基化位点(聚糖链)覆盖、装饰示意图。兰色图案代表N-糖基化位点(聚糖链)。
d) 三个柔性关节赋予的刺突蛋白的运动自由度可能有助于新冠病毒逃避抗体与其RBD的结合;
e) 三个柔性关节赋予的刺突蛋白的运动自由度还可能使新冠病毒便于接触宿主细胞相对平坦的(细胞膜)表面,并有助于其RBD以更高的亲和力,更灵活的姿态,更有效地结合细胞表面的ACE2受体。
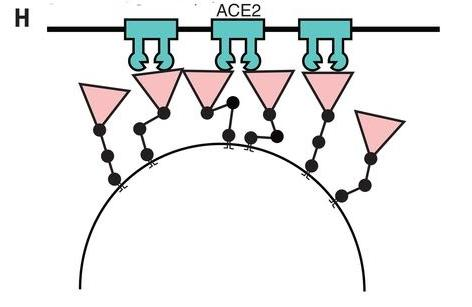
关节式铰链促进刺突蛋白与受体接合示意图。图中的刺突蛋白能以不同的高度、角度、姿态灵活地接触、结合ACE2受体。
f) 就我们所知,与新冠刺突蛋白这种广泛的(注:高度自由的)灵活性相当的特性,其他I类融合蛋白(注:冠状病毒刺突蛋白也是一种I类融合蛋白),包括HIV env、流感HA或Ebola GP,都尚未报道过,尽管流感HA的短接头结构允许高达25°的弯曲。(注:即,含其它I类融合蛋白的病毒可能都没有类似新冠的三关节结构)
注:HIV env,指艾滋病病毒(HIV)表面包膜糖蛋白Env三聚体,它介导HIV病毒与宿主细胞发生膜融合,是HIV-1疫苗研究的重要靶点;
流感HA,即流感病毒血球凝集素蛋白(HemAgglutinin,HA),它是流感病毒表面的一种囊膜蛋白,是流感病毒结合宿主细胞受体的主要工具,相当于冠状病毒的刺突蛋白;
Ebola GP,指埃博拉病毒表面的包膜糖蛋白(glycoprotein,GP),它介导Ebola病毒与宿主细胞发生膜融合,作用与HIV env类似。
HIV病毒属于逆转录病毒科,慢病毒属; 流感病毒属于正黏液病毒科,下分甲、乙、丙、丁四个属;Ebola病毒属于丝状病毒科,埃博拉病毒属。它们都不属于冠状病毒科,都不是冠状病毒。
新冠刺突蛋白的这种三关节式组合铰链结构应该是首次在病毒研究中发现。从论文一的相关引用论文判断,SARS-CoV、MERS-CoV、PEDV三个病毒刺突蛋白中的铰链很可能都是简单的单一铰链,因为被引用论文无一指出相关病毒刺突蛋白中存在一个以上的铰链(hinge);论文二要点f)指出,含其它I类融合蛋白的非冠状病毒(HIV、流感、Ebola)都未报道过类似的三关节式组合铰链结构。那么,同样含刺突蛋白这种I类融合蛋白的其它冠状病毒(包括SARS-CoV、MERS-CoV、PEDV)是否有类似结构呢?如果之前有论文报告过类似的三关节式组合铰链结构,无论其是否发现于冠状病毒,我相信,论文一、论文二,及稍后将介绍的论文三的作者们一定会指出来,这么重要的发现,他们不会全都不知道。
因此,新冠刺突蛋白的三关节式组合铰链结构,不仅应该是首次在病毒研究中发现,而且有可能在病毒中是独一无二的(截止目前)。
新冠刺突蛋白的三关节式组合铰链结构,是无人为干预地自然演化产生的吗?理论上存在这种可能性。但无论通过自身变异或重组,自然演化、获得或产生如此复杂、精巧的结构必然要经历漫长的岁月,留下由简单到精巧,由低级到高级的阶段性演化印迹。新冠刺突蛋白的铰链不同于SARS等病毒的简单铰链,它含三个铰链,而且,这三个铰链不是彼此无关的,它们能高度协调地配合工作。突如其来地从简单铰链“演化”出三关节式组合铰链,看不到任何类似的高级结构,看不到任何过渡性的中间演化产物,这样的演化太神奇、太不可思议了。
新冠病毒刺突蛋白的三关节式组合铰链结构,可能是随机性、无目的自然演化的结果吗?
来历不明的新冠病毒在“自然演化”过程中完成的不可思议的奇迹是不是太多了一点?
论文三。
2020年5月26日(first published May 6, 2020),美国明尼苏达大学李放团队在美国科学院院报(PNAS)发表了一篇论文:Cell entry mechanisms of SARS-CoV-2(新冠病毒的细胞进入机制)
https://www.pnas.org/content/117/21/11727
论文揭示了新冠病毒感染人体细胞以及免疫逃逸的机制。与“刺突蛋白三关节式组合铰链”相关的论文要点归纳如下:
a) 和SARS病毒一样,新冠的RBD也可以在站立姿势和躺卧姿势之间不断切换。站立姿势的RBD适合与受体进行结合;躺卧姿势的RBD非常不适合与受体结合,但可以使RBD隐藏起来逃避免疫系统的搜索、攻击或抗体药物的结合。
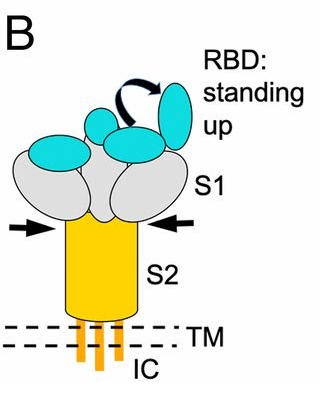
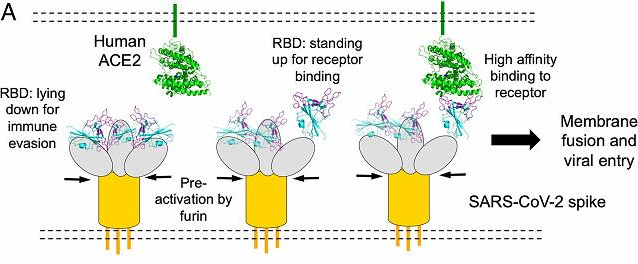
b) Cryo-EM(低温电子显微镜或冷冻电镜) 研究表明,SARS刺突蛋白RBD处于站立状态的频率更高,而新冠刺突蛋白RBD则更常处于躺卧状态。
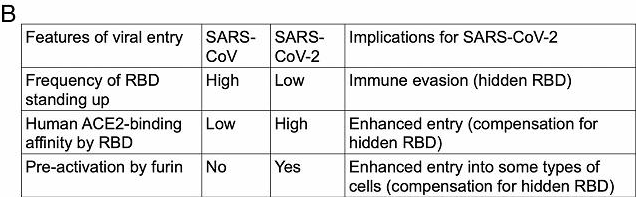
c) 表面等离子体共振(SPR)检测结果表明,新冠RBD与hACE2的结合亲和力显著高于SARS病毒RBD;但蛋白质下拉测定的结果却是:新冠刺突蛋白与hACE2的结合亲和力低于SARS刺突蛋白与hACE2的结合亲和力。
注:为什么两种测定的结果不一致?因为新冠有更多RBD处于躺卧状态,不适于结合hACE2,更多处于躺卧状态的RBD(或刺突蛋白)拉低了蛋白质下拉测定的结果。
d) 病毒通常使用两种主要策略隐藏RBD或刺突蛋白的其他关键部分,以避免触发宿主的适应性免疫反应。第一种是构象掩蔽,将RBD隐藏在峡谷(如小核糖核酸病毒)或凹陷的口袋(如HIV)等位置、结构处。第二种是聚糖屏蔽,利用聚糖簇来屏蔽、隐藏刺突蛋白的关键部分(如HIV、埃博拉病毒、丙型肝炎病毒)。新冠病毒将RBD隐藏在刺突蛋白三聚体头部内的方式属于构象掩蔽策略。
注:除构象掩蔽外,新冠病毒还应用了聚糖屏蔽,而且应用了两种聚糖屏蔽方式。第一种聚糖屏蔽是用大量的聚糖链(N-糖基化位点)覆盖、装饰刺突蛋白的三个关节式铰链,使其免受抗体结合。参见论文二要点c) ;第二种聚糖屏蔽是用O-Linked聚糖结构来形成糖链屏障。参见上篇文章内容摘要部分列举的第5项人为设计特征:O-Linked聚糖设计。
e) 最近的一项研究显示,
https://www.nature.com/articles/s41422-020-0305-x
SARS-CoV RBD诱导的小鼠血清也能以高亲和力结合SARS-CoV-2 RBD,但对SARS-CoV-2假病毒感染宿主细胞的中和作用却很差;相比之下,相同的血清不仅能以高亲和力结合SARS-CoV RBD,并且能有效地中和SARS-CoV假病毒对宿主细胞的感染(注:假病毒是人工改造或人工合成的,去除了致病力的缺陷型病毒,用于更安全、便利地模拟研究原生病毒的行为)。
注:为什么小鼠血清中的抗体能有效结合新冠RBD,却不能阻止新冠对细胞的感染?这应该是因为,(在实际感染环境中)新冠RBD有效地躲避了抗体,使抗体很少有机会与之接触并进而发生结合。上述研究结果或许可以表明,新冠隐蔽RBD,逃避抗体结合的“技能”,远比SARS高超。
f) 新冠的RBD隐藏“技能”还延迟了免疫反应,或使免疫反应不足。
注:这应该是新冠潜伏期较长的原因之一。
g) 新冠逃避宿主免疫系统监视、搜索、打击的能力也明显比SARS出色,这可能是许多新冠患者只能产生低水平的抗体并长期患病的原因之一。
h) 新冠隐藏RBD的技能加大了抗体研发的难度,有效的新冠抗体药物应能在新冠RBD的有限暴露期间快速锁定并非常紧密地保持与RBD的强力结合。
李放团队的这篇论文还(率先?)指出新冠病毒存在furin蛋白酶切位点,并实验证实了furin蛋白酶在新冠感染过程中的显著作用,论文同时实验确认了其它一些蛋白酶,包括TMPRSS2(跨膜丝氨酸蛋白酶2),及某些溶酶体组织蛋白酶在新冠感染中的作用。这些内容可能会在后续文章中引用、介绍。
谁设计了“刺突蛋白三关节式组合铰链”?
上篇文章指出,新冠设计者参照跨物种传播能力最强的病毒rs3367(WIV1),复用+替代rs3367的五个关键氨基酸,设计出了新冠病毒RBD的五个关键氨基酸。“RBD关键氨基酸设计”的最大设计嫌疑人是北卡罗来纳大学教堂山分校的国际病毒学顶级权威Ralph S. Baric(拉尔夫.巴里克)及其团队。
Ralph S. Baric团队对rs3367(WIV1)做过非常深入、反复的研究,包括功能增益研究。上篇文章已经介绍了部分与rs3367(WIV1)相关的Baric团队论文,但还非常不完备。有必要专门整理出一篇更全面的文章,例举、介绍Ralph S. Baric团队发表过的,改造rs3367(WIV1),或利用rs3367进行病毒改造的论文,及其它研究、涉及rs3367的论文;同时例举、介绍该团队对刺突蛋白进行改造的论文,包括使用刺突蛋白或其一部分进行病毒嵌合的论文,对RBD进行基因编辑和氨基酸替换的论文,对RBD外的S1蛋白其它部分进行基因编辑、氨基酸替换的论文,对S2蛋白进行基因编辑、氨基酸替换的论文等。在关注候选论文的过程中,我发现,Ralph S. Baric及其团队发表过的涉及病毒改造(包括功能增益改造)或病毒人工合成的论文比我之前已知的要多得多,较完备地搜集、阅读、归纳、总结相关论文将花费大量的时间和精力。但我稍后将进行这一工作,即使文章的初始版本只能总结、展示Ralph S. Baric及其团队相关论文中的一部分。
Ralph S. Baric或其团队成员是否也有设计“新冠刺突蛋白三关节式组合铰链”的嫌疑?答案是肯定的。我先提供一组证据。
上篇文章介绍了Ralph S. Baric团队2016年3月14日发表于PNAS(Proceedings of the National Academy of Sciences of the United States of America,美国国家科学院院刊)的以rs3367(WIV1)为研究主角的病毒嵌合-功能增益论文(用rs3367即WIV1的刺突蛋白+SARS-CoV-MA15的骨干合成了人、小鼠致病性嵌合病毒WIV1-CoV):SARS-like WIV1-CoV poised for human emergence(类SARS冠状病毒WIV1-CoV有产生人类流行疫情的潜在危险)
https://www.pnas.org/content/113/11/3048
论文“Discussion”部分指出:除受体结合域(RBD)外,S1蛋白的其余部分及S2蛋白的变化也可能在冠状病毒感染、传播、发病机制中发挥关键作用。这些刺突蛋白区域可能会影响蛋白酶的靶向性,刺突的切割特性或扩展性,它们的某些变化可能使病毒获得更健全的感染能力(原文:Whereas the receptor binding domain had garnered the most interest, changes in the remaining portion of S1 as well as the S2 portion of spike may also play a critical role in facilitating CoV infection, transmission, and/or pathogenesis.Differences in these regions of spike may yield increased protease targeting, enhanced spike cleavage, and/or expanded tropism leading to more robust infection for the epidemic SARS strains)。
这段文字实际上提出了以完善、健全病毒感染能力为目标的病毒改造建议和实验方向,即:进一步改造RBD之外的刺突蛋白部分,如改造S1蛋白RBD外的部分,或改造S2蛋白,改造产生的变化可能使刺突蛋白更有针对性(靶向性、目的性)地与蛋白酶发生作用,可能增加刺突蛋白的切割(被蛋白酶切割)特性,可能使刺突蛋白更具扩展性。
令人惊奇的是,这三项病毒改造建议兼预测,即与蛋白酶作用的针对性、刺突蛋白新的酶切特性、刺突蛋白的扩展性(及灵活性),全都在新冠病毒中实现了!它们都是通过改造刺突蛋白的RBD外部分实现的。其中,与蛋白酶作用的针对性、刺突蛋白的扩展性(及灵活性)这二项特性,都是“刺突蛋白三关节式组合铰链设计”所赋予的。三关节式组合铰链横跨S2蛋白和S1蛋白的RBD外部分,它正是通过对这两部分施以基因改造而实现的,进而赋予了新冠与蛋白酶作用的针对性,提高了刺突蛋白的扩展性(、灵活性)。
关于新冠刺突蛋白的扩展性、灵活性。由论文二、论文三相关要点可知,新冠刺突蛋白或其RBD能够弯曲、挺直,收缩、伸展,倾斜(甚至倒伏或躺卧)、直立,变换方向,这表明,三关节式组合铰链设计大大提高了新冠刺突蛋白的扩展性和灵活性;
关于新冠与蛋白酶作用的针对性。同样由论文二、论文三可知,新冠RBD“平时”可以非常有效地隐蔽起来,逃避人类抗体或抗体药物的结合,逃避免疫系统的搜索和攻击,在需要时,它又可以暴露出来,以不同的高度、角度、姿态灵活、高效地接触、结合ACE2受体。这表明,三关节式组合铰链设计也高质量地赋予了新冠RBD与蛋白酶(ACE2)作用、结合的针对性或者说靶向性、目的性。注意,ACE2(Angiotensin Converting Enzyme2,血管紧张素转换酶2)受体,本身就是细胞表面的一个膜蛋白酶。
刺突蛋白新的切割(酶切)特性,则是S1、S2蛋白交界处的furin酶切位点赋予的,这涉及新冠病毒的另一组人为设计特征,即上篇文章内容摘要中的第3项-“furin酶切位点设计”,它将在后续文章中聚焦和展开。
Ralph S. Baric(团队)2016年3月功能增益论文中提出的三个病毒改造建议,在新冠病毒中全都出色地实现了,这又是偶然的巧合吗?
(未完待续)












