接續:“萬能”受體適配器--新冠S蛋白 0
有些事實需要迴避,不便公開申明、反覆強調,不便廣而宣告,廣為討論,那等於將真相搬出隱蔽、黑暗的角落,擺放到沒有遮蔽的陽光下。
新冠病毒具有泛器官、泛組織感染、破壞能力,新冠病毒能夠感染、損傷幾乎所有的人體器官、人體組織。未見權威組織、權威人士專門指出、明確強調這一點,但人們能夠從新冠致病情況的紛紜報道中自行總結出這一事實。已論文報告或媒體報道的新冠病毒感染、致病部位遍及人體的呼吸系統、消化系統(包括胃腸道、肝臟、胰腺)、血液循環系統(包括心臟、血管、紅細胞、白細胞)、泌尿系統(包括腎臟、膀胱等)、淋巴免疫系統(包括T細胞、樹突細胞、單核細胞和巨噬細胞)、內分泌系統、生殖系統、大腦神經系統(包括腦組織、神經元、嗅覺、味覺細胞)。。。
公眾能夠自行認識到,新冠病毒的泛器官、泛組織感染、破壞能力;但普通公眾難以知道,難以想象到,新冠病毒這一外在能力背後所蘊含的一組震古爍今的內在能力:新冠病毒的受體結合蛋白(S蛋白)能夠結合超過30種人類細胞受體(人類細胞膜蛋白)!
坐擁30種以上人類細胞受體不是新冠病毒非凡受體結合能力的全部。新冠病毒不僅集眾多冠狀病毒、眾多非冠狀病毒的受體結合能力於一身,而且兼具細菌分泌物、人體蛋白、人類藥劑的受體/蛋白結合能力。比如,新冠病毒S蛋白結合TCR(T
Cell
Receptor,T細胞受體)的多肽,在序列和空間結構上與葡萄球菌腸毒素B(金黃色葡萄球菌的代謝產物)高度相似;再比如,新冠病毒S蛋白結合NRP1(神經纖毛蛋白-1)受體的Cendr多肽,與NRP1的一種體內天然結合配體--VEGF-A(血管內皮生長因子-A,一種人體內的二聚體糖蛋白),在NRP1的結合結構、結合機制上非常相似;又比如,新冠病毒S蛋白結合GRP78(葡萄糖調節蛋白78)受體的四個多肽區域,與一種腫瘤化療的藥物載體Pep42(Pep42是GRP78的特異性結合配體)在序列上、在空間環狀性質上,在物理、化學性質上都具有相似性。
由於新冠病毒能夠結合超過30種人類細胞受體--人類細胞膜蛋白,由於這些膜蛋白駐留的細胞分布在各種人體器官、組織中,因此,各個器官、組織中的每種人體細胞的表面,幾乎總有一種或多種新冠病毒可結合的膜蛋白受體,進而,幾乎每一種人體細胞,都可被新冠病毒經由一種或多種受體結合途徑感染。S蛋白極其廣泛、驚人的受體結合能力,是新冠病毒具有泛器官、泛組織感染、破壞能力的最關鍵原因。
新冠病毒30種以上的受體結合能力,是前所未見的,是其它所有冠狀病毒,其它所有病毒難以企及、難望頸背的。
如果新冠病毒來自自然、來自動物,那麼它是前無古人的超級自然演化天才,它在遠離人類的地方,無師自通,通過隨機性的、無目的的自然演化,自然而然地演化出了史無前例的超級廣泛、超級驚人的人類受體結合能力。它自然演化出了近親病毒無一具有的20多種人類受體結合能力,它自然演化出了眾多非冠狀病毒的人類受體結合能力,它還自然演化出了細菌分泌物、人類蛋白、人類藥劑的人類受體結合能力、結合結構。這樣的自然演化真的自然嗎?
如果新冠病毒來自自然,來自動物,那麼,剛剛在人群中出現的這種病毒,為什麼對人體如此熟悉,如此瞭如指掌?為什麼對結合人體膜蛋白受體,對感染、破壞人體細胞、組織、器官,這種病毒如此輕車熟路、得心應手、遊刃有餘?
無法解釋、無法面對,只能迴避、躲閃、拖延、淡化、冷處理、裝糊塗、隱瞞、混水摸魚。你的聲音難以得到傳播和討論,甚至得不到反駁。對某些人來說,強權即公理;對某些人來說,陣營、立場、利益決定是非;通常人們願意相信,一種鮮有呼應、過於孤獨的訴說應該是虛構的或臆想的,不會是事實、真相。儘管反面的例子在人類歷史上一再發生。
下面將一一介紹新冠病毒S蛋白可結合的人類細胞受體,每一種受體都將給出論文依據。如果某些論文的介紹比較冗長,讀者可一目十行或直接跳過它們,論文標題往往已可說明問題。論文細節對筆者和某些讀者或許有參考價值。
1、ACE2
ACE2:Angiotensin-Converting
Enzyme
2,血管緊張素轉換酶2,最早確認的、眾所周知的新冠病毒受體。ACE2較廣泛地存在於脊椎動物的呼吸、消化、血液、泌尿、生殖、視覺等系統的眾多器官、組織內,但在新冠病毒的首要感染部位--呼吸道和肺部,ACE2的表達量(含量)卻相當低或僅有一小部分細胞表達,在新冠病毒的另外一些感染部位,如肝臟,腦和血液中,甚至檢測不到ACE2表達。
ACE2也是SARS-CoV和HCoV-NL63的主要受體,HCoV-NL63是有人類致病能力的七種已知冠狀病毒之一,可引發普通感冒。
對ACE2就不多作展開了。
2、DPP4(CD26)
DPP4:dipeptidyl
peptidase
IV,二肽基肽酶4,是一種II型(N端在胞內,C端在胞外)單次跨膜蛋白,也是一種絲氨酸蛋白酶。DPP4也叫CD26(cluster of
differentiation 26,表面抗原分化簇26,白細胞/T細胞活化抗原26),它還有adenosine deaminase (ADA)
complexing protein-2 (腺苷脫氨酶複合蛋白-2)等其它名稱。
DPP4在眾多人體器官、組織中廣泛分布,如下呼吸道(支氣管)、肺(特別是肺成纖維細胞)、胃腸道、肝臟、腎臟(近端腎小管)、胰腺、胸腺、前列腺、淋巴結、胎盤、血漿(及其它組織液)、中樞神經系統、受傷皮膚、肌肉等等;DPP4也廣泛表達於各種活化的免疫細胞,如CD4(+)和CD8(+)T細胞、B細胞、自然殺傷細胞、樹突狀細胞和巨噬細胞。
DPP4在血糖控制(是腸降血糖系統的關鍵調節因子)、細胞遷移、增殖、免疫等多種生理過程中發揮作用;DPP4通過調節細胞因子、趨化因子和肽激素的產生,參與免疫、炎症反應並參與、影響多種疾病的發病機制。其中一個例子是,糖尿病患者潰瘍部位組織DPP4
水平升高是創面難以癒合的原因。
DPP4是MERS-CoV(Middle East Respiratory Syndrome
Coronavirus,中東呼吸綜合症冠狀病毒)的主要受體。MERS屬於冠狀病毒β譜系的C支系,新冠屬於冠狀病毒β譜系的B支系,雖然同處β譜系,但二者親緣關係遙遠,基因差異巨大,二者全基因組序列一致性僅為53.5%。雖然遺傳關係遙遠,基因差異巨大,但新冠病毒依然兼容並蓄地“繼承”、兼具了非近親MERS的DPP4受體結合能力。
新冠病毒(SARS-CoV-2)S蛋白有較強的DPP4結合親和力,DPP4可能是新冠病毒的受體或共受體。
論文依據一:
The MERS-CoV Receptor DPP4 as a Candidate Binding Target of the SARS-CoV-2 Spike
MERS-CoV受體DPP4是SARS-CoV-2刺突的候選結合靶點
https://www.cell.com/iscience/fulltext/S2589-0042(20)30345-X
論文要點如下:
1、軟件模擬計算表明,SARS-CoV-2-S(SARS-CoV-2的S蛋白,Spike蛋白)可以較高的結合親和力結合DPP4,SARS-CoV-2-S與DPP4的結合親和力略低於MERS-CoV-S與DPP4,及SARS-CoV-2-S、SARS-CoV-S與ACE2的結合親和力。如下圖所示:
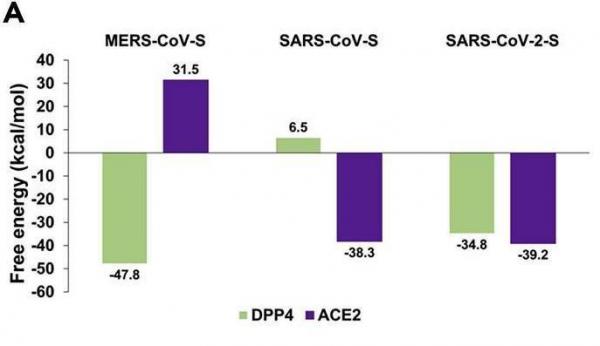
三種病毒S蛋白RBD與兩種受體的結合自由能
RBD:Receptor Binding Domain,受體結合域,是S蛋白S1亞基的一個子區域。
結合自由能(binding
free
energy)大體是兩個分子/蛋白結合後的總能量與結合前總能量的差值。自髮結合的兩個分子/蛋白不需要外部能量(類似磁鐵相異的兩極),其結合過程釋放能量,結合後二者的總能量降低,二者的結合自由能為負。結合自由能的絕對值等於解開結合(解離)時所需的外部能量。結合自由能越小,即負值的絕對值越大,越容易自髮結合,結合親和力越強,結合越穩固,解離所需的能量也越高。在上圖中,MERS-CoV-S與DPP4的結合親和力最強。
2、DPP4結合SARS-CoV-2-S的氨基酸殘基,與DPP4結合MERS-CoV-S的氨基酸殘基是相同的,即SARS-CoV-2-S、MERS-CoV-S與相同的DPP4殘基作用、結合。如下圖所示:
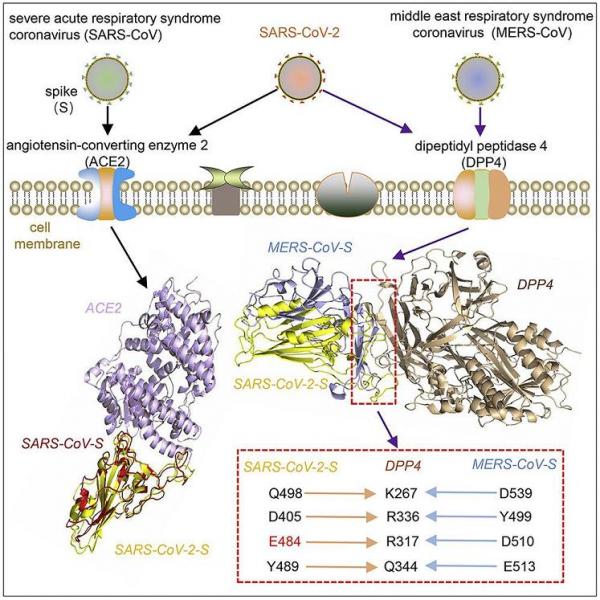
新冠兼具SARS(ACE2)、MERS(DPP4)的受體結合能力;
右下紅色虛線框顯示,新冠、MERS與4個相同的DPP4氨基酸殘基作用、結合。
筆者註:層出不窮的新冠巧合。SARS-CoV-2-S、MERS-CoV-S恰好共用相同的DPP4結合殘基,這可能意味着,有人參照MERS-CoV-S與DPP4的作用機制,設計出了可與同一組(4個)DPP4氨基酸作用、結合的另一套氨基酸,並將這套氨基酸應用到了SARS-CoV-2-S的RBD之中。
3、負責與DPP4作用、結合的四個SARS-2(RBD)關鍵氨基酸(殘基)D405、E484、Y489、Q498,其中的二個D405(天冬氨酸)、Y489(酪氨酸)在SARS-CoV中的對應氨基酸與它們相同;另外的兩個E484、Q498在SARS-CoV中的對應氨基酸與它們不同。E484(穀氨酸)在SARS-CoV中的對應氨基酸空缺(SARS-CoV氨基酸序列相對SARS-CoV-2氨基酸序列的一個缺失位點),Q498(穀氨酰胺)則在SARS-CoV中對應一個酪氨酸Y位點。如下圖所示:

SARS-CoV-2的四個DPP4結合氨基酸在SARS-CoV中的對應氨基酸
筆者註:這意味着,SARS-CoV如果在第一個差異位點突變新增穀氨酸E,並將第二個差異位點的酪氨酸Y突變為穀氨酰胺Q,那麼,就能演化出DPP4結合能力;或者,在第一個差異位點插入穀氨酸E,將第二個差異位點的酪氨酸Y替換為穀氨酰胺Q,就可以基於SARS-CoV的氨基酸序列,設計、改造出具有DPP4結合能力的新型冠狀病毒。
4、論文指出,雖然SARS-CoV-2的S蛋白具有較強的DPP4結合親和力,但尚未實驗證實DPP4可獨立介導SARS-CoV-2對人體細胞的感染,因此,論文的結論是,DDP4可能作為SARS-CoV-2的候選結合靶點或共受體(協同受體)。
論文依據二:
Emerging COVID-19 coronavirus: glycan shield and structure prediction of spike glycoprotein and its interaction with human CD26
新出現的COVID-19冠狀病毒:刺突糖蛋白的糖鏈屏蔽和結構預測及其與人CD26的相互作用
https://www.tandfonline.com/doi/full/10.1080/22221751.2020.1739565
論文指出:COVID-19冠狀病毒S蛋白的S1結構域可能與人類CD26(即DPP4)相互作用,而CD26是劫持和毒力的關鍵免疫調節因子。
註:S蛋白的S1結構域即S蛋白的S1亞基,S1亞基也叫受體結合亞基,RBD是S1亞基的子區域。相應地,S2亞基也叫膜融合亞基,它富含融合肽,可介導病毒包膜與細胞膜、內體膜或溶酶體膜等細胞的膜結構發生膜融合以釋放病毒RNA,開啟病毒複製。
論文依據三:
Unraveling
the Interactions between Human DPP4 Receptor, SARS-CoV-2 Variants, and
MERS-CoV, converged for Pulmonary Disorders Integrating through
Immunoinformatics and Molecular Dynamics
通過整合免疫信息學和分子動力學,揭示人類DPP4受體、SARS-CoV-2變體和MERS-CoV之間的相互作用,聚焦治療肺部疾病
https://www.biorxiv.org/content/10.1101/2023.03.06.531252v1
論文指出:SARS-CoV-2的幾種變體Delta、δ、α和γ具有比原始毒株更強的DPP4結合能力,增強最顯著的是Delta變體,其DPP4結合親和力非常接近MERS-CoV的DPP4結合親和力;SARS-CoV-2的S蛋白與DPP4的相互作用影響病毒毒性,DPP4結合能力的增強更容易引發感染合併症。
論文依據四:
Circulating levels of soluble Dipeptidylpeptidase-4 are reduced in human subjects hospitalized for severe COVID-19 infections
因嚴重COVID-19感染而住院的人類受試者中可溶性二肽基肽酶4的循環水平降低
https://www.nature.com/articles/s41366-020-00689-y
論文指出:COVID-19患者的sDPP-4(soluble DPP4/serum DPP4,可溶形式的DPP4或血清中的DPP4)水平顯著降低;DPP-4在COVID-19感染中可能發揮調節作用,肥胖和2型糖尿病可能是導致重症的主要危險因素。
反對意見,這篇論文稱不支持DPP4(CD26)是SARS-CoV-2的重要受體。
Does
the SARS-CoV-2 Spike Protein Receptor Binding Domain Interact
Effectively with the DPP4 (CD26) Receptor? A Molecular Docking Study
SARS-CoV-2刺突蛋白受體結合域是否與DPP4 (CD26) 受體有效相互作用?一個分子對接研究
https://www.mdpi.com/1422-0067/22/13/7001
其它相關論文:
Role of Dipeptidyl Peptidase-4(DPP4) on COVID-19 Physiopathology
二肽基肽酶4(DPP4)在COVID-19病理生理中的作用
https://www.mdpi.com/2227-9059/10/8/2026
DPP-4 Inhibitors as a savior for COVID-19 patients with diabetes
DPP-4抑製劑是有糖尿病的COVID-19患者的救星
https://www.futuremedicine.com/doi/10.2217/fvl-2022-0112
Dipeptidyl peptidase-4 (DPP4) inhibition in COVID-19
COVID-19中的二肽基肽酶4(DPP4)抑制
https://link.springer.com/article/10.1007/s00592-020-01539-z
3、NRP-1
NRP-1/NRP1
:Neuropilin-1,神經纖毛蛋白-1,一種Ⅰ型(C端在胞內,N端在胞外)跨膜蛋白,是最早被發現的NRP家族成員,在人體多種組織(如呼吸道、心臟、血管、淋巴結、淋巴管和神經元等等)的上皮和內皮細胞中大量表達。Nrp-1還在自然調節性T細胞上高表達,是這類T細胞區別於誘導性調節性T細胞的標誌。
NRP-1與另一種神經纖毛蛋白NRP-2參與各種生理過程,包括免疫突觸形成、免疫應答調節、心臟發育、血管生成、淋巴管生成、神經元發育、神經嵴細胞遷移、調節生長因子信號傳導等等。NRP-1和NRP-2與癌症、神經系統疾病及心血管疾病的發病機制有關。
NRP-1也是EBV和HTLV-1的感染受體或細胞進入因子。
EBV:Epstein-Barr virus,愛潑斯坦-巴爾病毒,即人類疱疹病毒第四型,B淋巴瘤和鼻咽癌的致病因;
HTLV-1:Human T-cell lymphotropic virus type-1,人類T細胞嗜淋巴細胞病毒1 型,成人T細胞白血病的病原體。
就SARS-CoV-2而言,NRP-1是ACE2的輔助受體,當與ACE2同時存在於細胞表面時,NRP-1能大幅提升SARS-COV-2的感染能力。
論文依據一:
Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity
Neuropilin-1促進SARS-CoV-2細胞進入和感染
https://www.science.org/doi/full/10.1126/science.abd2985
論文要點摘錄如下:
1、SARS-CoV-2(假病毒)不能感染僅表達NRP1的人腎HEK-293T細胞(下圖未體現這一點),但當NRP1與ACE2及TMPRSS2同時在HEK-293T細胞中表達時,SARS-CoV-2對HEK-293T細胞的感染能力得到大幅提升(HEK-293T細胞自身不表達ACE2和NRP1,所用的是轉染了相應蛋白基因的細胞)。
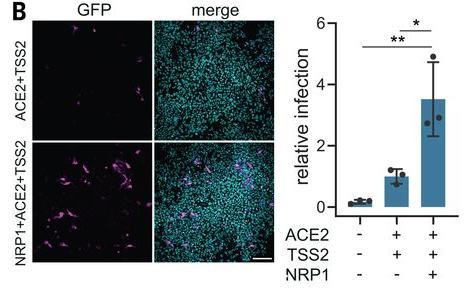
NRP-1顯著提升了SARS-CoV-2 對HEK-293T細胞的感染能力
依據論文,該研究所用的SARS-COV-2假病毒是用SARS-CoV-2的S蛋白與lentiviral(慢病毒,逆轉錄科慢病毒屬病毒)骨架嵌合製作的。最常用的慢病毒類型的假病毒骨架(載體)是去毒性HIV(艾滋病病毒)。
HEK293細胞,Human Embryonic Kidney Cells 293,人胚胎腎細胞293,一個衍生自人胚胎腎細胞的細胞系;
HEK293T細胞,在HEK293細胞中加入SV40(Simian vacuolating virus 40,猿猴空泡病毒40)大T抗原基因所得的再衍生細胞系。
TMPRSS2:Transmembrane
Serine Protease 2(跨膜絲氨酸蛋白酶2)/TransMembrane PRoteaSe, Serine
2(跨膜蛋白酶絲氨酸2),SARS-CoV-2、SARS-CoV的S蛋白激活因子,ACE2介導的SARS-CoV-2/SARS-CoV感染需要TMPRSS2作為S蛋白激活因子。
2、NRP1還促進了SARS-CoV-2假病毒對人結腸Caco-2細胞的感染,對照結果是,NRP1沒有促進VSV-G假病毒對Caco-2細胞的感染,如下圖所示:
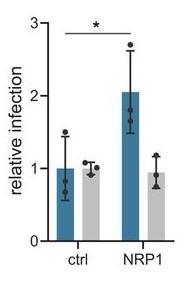
NRP1促進了SARS-CoV-2假病毒對Caco-2細胞的感染,但未影響VSV-G假病毒感染
圖中藍色條柱對應SARS-CoV-2假病毒,灰色條柱對應VSV-G假病毒,ctrl(對照組)使用的是未轉染NRP1基因的Caco-2細胞。
Caco-2細胞是一種人類結腸腺癌上皮細胞系細胞,Caco-2細胞自身表達ACE2。
所用VSV-G假病毒是用VSV(vesicular stomatitis virus,水泡性口炎病毒)的受體結合蛋白--G蛋白與慢病毒嵌合製作的。
3、NRP1單克隆抗體mAb3可顯著抑制SARS-CoV-2對表達NRP1的HEK-293T細胞(同時轉染表達ACE2、TMPRSS2和NRP1)的感染,mAb3並不抑制SARS-COV-2對不表達NRP1的HEK-293T細胞(只轉染表達ACE2、TMPRSS2)的感染;
4、對六位Covid-19患者的屍檢結果表明,其中五位患者的嗅覺上皮細胞被SARS-CoV-2感染。嗅覺上皮細胞的ACE2表達非常低,但NRP1的表達卻很富集。
論文依據二:
Neuropilin-1 is a host factor for SARS-CoV-2 infection
Neuropilin-1是SARS-COV-2感染的宿主因子
https://www.science.org/doi/full/10.1126/science.abd3072
論文指出:
1、(跨膜蛋白)NRP1的b1結構域(NRP1胞外域兩個凝結因子域中的一個)直接結合SARS-CoV-2-S的S1亞基的Cendr肽。Cendr肽由SARS-2
S蛋白氨基酸序列的第679~685氨基酸(679NSPRRAR685
,即679天冬酰胺N-絲氨酸S-脯氨酸P-精氨酸R-精氨酸R-丙胺酸A-精氨酸R)組成,它們恰好是S1亞基的最後七個氨基酸,Cendr肽的後四個氨基酸“RRAR”就是SARS-2的基本furin切割序列。
下面又是一處新冠巧合,這次不是SARS-2與MERS的巧合,而是SARS-2與人體蛋白的結構、功能巧合。
2、在NRP1結合特性、結合結構方面,SARS-CoV-2的Cendr肽與一種人體蛋白VEGF-A非常相似。一方面,二者與幾乎完全相同的一組NRP1-b1域氨基酸作用並結合;另一方面,Cendr肽、VEGF-A二者與NRP1-b1作用、結合的區域,在空間結構、空間形態上非常相似、吻合,如下圖所示:
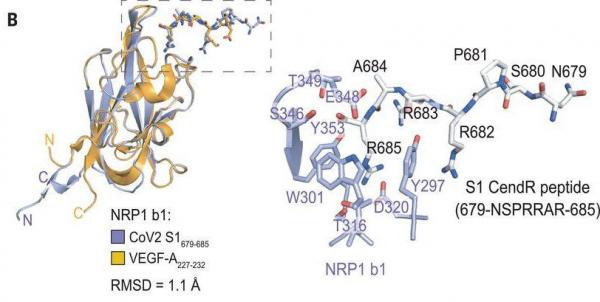
左圖:SARS-2的CendR肽(藍色)與人類的VEGF-A(黃色)方框區域的相似性、吻合性
右圖:NRP1的b1域與SARS-2 CendR肽的結合複合物示意圖;
3、CendR肽與NRP1 b1域之間的相互作用決定NRP1對SARS-CoV-2感染的促進,突變(替換)CendR肽中的氨基酸殘基(R685)或NRP1 b1域的氨基酸殘基(T316)都將喪失NRP1對SARS-CoV-2感染的促進作用;
4、NRP1 b1域、b2域的胞外域單克隆抗體mAb#3和mAb#1可抑制SARS-CoV-2對Caco-2細胞和Calu-3細胞(也是一種人肺腺癌細胞系)的感染;
5、選擇性NRP1拮抗劑EG00229可抑制SARS-CoV-2對Caco-2細胞的感染;
該論文就摘要介紹到此。思考、探討一下論文所指出的,SARS-CoV-2的CendR肽與人類蛋白VEGF-A的相似性。
VEGF-A,Vascular
Endothelial Growth Factor-A,血管內皮生長因子-A,也叫做血管通透因子(Vascular permeability
factor,VPF)或血管調理素(vasculotropin),是一種二聚體糖蛋白,發現於1983年,是發現最早、研究最多、在組織和細胞中含量最豐富的VEGF家族成員(該家族共七個成員)。
VEGF-A的一個重要特性就是它具有NRP1/NRP2的結合能力,特別是,VEGF-A有非常高的NRP1
b1域結合親和力,是NRP1 b1域的經典內源性(結合)配體(內源指二者都來自機體內)。2012年的如下論文解析了VEGF-A與NRP1
b1高結合強度的內在結構原因,並指出VEGF-A164(小鼠中的VEGF-A)與Nrp1的結合強度是其與Nrp2結合強度的50倍。
Structural Basis for Selective Vascular Endothelial Growth Factor-A (VEGF-A) Binding to Neuropilin-1
與Neuropilin-1結合的選擇性血管內皮生長因子-A(VEGF-A)的結構基礎
https://www.jbc.org/article/S0021-9258(20)48040-8/fulltext
SARS-2不僅模仿了MERS的DPP4結合能力、結合機制,還模仿了人類蛋白VEGF-A的NRP1-b1結合能力、結合結構。SARS-2的Cendr肽,與人類的VEGF-A蛋白,結合幾乎完全相同的NRP1-b1氨基酸,二者與NRP1-b1作用區域的空間結構、空間形態非常相似、吻合。試問,Cendr肽與VEGF-A的相似、相關性,前者對後者NRP1-b1結合能力、結合結構的模仿,是隨機、無目的自然演化的偶然結果嗎?
新冠病毒的結構、能力巧合與模仿,筆者已經介紹過很多,後繼文章中還將出現更多新冠專有的模仿和巧合。
4、MYH9(NMMHC-IIA)
MYH9
:Myosin Heavy Chain 9 ,肌球蛋白重鏈9,也叫non-muscle myosin heavy chain IIa
(NMMHC-IIA或NMHC-IIA),非肌性肌球蛋白重鏈IIa,是一種六聚體蛋白,由2個重鏈亞基MHC,2個鹼輕鏈亞基MLC和2個調節輕鏈亞基MLC-2組成。
MYH9蛋白空間形態示意圖
MYH9是一種運動蛋白,參與多種需要收縮力的過程,如胞質分裂,細胞遷移、極化和粘附,細胞形狀的維持和信號轉導等等。
MYH9在各種人體組織、細胞中廣泛表達,在眾多組織、細胞中高度表達,包括病毒組織、細胞,特別是各種癌細胞。
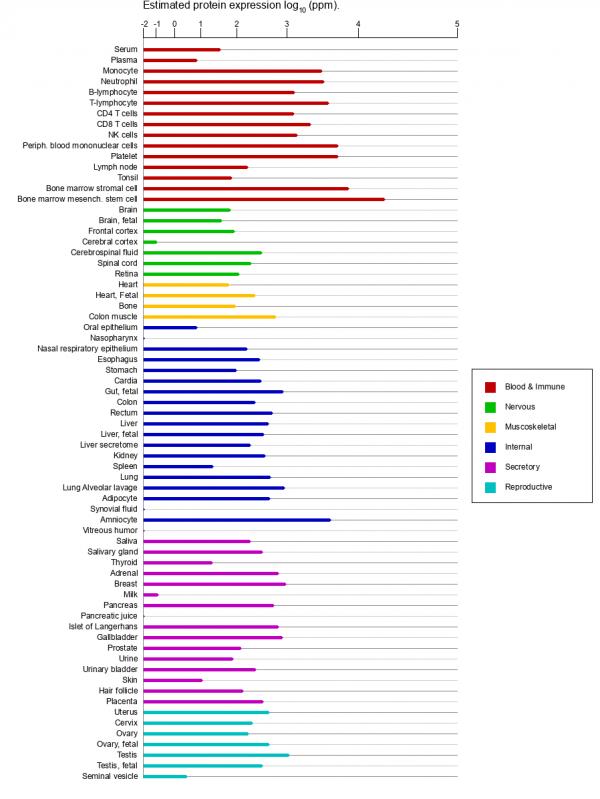
MYH9在正常組織、細胞中的表達情況
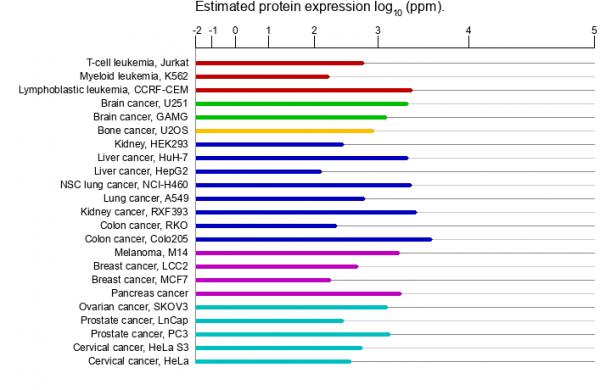
MYH9蛋白在病理組織、細胞中的表達情況
以上三張資料圖摘自:
https://www.genecards.org/cgi-bin/carddisp.pl?gene=MYH9
MYH9也是HSV-1(herpes
simplex virus-1,單純疱疹病毒1)、EBV(Epstein-Barr
virus,愛潑斯坦-巴爾病毒)、PRRSV(Porcine Reproductive and Respiratory Syndrome
Virus,豬繁殖與呼吸綜合症病毒)、SARS-CoV、MERS-CoV等病毒的功能受體或感染促進因子。
對SARS-CoV-2而言,MYH9是ACE2的輔助受體或共受體,可顯著提升ACE2依賴性感染,對SARS-CoV-2感染ACE2低表達的細胞尤為重要;MYH9對SARS-CoV-2感染的促進作用依賴ACE2,但獨立於ACE2感染途徑的二個S蛋白激活因子TMPRSS2(跨膜絲氨酸蛋白酶2)和CatB/L(cathepsin
B and L,組織蛋白酶B和L)。
論文依據:
Nonmuscle myosin heavy chain IIA facilitates SARS-CoV-2 infection in human pulmonary cells
非肌肉肌球蛋白重鏈IIA促進人肺細胞中的SARS-CoV-2感染
https://www.pnas.org/doi/10.1073/pnas.2111011118
論文要點如下(略去了少數不易簡明理解的要點):
1、NMMHC-IIA(MYH9)是ACE2的輔助受體,是促進SARS-CoV-2感染人肺細胞的關鍵宿主因子,也是泛冠狀病毒感染的關鍵宿主因子。
2、敲除A549細胞和Calu-3細胞中的MYH9基因顯著減少了SARS-CoV-2假病毒對這兩種細胞的感染,內源性MYH9(細胞中自然表達的MYH9)的耗竭(敲除)也會降低SARS-CoV和MERS-CoV假病毒的感染。
A549、Calu-3是兩種人類肺泡腺癌細胞系。
3、MYH9的過度表達(通過轉染增加其表達)增強了SARS-CoV-2假病毒對A549和H1299細胞的感染。
H1299也是一種人類肺腺癌(非小細胞肺癌)細胞系,A549、H1299都是源自2型肺泡細胞的人類肺腺癌細胞系。另說H1299細胞摘取自淋巴結。
4、MYH9主要在細胞膜上與SARS-CoV-2
Spike共定位,通過其C端(碳端、羧基端、COOH端)結構域(C-terminal
domain)與Spike的S2亞基以及S1亞基的N端(氮端、氨基端、NH2端)結構域NTD (N-terminal
domain)相互作用(與受體發生作用的區域不只是S蛋白的RBD)。
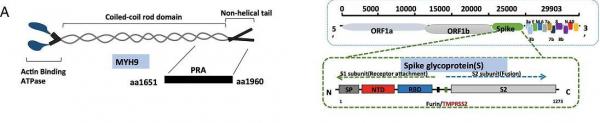
MYH9(左圖)、SARS-CoV-2 Spike(右圖)構成示意圖
5、細胞中PRA(MYH9的C端結構域)的過表達,對多種冠狀病毒進入細胞有着廣譜的促進作用,PRA的過表達,不同程度地增強了兩種α譜系冠狀病毒(HCoV-229E和HCoV-NL63)和三種β譜系冠狀病毒(SARS-CoV,MERS-CoV,HCoV-HKU1)的S蛋白假病毒對A549細胞的感染。
6、肌球蛋白抑製劑ML-7可有效抑制SARS-CoV-2假病毒對PRA-A549細胞的感染。PRA-A549細胞是轉染過表達PRA的A549細胞。
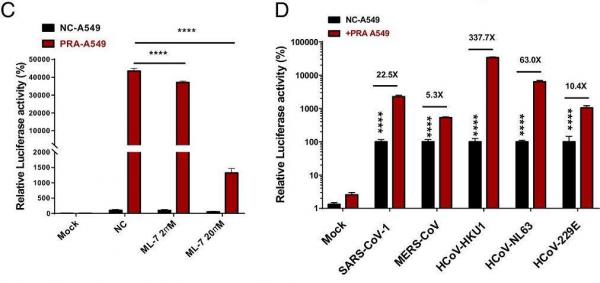
圖C:PRA表達增強了SARS-CoV-2假病毒對A549細胞的感染;ML-7抑制了SARS-CoV-2假病毒對PRA-A549細胞的感染;
圖D:PRA表達不同程度地增強了五種冠狀病毒假病毒對A549細胞的感染。
C、D兩圖的縱坐標是實驗中測得的細胞中熒光素酶的相對活性(Relative Luciferase activity),實驗前熒光素酶基因被嵌入到病毒S蛋白中,其數值指示被感染的細胞的相對數量。
7、TMPRSS2(跨膜蛋白酶絲氨酸2)抑製劑camostat mesylate(甲磺酸卡莫司他)和CatB/L(組織蛋白酶B和L)抑製劑E-64d不影響SARS-CoV-2假病毒對PRA-A549細胞的感染;但這兩種抑製劑強烈抑制SARS-CoV-2假病毒、SARS-CoV假病毒對Caco-2細胞的感染,並減少了SARS-CoV-2假病毒對野生型A549細胞的感染。即,當細胞不表達PRA或MYH9時,這兩種抑製劑可抑制SARS-CoV-2的感染;但當細胞表達PRA或MYH9時,它們不能抑制SARS-CoV-2的感染。這意味着MYH9對SARS-CoV-2感染的促進獨立於TMPRSS2和CatB/L。
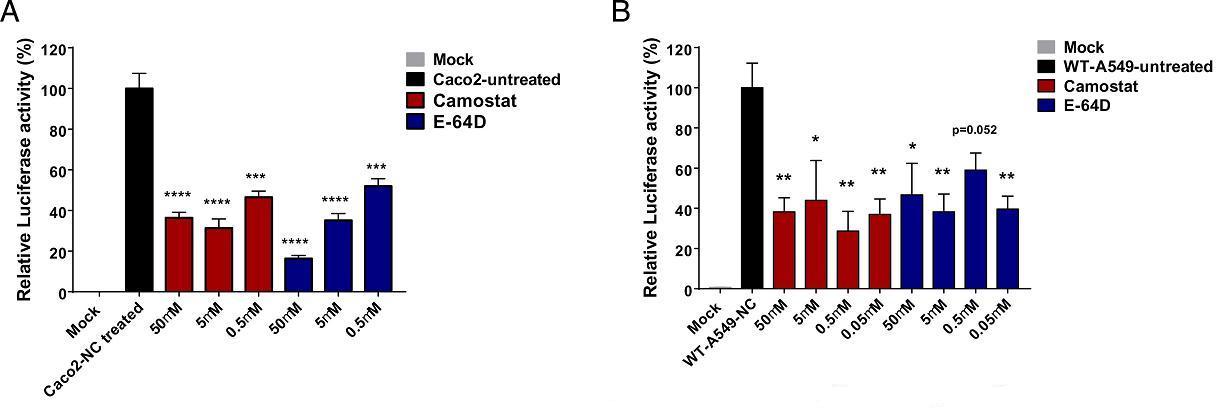
圖A:camostat、E-64d抑制SARS-CoV-2假病毒對Caco-2細胞的感染;
圖B:camostat、E-64d抑制SARS-CoV-2假病毒對A549細胞的感染。
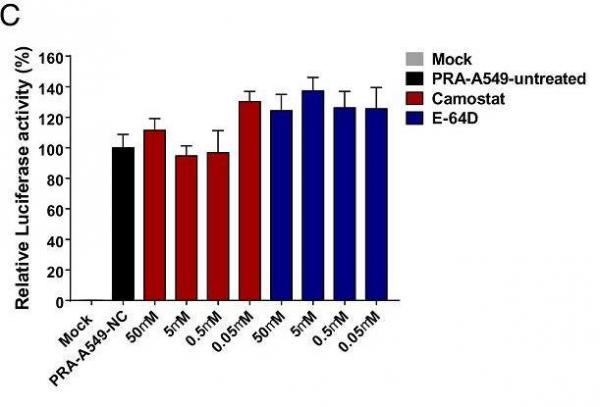
圖C:camostat、E-64d不影響SARS-CoV-2假病毒對PRA-A549 細胞的感染
8、內體抑製劑Chloq(氯喹)、NH4Cl(氯化銨)、Baf-A1(巴弗洛黴素-A1)顯著抑制SARS-CoV-2假病毒對PRA-A549細胞的感染,它們的抑製作用在較低濃度時已非常強烈,三者在100nM 濃度時就可近乎完全消除感染。
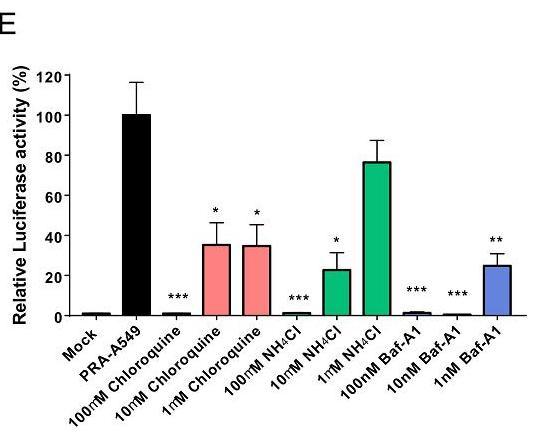
圖E:Chloq、NH4Cl、Baf-A1、強烈抑制了SARS-CoV-2假病毒對PRA-A549 細胞的感染
1nM(納摩爾每升)為10的−9次方mol/dm3(摩爾每升),100nM=0.1μM。
9、以上幾組實驗表明,MYH9對SARS-CoV-2感染的促進作用與內吞過程有關,但繞過了CatB/L在內吞中的作用(CatB/L在內體、溶酶體或其它轉運體中水解激活S蛋白,促成膜融合、釋放RNA),同時不依賴TMPRSS2對S蛋白的激活作用。
10、如果耗盡(敲除)PRA-A549細胞中的ACE2,則SARS-CoV-2假病毒的感染幾乎被消除,ACE2的過表達則增強了SARS-CoV-2假病毒對A549細胞的感染。
這表明MYH9可能無法充當SARS-CoV-2的獨立受體,MYH9對SARS-CoV-2感染的促進依賴於ACE2的存在(至少需要較低表達的ACE2)。
另一方面,MYH9的耗竭(敲除)也幾乎消除了SARS-CoV-2假病毒對A549細胞的感染。
如下圖所示,
a) SARS-CoV-2假病毒幾乎無法感染各種敲除(KO,Knocking Out)了MYH9或ACE2基因的A549細胞;
b) SARS-CoV-2假病毒能感染WT-A549細胞(Wild-Type A549細胞,野生型A549細胞,未作轉染或轉基因處理的天然A549細胞,該細胞自身表達ACE2和MYH9);
c) SARS-CoV-2假病毒對轉染的過表達ACE2的A549-ACE2細胞有更強的感染力。

SARS-CoV-2假病毒不能有效感染敲除了MYH9或ACE2的A549細胞
11、敲除MYH9基因也減弱了SARS-CoV-2真病毒對ACE2-A549細胞的感染。如下圖所示:
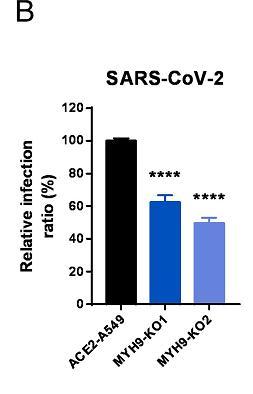
MYH9-KO1、MYH9-KO2是兩組敲除了MYH9蛋白基因的ACE2-A549細胞,不清楚二者的區別。
12、敲除MYH9基因也減弱了SARS-CoV-2真病毒對ACE2-H1299細胞的感染。如下圖所示:
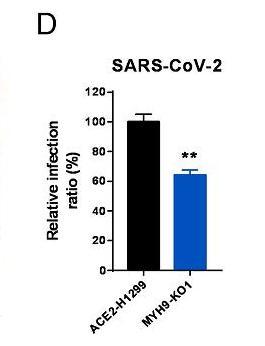
圖中的MYH9-KO1是敲除(KnockOut)了MYH9蛋白基因的ACE2-H1299細胞。
13、敲除MYH9基因極大抑制了SARS-CoV-2真病毒對Calu3細胞的感染。如下圖所示:
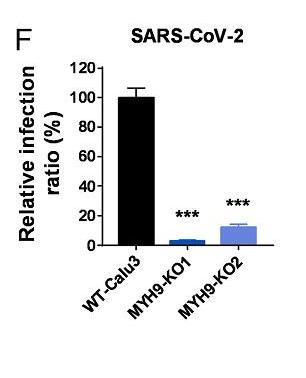
Calu3/Calu-3也是一種人肺腺癌細胞系。
14、論文總結說,MYH9在SARS-CoV-2感染過程中作為ACE2的共受體而發揮重要作用,它以ACE2依賴性方式通過內吞作用介導SARS-CoV-2進入宿主細胞,MYH9-PRA對SARS-CoV-2感染的促進與TMPRSS2和CatB/L無關。
該論文有中文報道:
徐建青_張曉燕團隊《PNAS》報道MYH9是SARS-CoV-2感染的共受體——增強ACE2依賴性內吞作用以促進感染
https://ibs.fudan.edu.cn/76/26/c24338a423462/page.htm
(未完待續)























