接续:谁设计、制造了新冠病毒(二 下)
谁设计、制造了新冠病毒?
新冠病毒为什么偏偏出现在武汉?是武汉病毒研究所泄漏了新冠病毒,还是有人在蓄意制造武汉病毒研究所泄漏新冠病毒的假象?
新冠病毒来自实验室,新冠病毒不可能来自动物,这其实早已铁证如山;新冠疫情发生的来龙去脉,其实同样不难疏理清楚。溯源工作之所以停滞不前,新冠病毒的来源真相、新冠疫情的发源真相之所以至今悬而未决,不是因为缺乏证据、线索,而是因为有极为强大的势力一直在装聋作哑、压制言论,隐匿证据、捂盖线索、回避基本事实,一再炮制、散布谎言,制造假象,转移视线、混水摸鱼。如果新冠病毒源自中国,不放过任何打击中国机会的美国及其盟友,在溯源问题上,为什么只能不断炮制谎言、捕风捉影、含沙射影?为什么始终拿不出一件货真价实的证据?新冠病毒到底出自哪个国家的病毒学家、实验室之手?哪个国家在新冠疫情发生前两年(2017年12月19日)全面重启了危险病毒体功能增益研究,重新以联邦资金资助本国功能增益研究,疫情发生后对此一直讳莫如深、百般回避?哪个国家操纵着国际组织,领导、操纵着科学界,操纵着全球话语权?到底是哪个国家最不甘让病毒、疫情的源起真相大白于天下,决心在欺骗世人、愚弄世人的道路上继续裸奔下去?
新冠病毒来自实验室,新冠病毒出自长期从事冠状病毒功能增益改造研究的病毒学家、实验室之手。
新冠病毒是广为借鉴、人为精心设计的跨科属病毒集大成者,新冠病毒有多项结构、特性借鉴自各种冠状病毒和非冠状病毒,这些结构、特性根本不可能自然演化(自然变异或自然重组)产生。我举六个例子。
借鉴示例一:新冠病毒刺突蛋白S1/S2处(S1亚基、S2亚基交界处)的“RRAR”furin酶切位点借鉴自小鼠肝炎病毒MHV-JHM株系、MHV-3株系,及猫传染性腹膜炎病毒(FIPV)某些毒株S1/S2处的“RRARR”酶切位点。这些毒性、致死能力极强的冠状病毒与新冠病毒差异巨大,根本不存在自然进化关系;
借鉴示例二:新冠病毒“RRAR”酶切位点附近的O-Linked聚糖结构借鉴自HIV-1、埃博拉、丙型肝炎等病毒,该结构有屏蔽、逃避宿主免疫系统打击的作用。HIV-1是逆转录科病毒,埃博拉是丝状病毒科病毒,丙型肝炎病毒是黄病毒科病毒,它们都不是冠状病毒;O-Linked聚糖结构未在其它冠状病毒中发现、报告过。
借鉴示例三:新冠病毒刺突蛋白的RBD关键氨基酸借鉴自蝙蝠冠状病毒Rs3367(WIV1),这一借鉴设计赋予了新冠刺突蛋白极强的人类ACE2结合能力,赋予了新冠病毒极强的人体细胞感染能力、极强的跨物种感染能力,它也是新冠病毒泛器官、泛组织感染、侵犯能力的两大来源之一。新冠与Rs3367(WIV1)总体差异很大,进化距离极为遥远。
借鉴示例四:新冠病毒刺突蛋白S1亚基中的gp120蛋白和Gag蛋白借鉴自艾滋病病毒HIV-1,gp120蛋白可赋予病毒感染、杀死CD4+T淋巴细胞,损害人体免疫系统的能力,这是新冠重症患者淋巴细胞计数显著减少的原因之一(新冠病毒还因具有“RRAR”furin酶切位点而可通过高效的膜融合感染、杀死T淋巴细胞)。这两种蛋白也未在其它冠状病毒中发现、报告过。
借鉴示例五:新冠病毒N蛋白(Nucleocapsid,核衣壳蛋白)中的nsp3A编码借鉴自HEV71病毒(71型人肠道病毒,婴幼儿手足口病的主要病原体),nsp3A编码有抑制、干扰宿主免疫反应的作用。HEV71也不是冠状病毒,它是微小RNA病毒科病毒。没有在其它冠状病毒中发现、报告过nsp3A编码,而且,冠状病毒的N蛋白高度保守,极少发生自然变异。
借鉴示例六:新冠病毒具有“逆转录自身RNA为cDNA(RNA的互补DNA),并将其整合到人体被感染细胞DNA中”的特性,它使新冠患者在康复后体内仍存在新冠病毒的RNA片断,使许多康复患者的PCR检测结果仍为阳性。这一“逆转录RNA-人体DNA整合”特性借鉴自逆转录科病毒,没有在其它冠状病毒中发现、报告过这一特性。
上述六项借鉴情况都有可靠的论文依据或其它依据(如基因序列依据),但难以得到广泛宣传(我的溯源文章证据详实充分可靠,写作慎重仔细,内容清晰准确,错误极少,有一说一、实事求是,挖真相、讲真话,不撒谎、不欺骗,我个人认为这些文章非常优秀、非常难得、独一无二,但它们一直被冷处理,既得不到广泛宣传,也得不到广泛讨论),也难有人把他们串联起来深入思考。六项借鉴示例的依据我在以前的文章中都提供过;部分借鉴示例我还详细展开介绍过,比如,
“RRAR”furin酶切位点相关的借鉴可参阅:
新冠furin酶切位点探源,病毒学界的集体捂瞒
逆转录-人体DNA整合相关的借鉴可参阅:
新冠病毒与拉尔夫·巴里克的不解之缘(一)
gp120蛋白、Gag蛋白相关的借鉴可参阅:
谁设计、制造了新冠病毒(二 上)
一文中的有关内容(可在文中搜“gp120”)。
为什么没有科学权威站出来对世人点明上述情况?要么是我撒谎造谣、无中生有,要么是科学权威们在回避、隐匿这些事实。哪个国家有能力操纵科学界、科学权威、科学刊物?哪个国家最需要装聋作哑,隐匿、捂盖上述指示新冠病毒来源的重大证据、线索?
本文及本文续篇将再次展开讨论RBD关键氨基酸相关的借鉴情况(我去年已写过三篇相关文章)。
新冠与rs3367(WIV1)RBD关键氨基酸的关联
冠状病毒刺突蛋白RBD中有五个重要位点,这五个位点上的氨基酸残基决定刺突蛋白的ACE2结合能力,进而决定冠状病毒通过结合ACE2受体进入、感染细胞的能力,它们被称为(ACE2相关的)RBD关键氨基酸残基,简称RBD关键氨基酸或RBD关键残基。
RBD即受体结合域(Receptor Binding Domain),它是冠状病毒刺突蛋白(spike protein,简称S蛋白)S1亚基的一部分。
蝙蝠冠状病毒被认为是新冠病毒的近亲,但大多数蝙蝠冠状病毒都不以ACE2为感染蝙蝠或其它动物的受体,或者说,大多数蝙蝠冠状病毒都不能结合ACE2,都不能通过结合ACE2来感染动物细胞,感染人类;只有约7种蝙蝠冠状病毒象新冠和SARS那样,能够通过结合ACE2来感染宿主细胞。
刺突蛋白是新冠病毒与蝙蝠冠状病毒差异最大的蛋白,除RaTG13外的蝙蝠冠状病毒与新冠病毒都有巨大的刺突蛋白差异,下图是有关对照示例,注意图中S蛋白处的“深谷”。
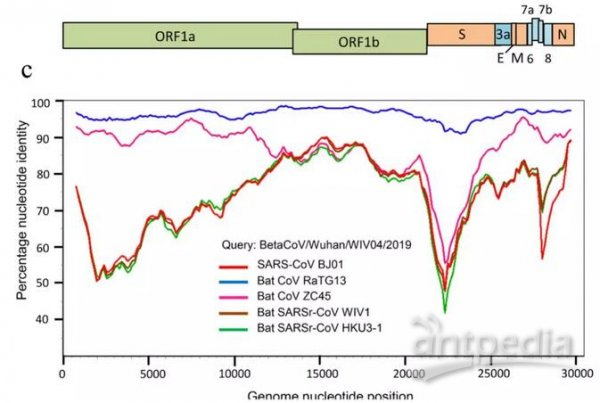
SARS及4种蝙蝠冠状病毒与新冠病毒基因序列一致度的线性变化
新冠病毒与蝙蝠冠状病毒RBD关键氨基酸的差异也很大,绝大多数蝙蝠冠状病毒与新冠病毒至多只有一对RBD关键氨基酸相同,下面是一个对照示例表,表中与新冠(SARS-CoV-2)作RBD关键氨基酸对照的是SARS和三种蝙蝠冠状病毒RaTG13、CoVZC45、rsSHC014。

新冠与几种同支系(β谱系B支系)病毒的RBD关键氨基酸对照表
表中关键氨基酸的表达格式为:氨基酸名称-缩写代号-(氨基酸序号)。以表中第二行第二列的“亮胺酸L(455)”为例,它表示新冠病毒的第一个关键氨基酸是一个亮胺酸,其单字母缩写为L(氨基酸还有三字母缩写),它是新冠病毒刺突蛋白氨基酸序列中的第455个氨基酸(残基)。
新冠病毒在进化树中的“第一近亲”是(真实性可疑的)蝙蝠冠状病毒RaTG13。RaTG13与新冠全基因组序列一致度(相似度)为96.2%,二者刺突蛋白aa(amino acid,氨基酸)序列的一致度约为97.4%。然而,由上表可见,新冠、RaTG13这两个“最亲的亲戚”,它们的五个RBD关键氨基酸仅有第一对相同(天冬酰胺与天冬氨酸是两种不同的氨基酸)。
RBD关键氨基酸与新冠最接近的蝙蝠冠状病毒是一对“孪生”病毒 rs3367和WIV1,它们和新冠有三对RBD关键氨基酸相同,见下表:
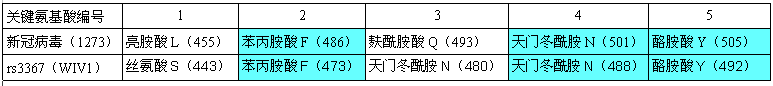
新冠、rs3367(WIV1)RBD关键氨基酸对照表
rs3367、WIV1这对“孪生”蝙蝠冠状病毒发现于云南同一山洞,二者全基因组序列一致度为99.92%,在决定物种感染能力及宿主范围的S蛋白S1亚基部分,二者的aa序列(氨基酸序列)完全相同(从而二者的5个RBD关键氨基酸也完全相同)。
由上表可见,新冠、rs3367(WIV1)的5个RBD关键氨基酸有三对是相同的:它们的第五、第四、第二关键氨基酸同为酪氨酸Y、天冬酰胺(亦称天门冬酰胺)N、苯丙氨酸F。
此外,它们的第三RBD关键氨基酸虽然不同,但却有重大潜在关联。新冠的第三关键氨基酸是麸酰胺酸Q,rs3367(WIV1)的第三关键氨基酸是天冬酰胺N,我们比较一下二者的理化属性。
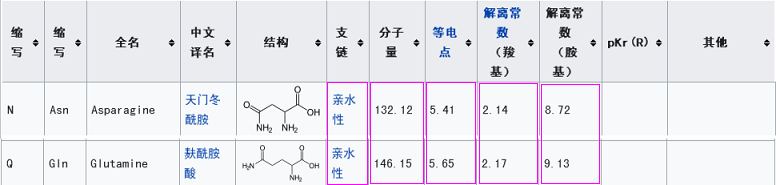
由上表可见,二者的五项理化属性或者相同,或者非常相似、接近(在20种常见氨基酸中,理化属性如此接近的氨基酸恐怕不容易找到第二对),这五项理化属性是分子间相互作用(吸引或排斥,作用力的方向、强弱)的重要决定因素或影响因素,理化属性的高度相似意味着,在刺突蛋白与ACE2相互作用时,这两个氨基酸残基所起的作用很可能是非常相似、非常接近的。
至此可知,新冠的5个关键氨基酸,与rs3367(WIV1)的5个RBD关键氨基酸高度关联,其中三对相同,还有一对理化属性高度相似。
以下论文可以帮助我们进一步认识新冠与rs3367(WIV1)RBD关键氨基酸的关联关系。
2020年9月8日,苏格兰Dundee大学生命科学学院的David Booth和Conchita Fraguas Bringas在Microbiology上发表了如下论文:
Identification
of a SARS-like bat coronavirus that shares structural features with the
spike glycoprotein receptor-binding domain of SARS-CoV-2
一种与SARS-CoV-2刺突糖蛋白受体结合域具有相同结构特征的SARS样蝙蝠冠状病毒的鉴定
https://www.microbiologyresearch.org/content/journal/acmi/10.1099/acmi.0.000166
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7717483/
论文要点如下:
1、论文指出,SARS-CoV-2与类SARS蝙蝠冠状病毒Rs3367,尽管二者刺突蛋白的序列一致度仅为77.70 %,但它们ACE2结合相关的RBD关键氨基酸残基却高度保守(保守即指变化、差异小),SARS-CoV-2决定ACE2结合强度和宿主范围的重要RBD氨基酸残基Phe486(苯丙氨酸F486)、Thr500(苏氨酸T500)、Asn501(天冬酰胺N501)、Tyr505(酪氨酸Y505),与Rs3367的对应RBD残基相同。
作点解释,论文认同ACE2相关的RBD关键(key)氨基酸残基为5个,这一段内容除指出新冠、Rs3367的第二、第四、第五RBD关键氨基酸相同(参见前面的“新冠、rs3367(WIV1)RBD关键氨基酸对照表”)外,还指出了二者另一对相同的氨基酸残基,(新冠的Thr500和Rs3367的Thr487),又并称其为RBD重要(important)残基。
另外,论文中使用的氨基酸三字母缩写与本文使用的单字母缩写是一致的,例如,三字母缩写Phe和单字母缩写F都代表苯丙氨酸;
2、论文指出,SARS-CoV-2与Rs3367之外的其它已研究的α谱系冠状病毒、β谱系冠状病毒RBD关键氨基酸的一致度都很低(新冠、SARS、Rs3367、WIV1都属于β谱系)。
再补充说明一下,β谱系B支系还有一对“孪生”蝙蝠冠状病毒Rs4874和WIV16(Rs4874、WIV16二者的全基因组序列一致度为99.93%),它们与rs3367、WIV1 也高度相似,WIV1与WIV16的全基因组序列一致度为97.54%。这二对四个病毒的5个RBD关键氨基酸完全相同,它们都发现于云南同一山洞,
据我所知,除上述二对“孪生”病毒外,其它蝙蝠冠状病毒至多只有一对RBD关键氨基酸与新冠病毒相同。
以上四个蝙蝠冠状病毒虽然都是武汉病毒研究所发现的,但它们的基因序列(核酸序列、蛋白aa序列)很早就国际共享了,其中,2013年4月8日,武汉病毒研究所将rs3367的全基因组序列、WIV1的spike蛋白序列上传至了NCBI(National Center for Biotechnology Information,美国国家生物技术信息中心)GenBank生物信息数据库,2013年7月8日,武汉所又将WIV1的全基因组序列上传至GenBank。请注意,美国病毒学家拉尔夫·巴里克(Ralph S. Baric)等人2000年就已发明了基于基因序列合成冠状病毒,收获活性毒株的反向遗传技术,美国可以轻松合成、复活所有基因序列国际共享的蝙蝠冠状病毒,美国资助武汉病毒研究所的最重要目的之一就是利用武汉所搜集特殊蝙蝠冠状病毒。
3、利用分子生物学相关软件构建了Rs3367的RBD模型,发现它与SARS-CoV-2的RBD模型有非常相似的三维结构;
4、将Rs3367的RBD模型叠加到SARS-CoV-2的RBD与ACE2相互作用的复合体上,获得了Rs3367的RBD与ACE2相互作用的复合体模型,研究发现,尽管两个复合体模型有所不同,但它们的空间构象也非常相似,而且,SARS-CoV-2对应的复合体中的关键接触(RBD关键氨基酸残基与ACE2氨基酸残基的接触和相互作用),在Rs3367对应的复合体中得到了维持(即SARS-CoV-2维持了Rs3367与ACE2的关键氨基酸接触)。
由3、4可知,SARS-CoV-2、Rs3367两病毒的RBD空间结构非常相似,它们与ACE2作用时的空间构象也非常相似。由此可以认为,SARS-CoV-2、Rs3367的RBD关键氨基酸是高度等价的。
新冠的RBD关键氨基酸是人为设计的
rs3367(WIV1)与新冠全基因组序列一致度约为82.13%,刺突蛋白aa(amino acid,氨基酸)序列一致度约为77%,rs3367(WIV1)与新冠的进化距离遥不可及;
相比之下,RaTG13与新冠全基因组序列的一致度为96.2%,刺突蛋白aa序列一致度约为97.4%。
新冠、rs3367(WIV1)与人类ACE2的结合能力都极强,而RaTG13却不能结合ACE2(结合亲和力非常弱);
新冠与RaTG13仅有一对RBD关键氨基酸相同,与rs3367(WIV1)却有三对RBD关键氨基酸相同,还有一对理化属性高度相似。
新冠的RBD关键氨基酸、人类ACE2结合能力与“第一近亲”RaTG13相去甚远,却与八杆子打不着、进化距离非常遥远的rs3367(WIV1)“酷肖”或密切关联,这是自然演化的偶然巧合,还是人为借鉴、精心设计的痕迹?
新冠病毒东鳞西爪,集多种冠状病毒、非冠状病毒结构、特性于一身?这可能是自然演化的结果吗?
新冠的五个RBD关键氨基酸不是随机突变或偶然重组,无目的进化产生的,它们是基于明确的设计目标,参照、借鉴rs3367(WIV1),通过关键氨基酸复用、替换,人为设计、确定的。
冠状病毒RBD的计算机建模,RBD与ACE2相互作用的计算机模拟是十多年前就已使用的非常成熟的技术,对一个经验丰富的病毒学家来说,使用蛋白质(或分子)设计、模拟、预测工具(如Rosetta Design、MacPyMol等等),参照、基于rs3367(WIV1)的RBD关键氨基酸,通过氨基酸重用、替代,设计出高度等效的新冠病毒RBD关键氨基酸并非难事。忽略摸索过程,试错、反复及琐碎细节,大致可通过以下步骤完成新冠RBD关键氨基酸的设计:
1、构建WIV1的RBD关键氨基酸结构模型,以该模型为新冠RBD关键氨基酸的初始模型;
2、复用WIV1的3个关键氨基酸:第五关键氨基酸--酪氨酸Y,第四关键氨基酸--天门冬酰胺N,第二关键氨基酸--苯丙胺酸F;
3、用理化属性非常相似的麸酰胺酸Q替代天冬酰胺N,以之为模型中新的第三关键氨基酸;
4、在20种常见氨基酸中挑选第一关键氨基酸—丝氨酸S的替代者,入选氨基酸与已确定的四个氨基酸构成的新的关键氨基酸模型应与初始模型高度同构;
5、进行ACE2结合模拟,新模型应尽可能维持初始模型与ACE2的相互作用构象。
6、使用反向遗传平台合成拥有所设计RBD关键氨基酸的病毒,通过实际的细胞感染实验验证新RBD关键氨基酸的有效性。
为什么要借鉴rs3367来设计新冠病毒的RBD关键氨基酸
rs3367(WIV1)是功能增益研究的极佳借鉴、参照对象和原材料。
rs3367(WIV1)是新冠病毒出现前跨物种感染能力最强的冠状病毒(另一对孪生病毒WIV16、Rs4874的跨物种感染能力应与WIV1、rs3367相同),它(们)的刺突蛋白能结合众多脊椎动物的ACE2,综合有限的研究成果可知,rs3367(WIV1)可感染的物种至少包括以下10种(类):
人类、非洲绿猴、恒河猴、果子狸、貉、雪貂、水鼬(即水貂)、猫、蝙蝠(包括菊头蝠、果蝠等翼手目动物)、老鼠。
参照、借鉴rs3367(WIV1)的RBD关键氨基酸来设计高度等效的新冠病毒RBD关键氨基酸,首先就是为了制造出一种有强大跨物种感染能力的病毒。
来看看新冠病毒的跨物种感染能力。
新冠病毒的跨物种感染、传播能力极为强大、惊人!已确认的,或已报告的可被新冠病毒感染的动物包括:
人类、灵长类动物(如大猩猩、非洲绿猴、恒河猴、食蟹猕猴、狒狒、黑长尾猴和狨猴)、穿山甲、狗、猪、兔子、某些鼠类(如仓鼠、田鼠)、鼬类或貂类(如雪貂、水貂、水獭、黄鼠狼等等)、家猫、老虎、狮子、雪豹、麝香猫、北美鹿(如白尾鹿)、貉、树鼩、果蝠等等。


新冠病毒的宿主名单看上去比WIV1(rs3367)长得多,这是否说明新冠的跨物种感染能力比rs3367 (WIV1)强得多呢?未必如此。这首先是研究的不对等造成的,对rs3367、WIV1的研究远远少于新冠,对它们感染能力的发现自然也大大少于新冠;此外,rs3367、WIV1虽然细胞进入、感染能力广泛,但它们毒性太弱,很少使被感染的动物发病或产生明显症状(它们还会从被感染器官、组织中自行消失,下篇文章将有论文说明这一点),不专门、细致地研究、实验,很难发觉、发现它们对某种动物的感染能力。因此,rs3367、WIV1可感染的动物绝不会只限于前述10种,它们的跨物种感染能力可能与新冠在伯仲之间。
除了跨物种感染能力非常强大外,rs3367 (WIV1)刺突蛋白与hACE2(human ACE2)的结合能力也非常强大,论文依据如下。
2016年3月14日,冠状病毒合成之父Ralph
S. Baric领导的团队在PNAS(美国国家科学院院刊)发表了如下论文:SARS-like WIV1-CoV poised for
human emergence(类SARS冠状病毒WIV1-CoV对人类有潜在威胁)
https://www.pnas.org/content/113/11/3048
我的文章多次提及这篇论文,论文以小鼠体内实验证明:
WIV1病毒刺突蛋白与hACE2的结合亲和力远强于它与mACE2(mice ACE2)的结合亲和力;
WIV1-CoV(WIV1的实验室克隆)、WIV1-MA15(WIV1刺突蛋白与SARS小鼠适应性变异体骨架的嵌合病毒)这两种病毒只能使普通小鼠产生轻微临床症状,但对表达hACE2的转基因小鼠(mACE2转基因为hACE2的小鼠),它们的致病能力大大加强。它们能使转基因小鼠体重减轻超过10%;它们在转基因小鼠肺中的复制滴度,比在普通小鼠肺中的复制滴度高100倍;它们在转基因小鼠大脑中的复制比在肺中更强劲,使部分转基因小鼠患上了致命的脑炎。
由转基因小鼠实验推测,WIV1的刺突蛋白应该具有人类大脑感染能力;进一步推测,新冠病毒的大脑感染、侵犯能力,很可能与其RBD关键氨基酸设计有关(S1/S2处“RRAR” furin酶切位点赋予新冠病毒的高效膜融合感染能力,应该是新冠具有大脑感染、侵犯能力的另一个重要原因)。
rs3367(WIV1)虽然有很强的人类ACE2结合能力和人体细胞进入能力,但它们的病毒骨架毒性很弱。它们只能使(非转基因的)实验室小白鼠产生轻度的疾病症状;它们没有人体致病能力,不会使人体产生临床疾病症状,而且它们会自行从人体内消失(它们可能没有机会到达人类大脑,或毒性不足以造成人类大脑损伤)。虽然本身没有人类致病能力,但如果将它们的刺突蛋白、RBD或RBD关键氨基酸嫁接、嵌合、或应用到毒性强的病毒(如SARS)骨架上,就可以制造出新的危险、可怕的人类致病性病毒。
新冠病毒的hACE2结合能力也极为强大。
2021年6月24日,澳大利亚弗林德斯大学、拉筹伯大学的四位科学家在Nature
Science上发表了如下论文:In silico comparison of SARS-CoV-2 spike protein-ACE2
binding affinities across species and implications for viral
origin(新冠刺突蛋白与ACE2结合亲和力的跨物种模拟比较及其对病毒起源的指示)
https://www.nature.com/articles/s41598-021-92388-5
研究者通过分子动力学定量模拟研究,计算出了新冠S蛋白(刺突蛋白)与各物种ACE2相互作用的结合能(binding
energies for the interactions),各物种ACE2与新冠S蛋白的结合能从高到低依次为:人类 > 穿山甲
> 狗 > 猴子 > 仓鼠 > 雪貂 > 猫 > 老虎 > 蝙蝠 > 麝猫 > 马
> 牛 > 蛇 > 老鼠。
定量模拟计算结果表明:在14个对照研究物种中,与新冠病毒刺突蛋白结合能力最强的物种ACE2,就是hACE2!
新冠、rs3367 (WIV1)的跨物种感染能力都非常强大,它们的刺突蛋白都极为适宜结合hACE2,这是自然演化的“巧合”,还是人为借鉴、人为设计的必然结果呢?
新冠、rs3367 (WIV1)还有一项“巧合”:它们都具有泛器官、泛组织感染能力(WIV1病毒泛器官、泛组织感染能力的论文依据将在下篇文章给出)。
为什么新冠、rs3367 (WIV1)能感染宿主的众多器官、组织?因为它们都有强大的物种ACE2结合能力,而细胞表面的跨膜蛋白ACE2(Angiotensin Converting Enzyme2,血管紧张素转换酶2 )广泛存在于脊椎动物的呼吸、消化、血液、泌尿、生殖、神经(如眼部的相关组织,大脑中负责嗅觉的区域等等)等系统的器官、组织内。
新冠的泛器官、泛组织感染、侵犯能力要远强于rs3367(WIV1),这不仅因为其毒性、抗免疫能力远强于后者,还因为新冠具有同谱系(β谱系)所有蝙蝠冠状病毒都不具有的furin酶切位点,而furin蛋白酶广泛存在于人体各器官、组织之中,其分布的广度、丰度超过了新冠使用的主要受体ACE2,furin酶切位点及其赋予新冠的膜融合感染能力极大地增强、加剧了新冠病毒的泛器官、泛组织感染、侵害能力。
接下来的问题是,谁借鉴rs3367(WIV1)的RBD 关键氨基酸,通过重用、替换,设计出了新冠病毒的RBD关键氨基酸?
相关文章:
连系新冠病毒与Ralph S. Baric的双纽带(上)
连系新冠病毒与Ralph S. Baric的双纽带(中)
连系新冠病毒与Ralph S. Baric的双纽带(下)
(未完待续)