和筆者一同溯源吧,和筆者一起破案吧。我們共同揭開、展示、宣傳那些被捂蓋、被封鎖的重大溯源證據、線索、疑點,共同查明SARS-CoV-2的真正來源,鎖定其設計、製造者;我們共同破解SARS-CoV-2遠涉重洋進入中國、抵達武漢、出現在人群中的曲折過程,還原疫情發生的隱秘真相,鎖定疫情的製造者;我們共同戳破諸如SARS-CoV-2來自動物、來自自然界,以及疫情源自武漢所事故泄漏之類的彌天大謊;我們共同偵破、揭穿其它來自實驗室的病毒,揪出、斬斷隱藏多年、不只一次作案、至今逍遙法外的邪惡黑手。
感謝平台,讓筆者有機會發聲,有機會發表研究所得、研究見解,讓筆者的文章有容身之所。在一些地方,筆者的溯源文章不能發表,不能存活,不能得見天日。
肯請平台,對這些研究了大量科學論文,披露了大量SARS-CoV-2研究成果,挖掘、披露了大量溯源證據、線索、疑點的溯源文章,對這些貢獻了獨創性的、可能意義深遠的溯源發現的溯源文章,對這些論據確鑿、紮實、豐富,邏輯嚴謹、周密,內容真實、可靠,信息全面、透明、無遮掩的優秀溯源文章,對這些凝聚了筆者大量心血、全網獨一無二的原創溯源文章,肯請平台,請不要壓制、消音或冷漠對待它們,請不要讓它們困處一隅,鮮有人知,請不要讓它們悄然埋沒、湮滅,如同未存在過;肯請平台,請給這些文章多一些關注、溫暖和支持,請給這些文章多一些展示、傳播的機會,請給這些文章多提供一些討論、交流的機會,請給這些文章多提供一些接受批駁、批判的機會。這些溯源文章不只是筆者的作品,它們也是世人的財富,它們也是平台的財富。
偏聽則暗,兼聽則明。聰明的人目光長遠、視野開闊,眼觀六路、耳聽八方,不會以沙埋頭、閉目塞聽。除了溯源證據、線索、疑點,對筆者總結、披露的,挖掘自眾多科學論文的其它信息,如SARS-CoV-2的隱性或長期的危險致病能力(包括但不限於高度致癌性),或許您也應該了解它們,而不是一無所知。
廣大網友,請不要迴避筆者的作品,它們配得上您關注的目光,它們值得您駐足停留,它們值得您仔細審視、深入思考。如果您並不仇視筆者的文章,如果您和筆者一樣,主張以是非定立場,而非以陣營定立場、定是非,如果您不是象某些人那樣,在用不留言、不討論,不質疑、不建議,不批評、不駁斥的方式冷凍筆者的文章,壓低它們的熱度,那麼,我誠摯地肯請您,請展現您對真相的渴望,請釋放您追求真相的熱忱,請留下您的寶貴意見!不要讓筆者心灰意冷,不要讓筆者失去堅持的勇氣和力量。
人類需要陽光,人類需要真相;我們需要知道SARS-CoV-2的來源真相,我們需要知道這次疫情的發生真相。
接續:
新冠中的跨物種、跨生物界、超生物基因 5
SARS-CoV-2與一些非“近親”冠狀病毒,與多種非冠狀病毒(包括但不限於艾滋病病毒、狂犬病病毒、流感病毒、乙肝病毒、丙肝病毒),
與多種致病細菌(包括但不限於炭疽桿菌 、霍亂弧菌、鼠疫耶爾森氏菌、幽門螺桿菌、破傷風梭菌、結核分枝桿菌、麻風分枝桿菌),
與某些寄生蟲(如惡性瘧原蟲),
與某些人體結構元件(如ENaC-α/上皮鈉離子通道的α亞基),
與某些人類蛋白(包括但不限於p53腫瘤蛋白、Hermansky-Pudlak syndrome protein/ 赫曼斯基-普德拉克綜合症蛋白、RhoGEF蛋白、ICAM-1/細胞間粘附分子-1、VEGF-A/血管內皮生長因子-A、MSH3/錯配修復蛋白同源物3、多種惡性腫瘤中的致病蛋白所共有的melanoma domain /黑色素瘤結構域),
與某些人類蛋白酶(如腺苷脫氨酶/ADA、血紅素加氧酶/heme oxygenase),
與某些人類激素(如鐵調素/Hepcidin),
與一些低等動物特有的結構元件、蛋白(如某些軟體動物、節肢動物特有的血藍蛋白/Hemocyanin,某些環節動物、節肢動物特有的巨血紅蛋白/Erythrocruorin),
與某些植物特有的成分(如存在於植物質體/色素體中的多酚氧化酶),
與某些細菌毒素(如葡萄球菌腸毒素B/SEB、肉毒桿菌神經毒素/Botulinum neurotoxin),
與某些動物毒素(如眼鏡蛇屬和銀環蛇屬蛇神經毒素),
與某些醫療藥劑(如腫瘤化療的極佳藥物載體Pep42),
與某些生物醫學專利(如莫德納公司February 4, 2016 Filed的一項名為“用於生產腫瘤相關蛋白質和多肽的修飾多核苷酸”的專利US 9587003),都存在離奇、驚人的結構、能力巧合!
SARS-CoV-2是廣為參照、借鑑,廣為模仿、植入,集眾多跨物種基因、跨生物界基因、超生物基因於一身的基因工程/轉基因集大成者,致病能力、致病因素集大成者;SARS-CoV-2出自長期從事病原體G-o-F(gain-of-function)研究,功能增益改造經驗極其豐富,技術積澱極其深厚的資深病毒學家、實驗室、研究團隊之手。
SARS-CoV-2具有高度致癌性,其致癌途徑異常豐富、多樣。筆者之前的文章已經介紹過多種SARS-CoV-2致癌機制、途徑,未來還將介紹SARS-CoV-2的其它致癌機制、途徑。SARS-CoV-2的核心設計者很可能身兼資深病毒學家和資深癌症/腫瘤專家雙重身份(當然,也有可能其某個團隊成員是資深癌症/腫瘤專家),身兼資深病毒學家和資深癌症/腫瘤專家雙重身份的科學家很容易鎖定。筆者之前的文章多次聚焦這個人,或許您已經知道他是誰了。
I SARS-CoV-2對冠狀病毒基因的繼承、借鑑、模仿、優化、集成(續五)
在SARS-CoV-2的眾多巧合對象中,有一種冠狀病毒。這種冠狀病毒不是SARS-CoV-2“近親”,它與SARS-CoV-2進化距離非常遙遠,基因組差異非常巨大,它的發現地,也與SARS-CoV-2的發現地遠隔重洋、相距萬里。然而,這兩種天差地遠的冠狀病毒,偏偏在感染、致病的關鍵環節、關鍵位點,存在多項極低概率的,極其反常、極為離奇的結構、能力巧合,如同它們是心有靈犀的跨時空靈魂知己,又如同它們是無比默契的同門師兄弟。這種冠狀病毒就是2012年9月現身於沙特的MERS-CoV(Middle East Respiratory Syndrome Coronavirus,中東呼吸綜合症冠狀病毒)。
本文是SARS-CoV-2與MERS-CoV結構、能力巧合的第二部分。兩篇文章報告、指出的眾多反常、離奇、詭異巧合鐵證如山地揭示、證明:不只SARS-CoV-2來自實驗室,MERS-CoV也是人造的!這兩種人類嚴重致病冠狀病毒設計思路高度一致、高度契合、一脈相承,它們極有可能出自同一團隊或同一團伙之手。
上一篇文章報告、指出了SARS-CoV-2、MERS-CoV、人類腺苷脫氨酶(ADA)之間的一組DPP4(dipeptidyl peptidase IV,二肽基肽酶4 )結合、利用巧合,這組巧合包括以下四項具體巧合:
1、SARS-CoV-2 Spike、MERS-CoV Spike都具有DPP4結合能力;
2、SARS-CoV-2、MERS-CoV都能以DPP4為受體感染人體細胞;
3、SARS-CoV-2 Spike、MERS-CoV Spike、人類腺苷脫氨酶(ADA)三者在結合DPP4時錨掛的4個DPP4關鍵氨基酸位點相同;
4、MERS-CoV在結合DPP4時共錨掛了14個DPP4氨基酸位點,巧合的是,DPP4在人體內的結合伴侶--人類腺苷脫氨酶(ADA)在結合DPP4時也錨掛了共14個DPP4氨基酸位點;令人震驚的是,而MERS-CoV、人類腺苷脫氨酶(ADA)所錨掛的14個DPP4氨基酸位點居然完全相同、一個不差!
### 2024-03-18 補充 ###
人類DPP4共有766個氨基酸個氨基酸位點。MERS-CoV、人類腺苷脫氨酶(ADA)錨掛的14個共同的DPP4氨基酸位點,按照論文依據指出它們時的順序依次是:1-R336、2-Q286、3-T288、4-R317、5-Q344、6-K267、7-L294、8-Y322、9-A291、10-L294 、11-I295、12-V341、13-I346、14-N229。
###### end ######!
以DPP4為感染受體,或具有DPP4結合能力的病毒(包括冠狀病毒和非冠狀病毒)非常罕見(蛋白結合能力是以該蛋白為感染受體的先決條件)。截止2020年,具有DPP4結合能力的病毒可能只有4種:艾滋病病毒HIV-1、扁顱蝠冠狀病毒HKU4、MERS-CoV、SARS-CoV-2 。SARS-CoV-2的“近親”病毒,同支系的眾多冠狀病毒(包括同支系的眾多蝙蝠冠狀病毒,眾多其它動物冠狀病毒),無一具有DPP4結合能力,更無一以DPP4為感染受體。
### 2024-03-23補充 ###
HIV-1能以gp120蛋白(HIV-1的包膜蛋白—gp160蛋白的受體結合亞基)結合DPP4,但筆者未見有論文將DPP4稱為HIV-1的感染受體;HKU4適宜結合蝙蝠DPP4,對人類DPP4結合能力微弱,它只能感染蝙蝠細胞,不能感染人體細胞。因此,在大千世界不計其數的病毒(包括冠狀病毒和非冠狀病毒)中,能以DPP4為受體感染人體細胞的病毒可能僅有兩種,就是SARS-CoV-2和MERS-CoV。
###### end ######
SARS-CoV-2是β譜系B支系(即乙型冠狀病毒屬Sarbe亞屬)冠狀病毒,MERS-CoV 是β譜系C支系(即乙型冠狀病毒屬Merbe亞屬)冠狀病毒,雖然隸屬同一譜系(屬),但兩者基因組差異非常巨大,進化距離非常遙遠。SARS-CoV-2、MERS-CoV全基因組序列(核苷酸序列)僅28%可比對(Blast比對結果中的Query Cover值為28%),可比對部分相似度為67.06%;兩者Spike蛋白aa序列(amino acid sequence,氨基酸序列)76%可比對,可比對部分相似度僅為34.91%;兩者Spike蛋白決定受體結合能力的RBD(receptor binding domain,受體結合域)部分的aa序列相似度同樣非常之低,僅為19.1%。不可思議的是,全基因組、Spike蛋白、RBD相似度如此之低的兩種病毒,不僅都能結合DPP4,不僅都能以DPP4為感染受體,而且,這兩種病毒結合DPP4時錨掛的4個DPP4關鍵氨基酸位點,還是相同的。更匪夷所思的是,人類DPP4共有766個氨基酸個氨基酸位點,而MERS-CoV結合DPP4時錨掛的14個DPP4氨基酸位點,與人類腺苷脫氨酶(ADA)錨掛的14個DPP4氨基酸位點,竟然完全相同、一個不差!這實在是太過於巧合了!
上述巧合是隨機性、無目的自然變異、自然演化的奇蹟嗎?筆者不這麼認為。合乎情理的解釋是:
SARS-CoV-2、MERS-CoV都參照、借鑑、模仿了人類腺苷脫氨酶(ADA)的DPP4結合機制。MERS-CoV完全復用了ADA的14個DPP4結合/錨掛位點,SARS-CoV-2可能作了一些變通、調整,只復用(或至少復用)了ADA14個DPP4結合/錨掛位點中的4個最關鍵位點。SARS-CoV-2、MERS-CoV都是來自實驗室的人為設計、製造的病毒。
DPP4結合、利用巧合不是SARS-CoV-2 、MERS-CoV巧合的全部。這兩種病毒還存在其它多項巧合,您將看到,這些巧合的離奇程度、匪夷所思程度,並不遜色於DPP4結合、利用巧合。
MERS-CoV (下)
S1/S2位點處氨基酸序列模式巧合
S1/S2表示冠狀病毒Spike蛋白S1亞基、S2亞基的交界處。S1/S2位點是冠狀病毒感染、致病能力的關鍵位點。
SARS-CoV-2、MERS-CoV這兩種病毒全基因組、Spike蛋白、RBD的差異都非常巨大,然而,在S1/S2這一感染、致病的關鍵位點處,二者的氨基酸序列卻反常地高度相似。如以下兩圖所示。

4種病毒S1/S2(箭頭指示處)位點附近的氨基酸序列
配圖論文來源:
The sequence at Spike S1_S2 site enables cleavage by furin and phospho-regulation in SARS-CoV2 but not in SARS-CoV1 or MERS-CoV
S1/S2位點處的序列使SARS-CoV-2 能夠被furin切割和磷酸化調節,SARS-CoV-1或MERS-CoV則不然。
https://www.nature.com/articles/s41598-020-74101-0
註:SARS-CoV-1沒有furin切割位點(即furin酶切位點,FCS),MERS-CoV在S1/S2處存在furin切割位點(furin切割序列為RSVR),但其切割效率遠低於SARS-CoV-2 。

SARS-CoV-2、MERS-CoV S1/S2位點附近的氨基酸序列
配圖論文來源:
Structures and dynamics of the novel S1_S2 protease cleavage site loop of the SARS-CoV-2 spike glycoprotein
SARS-CoV-2刺突糖蛋白新型S1/S2蛋白酶切割位點環的結構和動力學
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7534663/
如以上兩圖所示,SARS-CoV-2、MERS-CoV S1/S2位點左側氨基酸序列的高度相似性體現在以下3個方面:
1)、SARS-CoV-2 S1/S2位點左側存在“近親”皆無的獨特四氨基酸插入PRRA,非常巧合的是,MERS-CoV S1/S2位點左側恰恰存在與PRRA對應的四氨基酸PRSV。
2)、PRRA、PRSV皆以PR(脯氨酸-精氨酸)開頭,皆以非極性氨基酸結尾(A-丙氨酸、V-纈氨酸都是非極性氨基酸)。
3)、PRRA、PRSV之後同為精氨酸R,前者促成了SARS-CoV-2的furin切割序列RRAR,後者則促成了MERS-CoV的furin切割序列RSVR。SARS-CoV-2、MERS-CoV在S1/S2處都有furin酶切位點/furin切割位點(furin cleavage site,FCS)。
對比鮮明而極為反常的是,SARS-CoV-2的所有“近親”病毒,SARS-CoV-2同支系的所有冠狀病毒,無一例外,在S1/S2處全都空缺與PRRA 對應的氨基酸,無一例外,全都沒有furin切割序列/furin酶切位點。如以下兩圖所示。
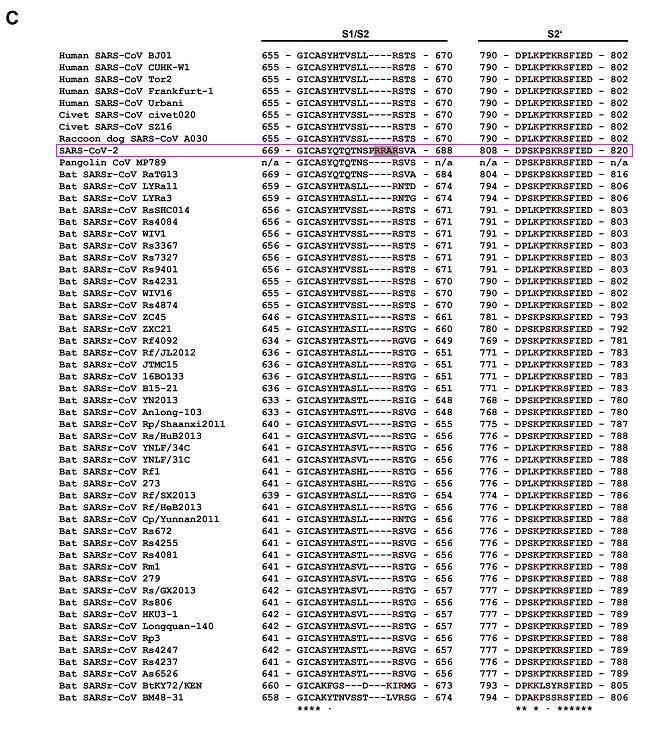
β譜系B支系部分人類、果子狸、貉、穿山甲、蝙蝠冠狀病毒局部氨基酸序列比對
配圖論文來源:
A Multibasic Cleavage Site in the Spike Protein of SARS-CoV-2 Is Essential for Infection of Human Lung Cells
SARS-CoV-2刺突蛋白的多鹼基切割位點對感染人肺細胞至關重要
https://www.cell.com/molecular-cell/fulltext/S1097-2765(20)30264-1
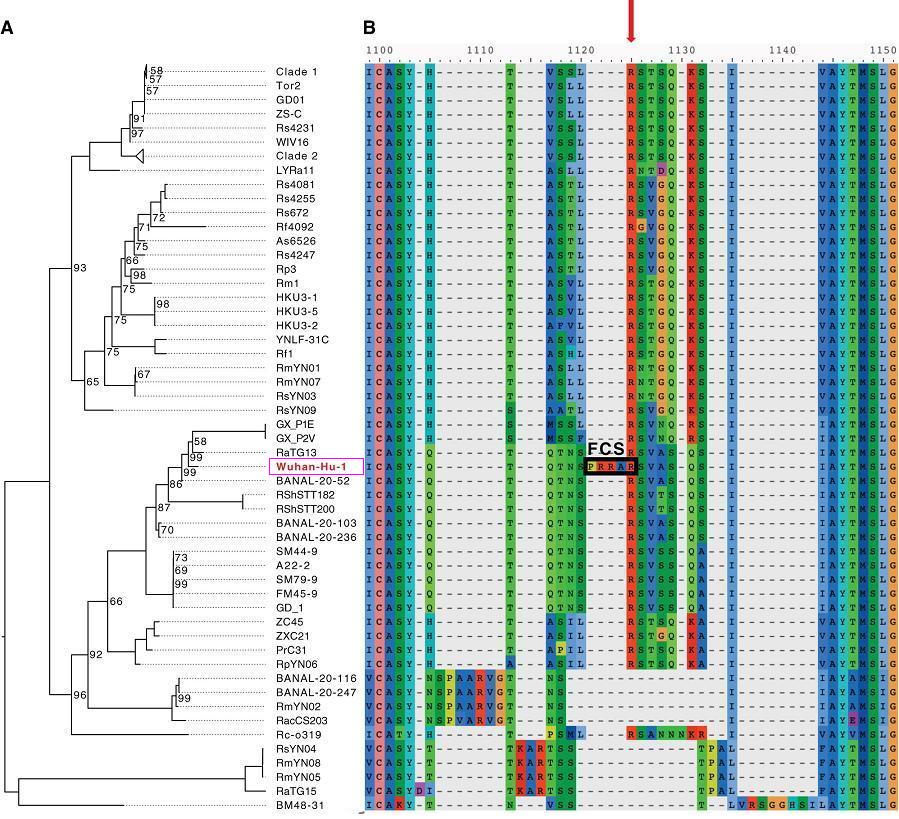
SARS-CoV-2(Wuhan-Hu-1毒株)與進化樹中冠狀病毒S1/S2位點附近的aa序列比對
配圖論文來源:
Emergence of the Spike Furin Cleavage Site in SARS-CoV-2
SARS-CoV-2中刺突弗林切割位點的出現
https://academic.oup.com/mbe/advance-article/doi/10.1093/molbev/msab327/6426085
由以上兩圖可見,SARS-CoV-2 S1/S2位點左側獨特的PRRA插入在圖中極為醒目、突兀,兩圖中的其它病毒全都空缺與PRRA對應的氨基酸。
事實上,
1)、SARS-CoV-2 是β譜系B支系(乙型冠狀病毒屬Sarbe亞屬)唯一具有furin 酶切位點的冠狀病毒;
2)、所有Spike與SARS-CoV-2 spike同源性(相似度)大於40%的冠狀病毒都不具有furin 切割位點(當然更不具有S1/S2處的furin切割位點或furin切割序列)。
第1點是眾所周知的事實,第2點的論文依據是:
Furin: A Potential Therapeutic Target for COVID-19
弗林:COVID-19的潛在治療靶點
https://www.cell.com/iscience/fulltext/S2589-0042(20)30834-8
論文原文:
We
performed furin digestion site prediction on the sequence of each type
of coronavirus Spike through online software. It was found that all
Spike with a SARS-CoV-2 Spike sequence homology greater than 40% did not
possess a furin cleavage site (Figure 1, Table 1), including Bat-CoV
RaTG13 and SARS-CoV (with sequence identity as 97.4% and 78.6%,
respectively). The furin cleavage site “RRAR” of SARS-CoV-2 is unique in
its family, rendering by its unique insert of “PRRA.” The furin
cleavage site of SARS-CoV-2 is unlikely to have evolved from MERS,
HCoV-HKU1, and so on. From the currently available sequences in
databases, it is difficult for us to find the source.
We aligned
1,000 Spike sequences and found that all Spikes with sequence homology
greater than 40% of SARS-CoV-2 Spike did not have a furin cleavage site,
but its possible evolutionary source cannot be found currently, and
more novel viruses are needed to be discovered.
本小節指出的巧合遠不是SARS-CoV-2、MERS-CoV最反常、最不可思議的巧合。我們接着往下看。
P5位點脯氨酸巧合
SARS-CoV-2、MERS-CoV furin切割序列P5位點皆為脯氨酸(P)。無比神奇、極度不可思之處在於,在大千世界難計其數的大量病毒(包括冠狀病毒、非冠狀病毒)中,具有furin切割位點,且furin切割序列P5位點為脯氨酸(P)的病毒僅有兩種,這兩種病毒恰巧就是SARS-CoV-2、MERS-CoV。
基本furin切割序列(也叫最小furin切割序列)“RXXR”(如RRAR、RSVR)的四個氨基酸位點從右至左依次被稱為P1位點、P2位點、P3位點、P4位點,P4位點左側緊鄰的氨基酸位點稱為P5位點,P5位點就是“RXXR”左側的第一個氨基酸位點。下圖示範了這種標記方式:
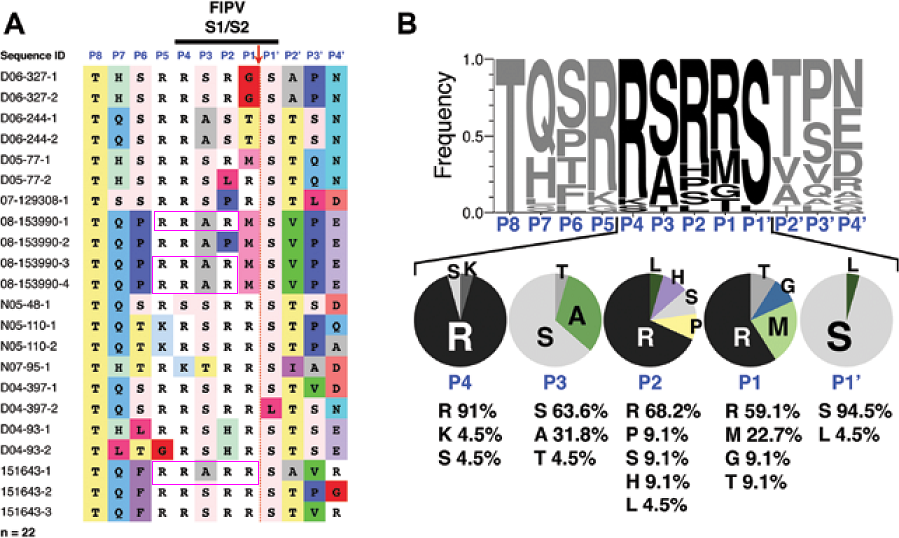
某些FIPV病毒株S1/S2處的RRARR、RRAR切割序列
說明一下,PRRA、PRSV中的P表示脯氨酸(proline,P),P1、P2、P3、P4、P5中的P則表示位點(position),同為字母P,含義並不相同。

SARS-CoV-2 、MERS-CoV furin切割序列P5位點皆為脯氨酸(P)
如上圖所示,SARS-CoV-2基本furin切割序列RRAR,MERS-CoV基本furin切割序列RSVR左側的第一個氨基酸位點,也就是P5位點的氨基酸皆為脯氨酸(P)。
furin切割序列P5位點為脯氨酸(P)的病毒僅有兩種,這兩種病毒就是SARS-CoV-2、MERS-CoV,除了SARS-CoV-2、MERS-CoV,再沒有其它P5位點為脯氨酸(P)的病毒了!
這一驚人事實的論文依據是:
Structures and dynamics of the novel S1_S2 protease cleavage site loop of the SARS-CoV-2 spike glycoprotein
SARS-CoV-2刺突糖蛋白新型S1_S2蛋白酶切割位點環的結構和動力學
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7534663/
論文由瑞士蘇黎世DS3Lab的Thomas Lemmin等人發表。
論文原文:
From a structural point of view, the SARS-CoV-2 S protein proline residue (P681; Figs. 1d and 3c) in the insertion is eye-catching, because of the special and unique structural properties of this proteinogenic amino (imino) acid. MERS-CoV S protein is one of the other rare CoV spike proteins, that also contains a proline residue at the corresponding position in the S1/S2 protease cleavage site (Fig. 1e). When searching the database FurinDB (Tian et al., 2011) (http://www.nuolan.net/substrates.html), which includes experimentally verified furin cleavage sites, it appears that a proline residue at position P5, i.e., the 5th residue prior to the furin cleavage site, is rare and appears in only 5 out of 132 sequences (three mammalian and two viral sequences).
如論文所述,P5位點為脯氨酸的furin切割序列很罕見,在FurinDB 數據庫中的132個序列中,僅有5個序列P5位點為脯氨酸。這5個P5位點為脯氨酸的furin切割序列3個是哺乳動物序列,2個是病毒序列,2個病毒序列一個來自SARS-CoV-2,另一個來自MERS-CoV。
furin切割序列P5位點為脯氨酸的病毒僅有兩種,這兩種病毒恰恰就是2012年9月出現的MERS-CoV和2019年11、12月出現的SARS-CoV-2。這實在於太過於巧合、太過於詭異、太過於幽默了!這又是無目的、隨機性自然變異、自然演化的神跡嗎?
為什麼SARS-CoV-2、MERS-CoV furin切割序列的P5位點都要使用脯氨酸(P)呢?這個設計頗有深意,P5位點的脯氨酸對於感染、致病能力(可能)有以下多重作用:
1)、與P6位點的絲氨酸(S)或蘇氨酸(T)構成脯氨酸定向激酶作用基序和磷酸化位點,通過干預、改變人體正常的磷酸化,擾亂、破壞正常生理過程,導致種種疾病。病毒還可通過磷酸化有關蛋白質使細胞處於有利於病毒複製、病毒生存的周期階段。詳情見下一巧合;
2)、脯氨酸有特殊的構象剛性,可將furin切割序列對應的多肽與Spike蛋白的其他結構元件分開,使前者更好地暴露於furin(等)蛋白酶,提升Spike蛋白切割、激活的效率,進而提升感染效率;
3)、脯氨酸產生的轉角預計(可能未得到確認)會導致PRRA插入兩側的2個絲氨酸(S673、S686)、1個蘇氨基酸(T678 )形成O-連接聚糖(O-linked glycans),O-Linked聚糖能與人體細胞表面的某些蛋白質相互作用,形成一個可逃避免疫打擊的糖鏈屏障,是SARS-CoV-2眾多可能的免疫逃避/免疫屏蔽途徑之一。
2)、3)兩點都是剛剛提到的Thomas Lemmin等人的論文所指出的。
4)、P5位點的脯氨酸還可能有助於調節Spike蛋白及病毒包膜的融合前構象,降低膜融合的能量門檻,使病毒包膜與細胞膜更容易發生膜融合,使病毒的感染(即細胞進入)更便捷、高效。這一推測基於英法兩國科學家1 December 1998發表的以下論文:
A
Proline-Rich Motif Downstream of the Receptor Binding Domain Modulates
Conformation and Fusogenicity of Murine Retroviral Envelopes
受體結合域下游富含脯氨酸的基序調節鼠逆轉錄病毒包膜的構象和融合性
https://journals.asm.org/doi/10.1128/jvi.72.12.9955-9965.1998
P6、P5位點脯氨酸定向激酶作用基序巧合
SARS-CoV-2、MERS-CoV furin切割序列P6、P5位點恰好分別使用了脯氨酸定向激酶的兩個作用基序(SP、TP)。furin切割序列P6、P5位點使用脯氨酸定向激酶作用基序的病毒依然僅有兩種,還是SARS-CoV-2、MERS-CoV!
脯氨酸定向激酶(proline-directed kinases)有兩個二元(雙氨基酸)作用基序:SP、TP。SARS-CoV-2的furin切割序列RRAR P6位點的絲氨酸S、P5位點的脯氨酸P組成的雙氨基酸短序列SP(絲氨酸-脯氨酸)恰好是兩個二元作用基序之一;而MERS-CoV的對應位點恰好使用了脯氨酸定向激酶的另一個二元作用基序TP(蘇氨酸-脯氨酸,P11、P10位點存在另一個TP基序)。如下圖所示。

MERS-CoV、SARS-CoV-2 P6、P5位點的脯氨酸定向激酶作用基序TP、SP
論文依據:
The sequence at Spike S1_S2 site enables cleavage by furin and phospho-regulation in SARS-CoV2 but not in SARS-CoV1 or MERS-CoV
https://www.nature.com/articles/s41598-020-74101-0
論文原文:
Further, we describe a surprising finding that the two serines at the edges of the insert SPRRAR↓SV can be efficiently phosphorylated by proline-directed and basophilic protein kinases. Both phosphorylations switch off furin’s ability to cleave the site.
Intriguingly, besides the RxxR motif, the sequence of the loop SPRRAR↓SV contains two serines that match the consensus of proline-directed kinases (SP), and basophilic protein kinases (RxxS), the two largest subfamilies of mammalian kinases21,22.
Spike S680 matches the consensus of proline-directed kinases (SP) and S686 forms a consensus for basophilic kinases (RxxS), two large subfamilies of mammalian kinases21,22.
The SARS-CoV1 S1/S2 segment does not contain a consensus site for proline-directed kinases, and while the MERS-CoV segment contains two potential proline-directed TP sites,
讀及此處,您是否和筆者一樣震驚、嘆服:遠隔重洋、相距萬里、差異巨大、進化距離遙不可及的SARS-CoV-2、MERS-CoV,是何等的默契!是何等的心心相印、心有靈犀!
由於furin切割序列P5位點為脯氨酸(P)的病毒僅有兩種,因此,P6、P5位點為脯氨酸定向激酶作用基序(SP、TP)的病毒同樣僅有兩種,依然是MERS-CoV、SARS-CoV-2。
為什麼MERS-CoV、SARS-CoV-2要使用脯氨酸定向激酶作用基序?因為脯氨酸定向激酶作用基序(SP、TP)中的絲氨酸S或蘇氨酸T可被脯氨酸定向激酶磷酸化。病毒可通過磷酸化基序干預、改變人體自身的磷酸化機制,擾亂、破壞正常的生理過程,製造各種疾病;病毒還可通過磷酸化有關蛋白質使細胞處於有利於病毒複製、病毒生存的周期階段。磷酸化(Phosphorylation),指在蛋白質的絲氨酸-S或蘇氨酸-T或酪氨酸-Y(殘基)上加入一個磷酸基團。
哺乳動物激酶家族兩個最大的亞家族(子家族),一是脯氨酸定向激酶(proline-directed kinases),二是嗜鹼性蛋白激酶(basophilic kinases)。
MERS-CoV在S1/S2位點附近只使用了脯氨酸定向激酶的磷酸化作用基序(如前圖所示,兩次使用了相同的TP基序);
SARS-CoV-2在S1/S2位點附近同時使用了兩種激酶的磷酸化作用基序。SARS-CoV-2 S1/S2處的長furin切割序列RRAR'SVAS中的第2至第5氨基酸RARS還符合嗜鹼性激酶發揮作用的RXXS 基序模式,RARS中的絲氨酸S可被嗜鹼性激酶有效磷酸化。
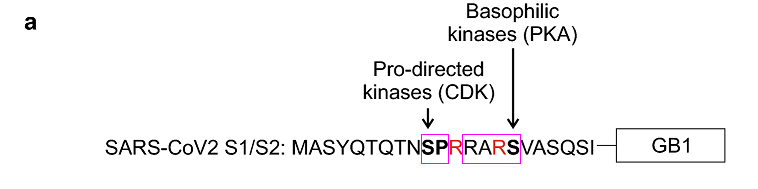 SARS-CoV-2 S1/S2位點附近的的脯氨酸定向激酶作用基序SP及嗜鹼性激酶作用基序RARS
SARS-CoV-2 S1/S2位點附近的的脯氨酸定向激酶作用基序SP及嗜鹼性激酶作用基序RARS
此配圖摘自剛剛提到的論文。
SARS-CoV-2 Spike蛋白上有十幾個磷酸化位點(phosphorylation sites),在其N、M、S(Spike)、nsp3a、nsp9b等蛋白中共有約 70個磷酸化位點。SARS-CoV-2感染會強力干預、改變人體自身正常的磷酸化機制,導致宿主蛋白顯著、嚴重的磷酸化改變,並顯著增加某些生理過程(如碳代謝,carbon metabolism)中的磷酸化,SARS-CoV-2感染會導致人體增加2000 多種磷酸肽,在SARS-CoV-2感染的細胞中觀察到超過15,000個宿主磷酸化位點。SARS-CoV-2感染還會改變(上調或下調)參與磷酸化的多種激酶的活性,並通過磷酸化與信號傳導和細胞周期有關的蛋白質,來干預、劫持宿主信號通路、信號傳導,阻滯/停滯細胞周期,使細胞處於有利於病毒複製、病毒生存的周期階段。
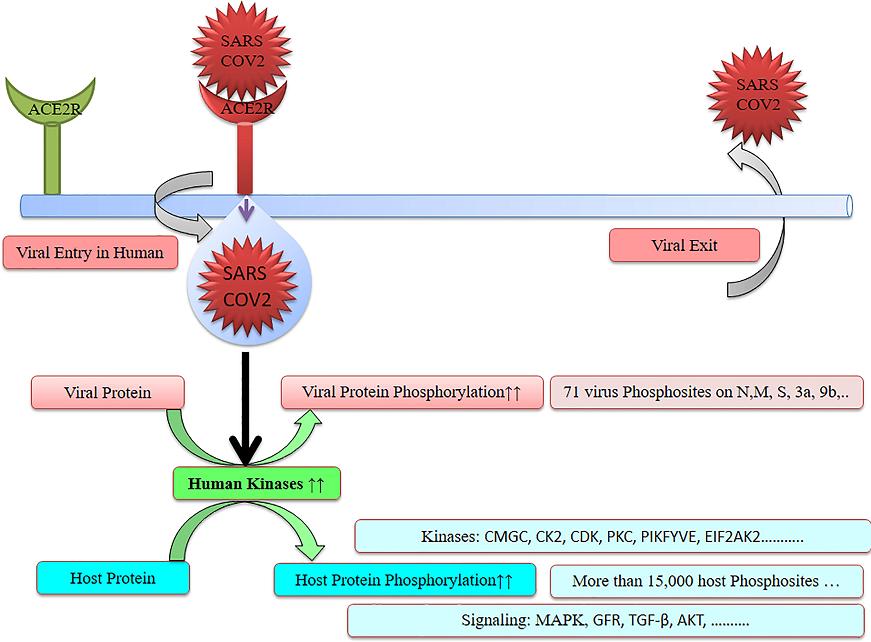
Figure 1 SARS-CoV-2 causes heavy phosphorylation
蛋白質磷酸化異常,包括磷酸化途徑的改變會導致多種嚴重疾病,尤其是癌症。靶向磷酸化途徑的藥物代表了癌症治療的有希望的領域。筆者已多次指出,SARS-CoV-2具有高度致癌性,SARS-CoV-2的致癌途徑異常豐富。其它與磷酸化異常有關的疾病包括糖尿病、心血管疾病、阿爾茨海默症(Alzheimer's disease)、炎症性疾病等等。
參考論文:
SARS-CoV-2 Infection Triggers Phosphorylation: Potential Target for Anti-COVID-19 Therapeutics
SARS-CoV-2感染觸發磷酸化:抗COVID-19治療的潛在靶點
https://www.frontiersin.org/articles/10.3389/fimmu.2022.829474/full
SARS-CoV-2、MERS-CoV,這兩種病毒基因組差異非常巨大,進化距離非常遙遠,但在結合、利用DPP4這一細胞感染的關鍵環節上,它們卻出奇地一致。它們都能結合DPP4,都能以DPP4為受體感染人體細胞(如前文所述,能結合DPP4或以DPP4為感染受體的病毒非常罕見,僅有約4種),它們在結合DPP4時錨掛的4個DPP4關鍵氨基酸位點相同,而MERS-CoV錨掛的所有14個DPP4氨基酸位點更是與人類腺苷脫氨酶(ADA)完全相同、一個不差!極為反常、對比極為鮮明的是,SARS-CoV-2的所有“近親”病毒,SARS-CoV-2同支系的所有冠狀病毒,無一例外,全都不能結合DPP4,全都不能以DPP4為感染受體。另外,以DPP4為感染受體,或具有DPP4結合能力的病毒非常罕見,可能只有4種(截止2020年),能以DPP4為受體感染人體細胞的病毒可能僅有兩種,就是SARS-CoV-2和MERS-CoV;
這兩種病毒基因組差異非常巨大,進化關係非常遙遠,但在S1/S2這一感染、致病的關鍵位點處,它們的氨基酸序列卻高度相似、高度匹配,它們在這一位點處都具有furin酶切位點(FCS)。極為反常、對比極為鮮明的是,SARS-CoV-2的所有“近親”病毒,SARS-CoV-2同支系的所有冠狀病毒,在S1/S2處,全都與SARS-CoV-2差異顯著,它們無一例外,全都存在顯著的4氨基酸空缺,它們無一例外,全都沒有furin酶切位點;
這兩種基因組差異非常巨大,進化距離非常遙遠的病毒,它們furin切割序列P5位點的氨基酸同為脯氨酸(proline,P)。極為反常、極其不可思議的是,在難計其數的冠狀病毒、非冠狀病毒中,具有furin切割位點,且furin切割序列P5位點為脯氨基酸的病毒僅有兩種,它們恰巧、偏偏就是SARS-CoV-2和MERS-CoV;
這兩種基因組差異非常巨大,進化距離非常遙遠的病毒,它們furin切割序列P6、P5位點都使用了脯氨酸定向激酶基序並形成磷酸化位點。脯氨酸定向激酶有兩個二元作用基序(SP、TP),SARS-CoV-2、MERS-CoV恰巧各使用了一種(SARS-CoV-2使用了SP,MERS-CoV使用了TP);furin切割序列P6、P5位點使用脯氨酸定向激酶基序的病毒也只有兩種,它們依然是SARS-CoV-2、MERS-CoV。
如此之多極低概率的巧合,如此之多極為離奇、極為詭異、極度不可思議的巧合,不是隨機性、無目的自然變異、自然演化所能解釋、敷衍的,它們鐵證如山地揭示、證明:SARS-CoV-2、MERS-CoV都是人為設計、製造的實驗室病毒;這兩種病毒的設計思路高度一致、高度契合、一脈相承,它們極有可能出自同一實驗室、同一團隊或同一團伙之手。
(未完待續)













 SARS-CoV-2 S1/S2位點附近的的脯氨酸定向激酶作用基序SP及嗜鹼性激酶作用基序RARS
SARS-CoV-2 S1/S2位點附近的的脯氨酸定向激酶作用基序SP及嗜鹼性激酶作用基序RARS