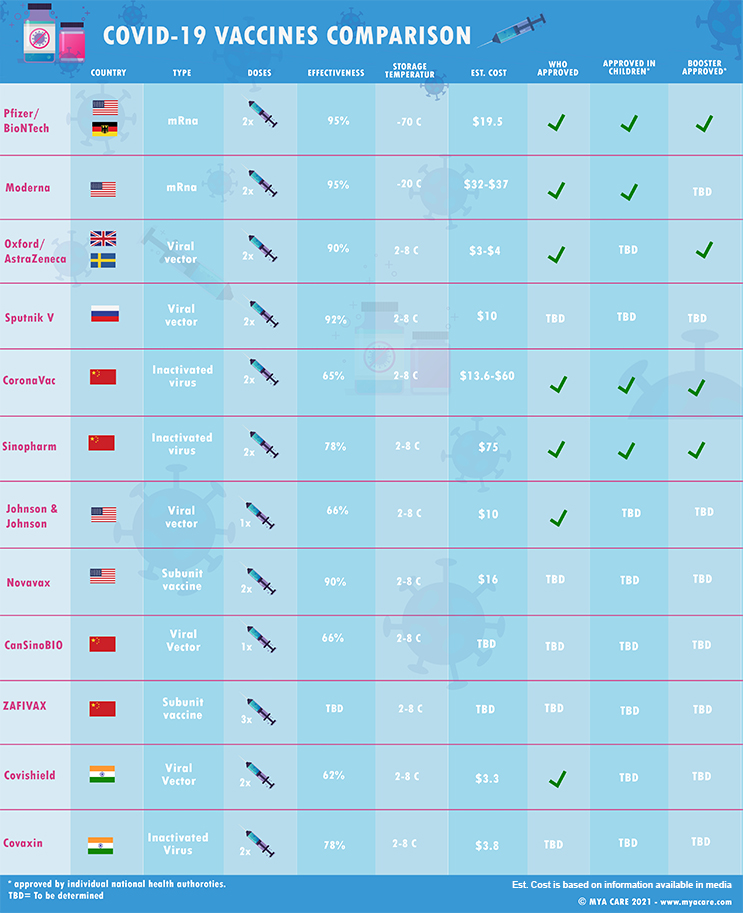
| COVID 19 疫苗的比較 2021 年 10 月 24 |
| 送交者: davidtao123456 2021年11月13日21:37:14 於 [健康生活] 發送悄悄話 |
|
目前正在進行全球大規模疫苗接種,以結束 COVID-19 大流行。 幾種候選疫苗已獲得國際衛生當局的批准,大多數國家正在使用多種疫苗類型來加快這一進程。
最著名的已經獲批或即將獲批的 COVID-19 疫苗是輝瑞/BioNTech、Moderna、牛津/阿斯利康、俄羅斯的人造衛星 V 疫苗、中國的 CoronaVac 和國藥集團疫苗等。 關於這些不同的疫苗有很多新聞,那麼它們如何比較?
1:美國德國: 輝瑞/生物技術疫苗
輝瑞/BioNTech 疫苗是第一種進入最後測試階段的 COVID-19 疫苗。它是目前市場上批准最廣泛的 COVID-19 疫苗,並在全球分銷和管理。輝瑞疫苗是通過美國製藥巨頭輝瑞和德國生物技術公司 BioNTech 之間的精彩合作開發的。
疫苗細節:輝瑞/BioNTech 疫苗是一種 mRNA 疫苗,而不是傳統疫苗。雖然 mRNA 疫苗以前從未在試驗環境之外用於人類,但輝瑞 / BioNTech 疫苗已獲得世界各地衛生當局的批准,例如美國食品和藥物管理局 (FDA) 和世界衛生組織 (WHO) )。您可以查看我們關於 mRNA 疫苗的文章,以了解有關其工作原理的更多信息。
有效性:輝瑞公司報告稱,該疫苗在預防冠狀病毒感染方面的有效率為 95%,並且該疫苗是安全的,不會引起嚴重的副作用。該數據基於一項涉及 43,000 多人的臨床研究。批准後進行的較新研究顯示出類似的有效性。
物流:輝瑞/BioNTech COVID-19 疫苗分 2 劑給藥,每劑估計費用為 19.50 美元,間隔 3 周。然而,疫苗帶來了後勤問題,因為它只能在 -70°C 下儲存,這可能是有問題的,特別是在這種冷藏無法廣泛使用的欠發達國家。儘管如此,正在實施國家和國際配送計劃以滿足這些物流需求。輝瑞承諾到 2021 年底將生產多達 13 億劑。
青少年和兒童的批准:5 月,歐盟醫療機構 (EMA) 和 FDA 已批准輝瑞疫苗用於 12-15 歲的青少年,以進一步減緩 COVID-19 的傳播。青少年 COVID-19 疫苗接種已經在美國開始,並且應該在歐洲以及最快 6 月的第一周開始。
許多父母仍然不願意給他們的孩子注射,然而,所有主要的衛生當局都推薦它作為一種安全和保護性的干預措施。最近對 2,260 名青少年進行的一項研究表明,該疫苗對 12 至 15 歲兒童的有症狀感染 100% 有效。
21 年 6 月 1 日更新: 根據一項新發布的研究,輝瑞疫苗似乎對印度和英國的變種具有保護作用。 2021 年 6 月 30 日更新:
發表在《自然》雜誌上的一項新研究表明,輝瑞/Biontech 疫苗可以提供持久的免疫力。該疫苗不僅會刺激“記憶”免疫細胞,還會導致在您的淋巴結中形成長壽的“生發中心”。這些中心可以生產數月或數年的抗體,並有可能更有效地對抗新的變異。 根據英國公共衛生部最近的研究,輝瑞疫苗似乎對新冠病毒 Delta (1.617.2) 變體非常有效。該疫苗為感染這種新型高傳染性毒株的患者提供 96% 的住院保護。
2021 年 8 月 1 日更新: 最近一項涉及 44,000 人的大型分析表明,輝瑞/BioNTech 疫苗在接種 6 個月後仍保持 86% 以上的有效性。還發現該疫苗對南非冠狀病毒變種非常有效。 輝瑞和 BioNTech 已宣布,他們將進行臨床試驗,以確定是否需要加強注射,因為人們對 delta 變體的擔憂日益加劇。到目前為止,CDC 和 FDA 不推薦第三劑。 一項新研究表明,輝瑞疫苗在完全接種疫苗的人群中對 delta 變體的有效率為 88%。 輝瑞宣布將在 5-11 歲兒童中測試 BioNTech 疫苗,預計結果將於明年 9 月公布。 鑑於新的 delta 變體,輝瑞已宣布計劃尋求第三次“助推器”注射的批准。不過,FDA 和 CDC 仍然不推薦第三針。
2021 年 8 月 22 日更新: 美國食品和藥物管理局已批准輝瑞-BioNTech 疫苗用於免疫功能低下患者的第三針。這包括接受移植或有其他原因導致免疫力極低的患者。 預計輝瑞疫苗最早將於 9 月獲得 FDA 的全面批准。這意味着它不會被指定為“EUA - 緊急使用授權”疫苗,這可能會轉化為更多的公眾信任。 一項新研究得出的結論是,第三次 Pfizer-BioNTech 刺戳可以在已經接受過兩次注射的人中預防高達 86% 的突破性病例。該研究涉及 60 歲及以上的人。
2021 年 8 月 24 日更新: 美國食品和藥物管理局 (FDA) 於 2021 年 8 月 23 日在美國全面批准輝瑞 BioNTech 的 Covid 疫苗。 以前 mRNA 疫苗處於緊急使用授權之下,但最近的授權使人們可以隨時獲得疫苗16歲及以上。
2021 年 9 月 24 日更新: 臨床試驗的早期結果顯示,輝瑞-BioNTech 疫苗在 5 至 11 歲兒童中的有效性和安全性方面取得了可喜的結果。10 微克的小劑量疫苗已產生針對該病毒的強烈抗體反應。
FDA 已允許對 65 歲及以上的個人、18 至 64 歲的 COVID-19 高風險個人以及 18 至 64 歲的經常接觸 SARS 的個人使用單次加強劑量的輝瑞 BioNTech 疫苗-CoV-2 使他們面臨嚴重 COVID-19 的風險。
在阿聯酋,DHA 將開始向中度至重度免疫功能低下的患者接種第三劑輝瑞 BioNTech 疫苗。這適用於 12 歲及以上的個人。
2021 年 10 月 6 日更新: 阿聯酋衛生和預防部 MoHAP 宣布,輝瑞 BioNTech 疫苗的加強劑量僅適用於以下人群,以及在接種 2 劑國藥後已接種輝瑞 BioNTech 疫苗的任何人不符合加強注射的條件:
60歲及以上的長者 50-59 歲有發生併發症風險的慢性病患者 18歲及以上接受長期健康的患者
2021 年 10 月 24 日更新: 輝瑞和 BioNTech 已要求美國 FDA 和加拿大衛生部批准在 5 至 11 歲兒童中接種第一劑 COVID-19 疫苗。該疫苗的劑量是成人和 12 歲以上青少年劑量的三分之一。加拿大衛生部期待更多的科學審查在批准 Pfizer-BioNTech 疫苗的兒童劑量之前。 最近的一項研究表明,第三劑輝瑞 BioNTech 疫苗對 COVID-19 症狀的有效率為 95.6%。兩個實驗室對 10,000 人進行了隨機試驗。兩家公司透露,與未接受加強劑的人相比,加強劑恢復了對病毒的高水平疫苗保護。 美國國立衛生研究院 (NIH) 宣布,輝瑞 BioNTech 疫苗可能是強生 COVID-19 疫苗的最佳加強劑量。這項對 500 人進行的研究發現,與第二劑強生相比,強生疫苗和 mRNA 疫苗提供了更強的免疫反應。 FDA 稱收益大於風險
2:美國Moderna疫苗:
Moderna 是一家美國生物技術公司,在宣布其 mRNA COVID 疫苗後成為 2020 年的頭條新聞。該疫苗使用的技術與輝瑞/BioNTech 使用的技術相同,也得到了世界各地衛生當局的好評。目前,Moderna 在美國的銷售最為活躍,然而,數百萬劑已經到達歐盟和其他國家。
有效性:與輝瑞公司相比,Moderna 的疫苗在預防感染新型冠狀病毒方面也有 95% 的有效性。 30,000 人參加了 Moderna 的 III 期臨床試驗,研究人員得出結論,該疫苗是安全的,並且只會引起罕見的副作用。許多國家還批准了用於孕婦和哺乳期婦女的疫苗。
物流:與大多數其他可用的 COVID-19 疫苗一樣,Moderna 的疫苗分 2 劑間隔接種。費用估計在 32 美元到 37 美元之間。在物流方面,Moderna的mRNA疫苗必須在-20°C儲存,這在第三世界國家也是一個挑戰。
21 年 6 月 1 日更新: Moderna 現在正在尋求獲得 FDA 的批准,用於 12 至 18 歲的兒童。該公司已經發布了一項涉及該年齡組 3,732 名兒童的研究的非常有希望的結果。 5 月 25 日公布的研究結果表明, Moderna 疫苗對 12 歲以上的兒童非常安全,可提供 100% 的 COVID-19 保護。
21 年 6 月 30 日更新: Moderna 已向加拿大衛生部和歐盟醫療機構 (EMA) 提交申請,以獲得青少年(12 至 17 歲)的批准。與 FDA 一樣,該授權仍在等待中。
21 年 8 月 1 日更新: 歐洲醫療機構 (EMA) 建議批准 Moderna 疫苗用於 12-17 歲的兒童。 Moderna 正在擴大其在兒童中的臨床試驗,以包括 11 歲及以下的兒童。
2021 年 8 月 22 日更新: 儘管公司提出要求,但 FDA 仍未批准 Moderna 用於兒童 FDA 目前正在審查心肌炎(心肌炎症)的報告,以評估這是否確實是疫苗的罕見副作用。官員們向人們保證,這種副作用極為罕見,而且通常是可控的。 FDA 已批准在免疫功能低下的患者中注射第三劑 Moderna 疫苗。這包括接受移植或有其他原因導致免疫力極低的患者。 早期報告表明,Moderna 在預防突破性 delta 病例方面比輝瑞更有效。然而,需要注意的是,該數據仍未得到證實,而且在所有情況下,這兩種疫苗首先都非常有效。
2021 年 9 月 24 日更新: Moderna Inc. 正在開發其 COVID-19 加強劑量和實驗性流感疫苗的組合疫苗 CDC 報告稱,Moderna 疫苗在預防住院方面比強生和輝瑞 BioNTech 的疫苗更有效。數據顯示,該疫苗對非免疫功能低下的成年人的有效率為 93%。牛津/阿斯利康疫苗
2021 年 10 月 24 日更新: FDA 的疫苗和相關生物製品諮詢委員會一致同意 Moderna 加強劑量的緊急使用授權。委員會批准為 65 歲及以上的人、18 至 64 歲的 COVID-19 高危人群以及 18 至 64 歲的經常接觸 COVID-19 的人提供 50 微克的加強劑。 FDA 可能允許 Moderna 和強生 COVID-19 疫苗接受者採用混合搭配方法。接受單次強生注射的人可能會在至少 2 個月後接受 Moderna 助推器。提交給 FDA 的數據顯示出有希望的結果,但是,該機構尚未批准該方法。
3:英國-瑞典: 牛津/阿斯利康疫苗
牛津大學與英國-瑞典製藥公司阿斯利康 (AstraZeneca) 之間的合作產生了一種 COVID-19 疫苗,該疫苗也得到了廣泛認可。牛津疫苗是一種傳統疫苗,而不是像 Moderna 和輝瑞 / BioNTech 的 mRNA 疫苗。該疫苗使用一種經過改造完全無害的普通感冒病毒,將 COVID-19“刺突蛋白”引入人體。
有效性:為了測試疫苗的有效性,研究小組分析了 11,000 多名志願者的結果。研究人員得出結論,牛津/阿斯利康疫苗在預防冠狀病毒感染方面的有效率為 90%。研究小組發現,在接種了疫苗但仍被感染的人中,所有病例都是輕度病例,沒有一個是重症病例。這意味着,即使您是未能從疫苗中獲得全部益處的不幸 10% 之一,您仍然可以免受嚴重感染。來自 20,000 多名參與者的安全數據顯示,該疫苗在一般人群中具有良好的耐受性和安全性。
物流:牛津/阿斯利康疫苗也分兩劑,每劑價格在 3 美元到 4 美元之間。最近的研究表明,劑量間隔 12 周更有效。與 mRNA 疫苗相比,牛津/阿斯利康疫苗更容易儲存,只需要在 2-8°C 的標準冷藏。
血栓問題:世衛組織發表了一份令人放心的聲明,並建議所有國家繼續使用阿斯利康進行疫苗接種,並指出好處遠大於風險。歐洲藥品管理局 (EMA) 安全評估委員會於 2021 年 4 月 7 日得出結論,異常血凝塊應被列為阿斯利康疫苗的一種非常罕見的副作用,這表明存在潛在的因果關係,從而使牛津-阿斯利康的 COVID 疫苗重回正軌。
阿斯利康疫苗的年齡限制:意大利建議阿斯利康的 COVID-19 疫苗只能用於 60 歲以上的人。此外,意大利衛生當局宣布,60 歲以下的人接受了阿斯利康的第一針疫苗也可以接收第二個。與此同時,英國已向 30 歲以下的人推薦阿斯利康疫苗的替代品,因為有證據表明它與罕見的血栓有關。許多其他國家/地區現在也遵循阿斯利康的年齡限制。
21 年 6 月 1 日更新: 根據英國公共衛生部的一項新研究,阿斯利康疫苗對印度變種的保護率為 60%,對原始英國變種的保護率為 66%。然而,作者報告說,需要給予 2 次全劑量才能有效。
21 年 6 月 30 日更新: 根據英國公共衛生部最近的研究,阿斯利康疫苗可防止因 Delta 變異感染而住院。研究發現,該疫苗可以保護 92% 的感染者。 一項新研究正在進行中,以測試針對南非 COVID-19 變體的阿斯利康助推器。計劃涉及約 2,250 名志願者。 牛津大學的一個研究小組宣布,兩次劑量之間最多延遲 10 個月可以產生更強大的免疫反應。 此外,他們發現,在第二劑注射 6 個月後進行第三次加強注射可以大大加強對 COVID 的保護。 同一個研究小組宣布,仍然沒有證據表明確實需要第三槍。
21 年 8 月 1 日更新: 阿斯利康將在 300 名 6 至 17 歲的幼兒中測試其疫苗效力。
2021 年 9 月 24 日更新: 儘管阿斯利康 COVID-19 疫苗研發者表示可能沒有必要,但英國疫苗接種和免疫聯合委員會 (JCVI) 已批准阿斯利康助推器。
2021 年 10 月 24 日更新: 一項包括超過 700,000 人的研究表明,與接種 2 劑牛津-阿斯利康疫苗相比,單劑牛津-阿斯利康疫苗後接種 Moderna 或輝瑞疫苗可提高對 COVID-19 的保護。
發表在《柳葉刀地區衛生》上的證據發現,牛津-阿斯利康疫苗: 針對 COVID-19 提供 50% 的保護。 輝瑞劑量後有 67% 的保護。 接種 Moderna 疫苗後,有效率為 79%。
4:印度: Covishield防護罩
到目前為止,已經在印度發現了三種“進口變種”——英國、南非和巴西。印度血清研究所的 COVID-19 疫苗稱為 Covishield,是印度製造商在當地生產的牛津-阿斯利康疫苗的一種版本。這種疫苗對英國和印度的變種有效,但正在等待對巴西毒株的療效數據。
有效性:兩劑 Covishield 方案在 3 期臨床試驗中顯示出 62% 的有效性。
後勤:疫苗需要兩劑才能建立免疫力,間隔 28 天接種。此外,它不需要低於零儲存並且在 2-8°C 下是穩定的。在私營機構中,政府為兩種疫苗(Covishield 和 Covaxin)設定了 250 盧比的最高價格,相當於 3.33 美元。迄今為止,Covishield 占印度給藥劑量的 90%,其餘為 Bharat Biotech 的 Covaxin。
血栓問題:在歐洲和英國監管機構提出阿斯利康疫苗與少數罕見血栓病例之間可能存在聯繫之後,印度專家組正在調查這種疫苗的安全性。然而,印度尚未報告凝血障礙病例。
21 年 6 月 30 日更新: 由於 COVISHIELD 是同一阿斯利康疫苗的另一個品牌,因此預計它對 Delta 變體也有效。此外,專家還建議,間隔 10 個月的劑量或加強第三劑可能會提供更多保護。 印度正在考慮在每次劑量之間採用 12 周間隔政策。事實證明,這可以提供更多保護,並可以更快地為更多人接種疫苗。單獨的第一劑在刺戳之間提供了顯着的保護 (76%)。
2021 年 8 月 22 日更新: 牛津大學的一項試驗已開始在 54 名成人中測試 COVISHIELD 的鼻內噴霧版本。鼻內疫苗已經在動物研究中顯示出一些前景。 早期數據表明,第一劑 COVISHIELD 僅提供 30% 的預防感染和嚴重疾病的保護。這提出了在使用這種疫苗的國家中更快接種疫苗的需求。 印度血清研究所 (SII) 宣布可能需要第三次加強劑量的 COVISHIELD。
2021 年 9 月 24 日更新: 一項研究報告稱,在服用兩劑 COVISHIELD 疫苗後,99% 的 COVID-19 抗體保持完整。研究表明,大多數接種了 COVISHIELD 的人在六個月後不需要加強免疫。 2021 年 10 月 24 日更新:
發表在《新英格蘭醫學雜誌》上的一項研究表明,2 劑 COVISHIELD 疫苗可提供針對 COVID-19 Delta 變體的高水平保護。研究人員分析了 540 萬人的數據,發現 COVISHIELD 在預防 COVID-19 陽性人群死亡方面的有效率為 91%。
5:印度: Covaxin科維新
印度的 Bharat Biotech 公司與國家病毒學研究所和印度醫學研究委員會合作,生產一種名為 Covaxin 的滅活冠狀病毒疫苗。基於有希望的早期試驗結果,印度於 1 月 3 日批准了該疫苗用於緊急使用。
疫苗特性:Covaxin 的作用是教您的免疫系統產生針對 SARS-CoV-2 冠狀病毒的抗體。抗體與病毒表面蛋白結合,例如“尖峰”蛋白。發現 Covaxin 對英國和巴西變種均有效。
有效性:III 期試驗結果顯示,一項涉及 25,800 名參與者的試驗的有效性為 77.8%。結果於2021年6月公布。
後勤: Covaxin 在給藥方案方面類似於 Covishield。此外,它可以儲存在2-8攝氏度。 Bharat biotech 已與世界上多個國家接洽,以提供 COVAXIN®。其中包括蒙古、緬甸、斯里蘭卡、菲律賓、巴林、阿曼、馬爾代夫和毛里求斯。
21 年 6 月 1 日更新: 印度計劃在 2021 年提高 Covaxin 的產量,估計今年 8 月至 12 月期間將生產 5.5 億劑。巴西最近訂購了 2000 萬劑 Covaxin,目前該藥已在該國獲得批准。 21 年 6 月 30 日更新:
經過漫長的等待,Covaxin III 期試驗結果出爐。該疫苗似乎對冠狀病毒的有效率為 77.8%。
21 年 8 月 1 日更新: Bharat Biotech 已向世界衛生組織提交了所有必要文件,以獲得印度疫苗全球緊急使用的批准。
2021 年 8 月 22 日更新: COVAXIN 在 525 名 2 至 18 歲的兒童中進行了測試,並顯示出“令人滿意的結果”。這可能意味着該疫苗將很快被批准用於兒童。 COVAXIN 正在加拿大尋求緊急使用批准
2021 年 9 月 24 日更新: 世衛組織推遲批准 COVAXIN。免疫戰略諮詢專家組 (SAGE) 將於 10 月舉行會議,以確定疫苗的 EUA。 18歲及以下兒童的小兒科伐辛已完成2/3期臨床試驗。 Bharat Biotech 將很快將數據提交給 DCGI。
2021 年 9 月 24 日更新: 世衛組織推遲批准 COVAXIN。免疫戰略諮詢專家組 (SAGE) 將於 10 月舉行會議,以確定疫苗的 EUA。 18歲及以下兒童的小兒科伐辛已完成2/3期臨床試驗。 Bharat Biotech 將很快將數據提交給 DCGI。
6:俄羅斯: Sputnik V人造衛星五號疫苗
俄羅斯 Gamaleya 國家中心於 2020 年 11 月宣布其 COVID-19 疫苗取得了積極成果。
疫苗細節:疫苗是使用傳統方法設計的。它與牛津/阿斯利康疫苗非常相似,其中使用改良的無害腺病毒載體將 COVID-19 刺突蛋白遞送至人體以產生針對它的免疫力。
有效性:Gamaleya 國家中心宣布,根據一項招募了 20,000 名志願者的臨床試驗,該疫苗在預防 COVID-19 方面的有效性為 92%。研究人員報告說,該疫苗是安全的,副作用非常小。結果於去年 2 月發表在著名的醫學雜誌《柳葉刀》上,並得到了全世界的認可。最近對阿聯酋 81,000 人進行的一項研究表明,人造衛星 V 的有效性為 97.8%。
物流:Sputnik V 估計每劑費用約為 10 美元,與其他疫苗一樣需要兩劑,間隔 21 天。與牛津疫苗一樣,人造衛星 V 相當容易儲存,只需要標準冷藏。 目前,俄羅斯和巴西、阿根廷、伊朗和中國等許多其他國家正在對 Sputnik V 進行大規模疫苗接種。 Gamaleya 國家中心還與這些國家合作,允許他們在當地生產疫苗,以加快疫苗接種率。印度監管機構也批准了俄羅斯人造衛星 V COVID-19 疫苗。
人造衛星輕型疫苗:俄羅斯政府於 2021 年 5 月早些時候批准了一種新的單劑量版本的人造衛星 V。研究人員宣布,單劑量 COVID-19 疫苗在預防電暈方面的有效率為 79.4%。
21 年 6 月 1 日更新: 與其他疫苗一樣,Sputnik V 疫苗沒有任何相關報道,到目前為止,它似乎對冠狀病毒具有很好的耐受性和保護作用。然而,WHO 和 EMA 仍未批准,原因不明。儘管如此,許多國家已經批准了這些疫苗,並且已經成功接種了數百萬劑。
印度已宣布 Sputnik V 將在 6 月的第二周后開始推出。這使 Sputnik V 成為繼 COVISHIELD 和 COVAXIN 之後印度第三個獲批的 COVID-19 疫苗。到 8 月,俄羅斯將向印度發送 1.25 億劑人造衛星五號。
俄羅斯政府已與印度簽署協議,從 2021 年 8 月開始在那裡生產人造衛星五號。該協議涉及在印度國內的 6 個中心生產 7.5 億劑,這將大大提高該國和全球的疫苗接種率。
21 年 6 月 30 日更新: 韓國將從夏季或初秋開始在當地生產 Sputnik V 和單劑量 Sputnik Light 疫苗。 俄羅斯正在努力獲得歐盟的批准,但目前尚不清楚何時應該獲得批准。 最近對阿聯酋 81,000 人進行的一項研究表明,人造衛星 V 的有效性為 97.8%。
21 年 8 月 1 日更新: 已宣布 Sputnik V 對新的 delta 冠狀病毒變體的有效率為 90%。
2021 年 8 月 22 日更新: 在巴拉圭進行的一項新研究中,發現單劑俄羅斯疫苗 Sputnik Light 的有效率為 93.5%。該研究涉及 320,000 名參與者。 根據最新的試驗數據,俄羅斯將 Sputnik Light 的使用範圍擴大到 60 歲或 60 歲以上的人。 較新的報告表明 Sputnik V 對 Delta 變體的有效率為 83% 一項新研究表明,將 Sputnik V 與其他 COVID-19 疫苗(即阿斯利康、國藥和 Moderna)結合使用是安全的。
2021 年 9 月 24 日更新: 報告表明,人造衛星 V 對 COVID-19 的有效性為 97.2%。 世衛組織暫停批准俄羅斯的人造衛星 V COVID 疫苗。世衛組織官員說,在檢查了其中一家生產工廠後,疫苗的生產過程沒有達到必要的標準。
2021 年 10 月 6 日更新: 阿聯酋衛生和預防部 MoHAP 宣布,人造衛星疫苗的加強劑量僅適用於以下人群,任何在接種 2 劑國藥後已經接種過人造衛星疫苗的人都沒有資格獲得助推器:
60歲及以上的長者 50-59 歲有發生併發症風險的慢性病患者 18歲及以上接受長期健康的患者
2021 年 10 月 24 日更新: 歐盟已暫停批准人造衛星 V 至 2022 年。製造商尚未提供所需數據並完成疫苗申請檔案。 世衛組織還暫停了 Sputnik V 的緊急使用清單處理,以等待缺失的要求。
7:中國: CoronaVac科羅納瓦克
CoronaVac COVID-19疫苗由中國生物製藥公司Sinovac開發。
疫苗特性:該疫苗也是使用傳統方法生產的,但與 Sputnik V 和 Oxford/AstraZeneca 疫苗有些不同。 CoronaVac 使用注射的滅活病毒顆粒來增強對 COVID-19 的免疫力。
有效性:來自在土耳其、智利、印度尼西亞、菲律賓和巴西進行的 III 期試驗的數據報告了高度可變的結果。儘管如此,疫苗似乎在所有試驗中都能完全預防嚴重疾病。 5 月發布的一項大型分析報告稱,對有症狀的 COVID-19 感染的保護率為 65%,對死亡的保護率為 86%。
物流:CoronaVac 的成本仍不清楚,不同來源稱每劑成本從 13.6 美元到 60 美元不等。需要兩劑疫苗才能建立免疫力,就像前面討論的其他四種疫苗一樣。 CoronaVac 不需要複雜的存儲和傳輸物流,標準製冷就足夠了。
巴西、墨西哥、土耳其和烏克蘭等國家已經批准並訂購了該疫苗。
21 年 6 月 1 日更新: 新冠疫苗(Sinovac)於2021年6月1日獲得世界衛生組織緊急使用批准,成為繼國藥集團之後全球第二個獲批的中國疫苗。 中國政府已經向COVAX提供了第一批疫苗,將在全球範圍內分發。埃及政府已經計劃在當地生產疫苗,開始時接種 200 萬劑。 需要指出的是,儘管世衛組織的批准有所延遲,但中國和其他國家也已經使用了超過 7000 萬劑新冠病毒。 華興認為,該疫苗也可用於 3 歲以下的兒童,並且已獲政府批准用於該年齡組。目前還缺乏關於兒童疫苗接種的完整數據,但一項大型臨床試驗已經在進行中。 根據最新研究結果(去年 5 月發布),Coronavac 似乎對 COVID-19 感染具有 65% 的保護作用,並且可以防止 86% 的病例死亡。
21 年 6 月 30 日更新: 發表在《柳葉刀》上的一項新研究宣布,CoronaVac 對 3 至 17 歲的兒童是安全有效的。該研究涉及該年齡組的 550 名參與者,並報告沒有嚴重的副作用。該疫苗已獲中國政府批准用於該年齡組。 印尼宣布Sinovac在12至17歲兒童中的授權。
21 年 8 月 1 日更新: Sinovac 已經宣布他們的疫苗對 delta 變體有效,但是,仍然沒有具體數據支持這一說法。
21 年 8 月 22 日更新: Sinovac 公布的數據證實,他們的第三劑疫苗在預防三角洲感染方面是安全有效的。 智利現在向那些完全接種 CoronaVac 疫苗的人提供阿斯利康注射劑
2021 年 9 月 24 日更新: 聯合國兒童基金會和 COVAX 向烏克蘭運送了超過 150,000 劑 CoronaVac COVID-19 疫苗。 一項對 Sinovac Biotech 疫苗的研究報告稱,加強劑量逆轉了針對 Delta 變體的抗體活性的下降。 Sinovac Biotech 將在南非啟動 COVID-19 疫苗試驗的 3 期試驗。該試驗旨在研究疫苗對兒童和青少年的療效。
2021 年 10 月 24 日更新: 馬來西亞衛生部有條件批准在 12 至 17 歲的兒童中使用 CoronaVac Covid-19 疫苗。藥物管制局旨在優先考慮患有合併症和過敏症的青少年。
8:中國: Sinopharm vaccine國藥疫苗
中國國有製藥公司國藥集團也公布了其 COVID-19 疫苗的樂觀結果。
疫苗特性:國藥的疫苗與另一種中國疫苗 CoronaVac 非常相似,兩者都基於 COVID-19 病毒的滅活版本。在國藥控股宣布該疫苗可安全有效預防 COVID-19 感染後,該疫苗獲得了阿聯酋和巴林監管機構的批准。
有效性:根據一項涉及約 31,000 名志願者的試驗,該公司宣布其疫苗的有效性為 79%。已有100多個國家訂購了中國的新疫苗。
物流:國藥的疫苗也分兩劑接種,每劑的費用估計約為75美元。國藥疫苗只需標準冷藏即可儲存,是發展中國家的理想選擇。
21 年 6 月 1 日更新: 5月初,世衛組織授予國藥緊急使用授權,使其成為首個獲得批準的非西方疫苗。負責委員會宣布,國藥控股的有效性和安全性結果令人鼓舞,其批准將有助於加快全球範圍內的冠狀病毒疫苗接種。 5月25日,美國醫學會雜誌(JAMA)發表了一項大型研究,證實了中國疫苗的有效性。該研究涉及埃及、阿聯酋、巴林和約旦疫苗接種中心的 40,000 名志願者。研究人員發現,國藥的 COVID-19 疫苗對冠狀病毒的有效率為 72.8% 至 78.1%,這與世界衛生組織的決定是一致的。
21 年 6 月 30 日更新: 根據最新報道,目前尚不清楚國藥控股的疫苗是否對新傳播的Delta變種有效。 在阿聯酋開展的一項新試驗將評估國藥控股在 3 至 17 歲兒童中的疫苗安全性和有效性。該研究將涉及 900 名將接受注射的兒童。 阿聯酋已開始向已服用 2 劑國藥集團的人提供額外的輝瑞加強劑。該劑量在最後一次國藥注射後 6 個月給藥。
21 年 8 月 1 日更新: 在斯里蘭卡進行的一項新研究發現,與自然感染相比,國藥控股的疫苗誘導了類似的針對 delta 變體的免疫反應。 經過廣泛的研究和試驗,阿聯酋衛生與預防部 (MOHAP) 宣布國藥 Covid-19 疫苗現在可以用於 13-17 歲的兒童和青少年。
21 年 8 月 22 日更新: 在阿聯酋之後,中國現在已經批准在 3 歲以下的兒童中使用國藥集團的疫苗。
2021 年 9 月 24 日更新: 泰國 FDA 拒絕了國藥集團向 3 歲及以上兒童提供 COVID-19 疫苗的要求,理由是缺乏疫苗安全性數據。 國藥控股正在等待正式批准開始開發自己的 mRNA 疫苗。
2021 年 10 月 24 日更新: 世衛組織呼籲對免疫功能低下者和 60 歲以上的人接種第三劑國藥 COVID-19 疫苗。數據顯示,增加第三劑可提高疫苗效力並增強免疫反應。
9:美國: JONHSON & JONHSON 強生和強生
強生公司是另一家美國醫療器械和製藥公司,最近其新疫苗進入市場。強生公司的單劑量 COVID-19 疫苗是繼輝瑞和 Moderna 之後第三種在 2 月份獲得 FDA 緊急使用批準的疫苗。強生疫苗的主要優勢之一是它是單劑量給藥。 疫苗特性:它是一種腺病毒疫苗,其作用類似於阿斯利康和人造衛星 V。
有效性:預防 COVID 感染的有效性略低於其他獲得許可的疫苗。強生公司報告說,他們的疫苗在預防中度至重度 COVID 感染方面的有效率為 66%,在預防住院和死亡方面的有效率為 100%。這些數字反映了疫苗對症狀的功效,而不是實際感染。儘管如此,FDA 宣布無症狀患者的傳播風險可以忽略不計,因此對症預防是有益的。
物流:美國、歐盟和許多其他國家現在也正在使用一次性疫苗。德國計劃向所有成年人提供強生,無論他們的年齡或風險群體如何,以加快疫苗接種速度。
血凝塊問題:首先是阿斯利康。現在是強生公司。 2021 年 4 月,美國報告了幾例接受強生疫苗後發生凝血的病例。世衛組織在審查現有數據後宣布,強生公司的 COVID-19 疫苗是安全的,凝血是一種非常罕見的不良事件。世衛組織建議繼續使用強生疫苗,因為好處大大超過了可以忽略的風險。在恢復與強生公司的疫苗接種之前,FDA 也發表了類似的聲明。
21 年 6 月 30 日更新: 根據初步消息,強生疫苗對新的 delta Indian 變種的保護率可能只有 60%。但是,在做出任何假設之前,仍然需要進一步調查。
21 年 8 月 1 日更新: 美國食品和藥物管理局對強生公司的格林巴利綜合徵疫苗添加了另一個警告。在接種疫苗的 1,300 萬美國人中,有 100 人觀察到了這種神經系統自身免疫性疾病。
21 年 8 月 22 日更新: 美國官員表示,可能會向已經接種強生疫苗的人提供加強注射。 在南非進行的一項新研究發現,強生疫苗可有效預防 Delta 電暈變異導致的死亡和住院——95% 的死亡率和 71% 的住院率。
2021 年 9 月 24 日更新: CDC 的一位流行病學家說,強生疫苗對 COVID-19 的有效性隨着時間的推移而增加,即使是對 Delta 變體也是如此。 強生公司官員報告的證據表明,強生加強劑量在接受加強治療 4 周后產生的抗體高出 12 倍。在批准加強注射之前,美國衛生官員需要強生公司提供更多數據。
2021 年 10 月 24 日更新: 美國 FDA 允許強生 COVID-19 疫苗在單次接種後至少 2 個月內進行加強劑量。該疫苗適用於 18 歲及以上的人群。 CDC 建議將包括強生在內的 COVID-19 疫苗與不同的加強劑量混合使用。諮詢小組宣布,接受強生注射的人可以在至少 2 個月後獲得輝瑞或 Moderna 助推器。 CDC 官員表示,與另一種強生劑量相比,一種 mRNA 劑量提供了更強的保護。
10:美國: Novavax諾瓦克斯
Novavax 是一家總部位於美國的公司,專門開發用於治療嚴重傳染病的創新疫苗技術。 Novavax COVID-19 疫苗顯示出巨大的希望,可能是迄今為止開發的最好的疫苗之一。
疫苗細節:該疫苗使用的技術與之前列出的技術不同。 Novavax 是一種亞單位疫苗,這意味着它由模擬 COVID 刺突蛋白的蛋白質製成,隨後會引發免疫反應。 Novavax 與其他創新疫苗(如輝瑞和 Moderna)相比的主要優勢在於它的製造更容易、更快捷,並且需要定期冷藏儲存。
有效性: Novavax 在英國和南非進行的 III 期試驗的結果非常有希望,並測試了該疫苗對英國和南非 COVID 變體的功效。 Novavax 對原始 COVID-19 變體的功效為 90.4%,與其他疫苗相當。該公司宣布對嚴重疾病提供 100% 的保護。此外,該疫苗對感興趣和關注的變體的有效率為 93.2%。該研究包括 29,960 名參與者,結果於 2021 年 6 月公布。
儘管 Novavax 進入現場有點晚,但它是首批針對新出現的 COVID 變體進行全面測試的疫苗之一。 Novavax 仍未獲准公開使用,但該公司預計將於 5 月在美國和英國獲得緊急使用授權。 Novavax 以兩個間隔劑量給藥,就像前面提到的其他變體一樣。
21 年 6 月 1 日更新: Novavax 宣布其疫苗的計劃推出出現了一些令人失望的延遲。該公司承諾在 2021 年下半年申請批准。屆時,Novavax 希望為生產做好更好的準備,並從正在進行的臨床試驗中獲得更多結果。
21 年 6 月 30 日更新: 宣布的 III 期試驗結果顯示有效率高達 90.4%。此外,研究人員發現該疫苗對新型冠狀病毒變種非常有效(93.2%)
21 年 8 月 22 日更新: 迄今為止,Novavax 仍未在任何國家/地區推出,儘管它似乎即將在印度發布。
2021 年 9 月 24 日更新: Novavax Inc. 和印度血清研究所已向世衛組織申請 Novavax 的 COVID-19 疫苗的緊急使用授權。總體試驗表明,在美國和墨西哥的療效為 90.4%。 Novavax 的目標是到 2022 年推出至少 20 億劑 COVID-19 疫苗。
2021 年 9 月 24 日更新: Novavax Inc. 和印度血清研究所已向世衛組織申請 Novavax 的 COVID-19 疫苗的緊急使用授權。總體試驗表明,在美國和墨西哥的療效為 90.4%。 Novavax 的目標是到 2022 年推出至少 20 億劑 COVID-19 疫苗。
11:中國: CANSINOBIO康西諾生物
一種新的中國疫苗最近被批准在中國公開使用。這種疫苗與強生公司一樣,是一種單劑量疫苗,它是一種基於腺病毒的病毒載體疫苗,類似於 Sputnik V。 CanSinoBIO 的疫苗在預防 COVID 症狀方面顯示出 66% 的功效,在預防嚴重疾病方面顯示出 91% 的功效。在接種其單劑量 COVID-19 疫苗的人群中,沒有報告出現嚴重的血栓病例。 CanSinoBIO 的疫苗已在中國、匈牙利、智利和巴基斯坦獲得批准。
2021 年 9 月 24 日更新: 據新聞報道,CanSinoBio 的第一個霧化吸入腺病毒 5 型載體 COVID-19 疫苗(Ad5-nCoV)的 1 期臨床試驗顯示出強大的 IgG 和中和抗體反應。 該公司的一項小型試驗表明,CanSinoBIO 的單劑量疫苗對 6 至 17 歲的兒童是安全有效的。該疫苗的測試劑量低於成人接種的劑量。
12:中國: ZAFIVAX (ZF2001)
第五個也是最新獲批的中國疫苗是由安徽智飛龍科生物製藥有限公司和中國科學院共同開發的疫苗。它是一種亞單位疫苗,類似於 Novavax。目前,全球多個國家正在進行 III 期試驗。製造商表示,該疫苗對 COVID-19 安全有效,但是,尚無公開數據證實這一點。
安徽知非龍康疫苗雖然提供了定期冷藏儲存的便利,但它有一個主要的缺點:三劑方案。接受者必須在劑量間隔一個月內注射 3 次。
13:印度: CADILA INTRANASAL VACCINE卡迪拉鼻內疫苗
截至 2021 年 8 月下旬,印度藥品監管機構建議當地製藥公司 Zydus Cadila 批准緊急使用一種新型無針疫苗。
Cadila COVID-19 疫苗是全球第一個也是唯一一個進入最後測試階段的非注射 COVID 疫苗。
疫苗是鼻內的,這意味着它被噴灑在鼻子內。它以 3 個單獨的劑量給藥。 該建議是在一項涉及 28,000 名參與者的 III 期試驗的積極結果發表之後提出的。研究人員發現,該疫苗對 COVID-19 的有效性為 66.6%。
無針新型冠狀病毒疫苗是否會被批準是一個時間問題。
14:澳大利亞:COVAX - 19 科瓦克斯 – 19
這種新的澳大利亞冠狀疫苗仍未獲得批准,但值得一提。
該疫苗最初由南澳大利亞弗林德斯大學開發。該研究小組於 2021 年 8 月發表了一篇同行評議的文章,顯示了一些有希望的結果。
澳大利亞的 COVAX-19 疫苗是一種基於重組蛋白的疫苗,這意味着它基本上是一種合成蛋白,看起來像 COVID-19 刺突蛋白。它訓練免疫系統識別和攻擊真正的病毒。
重組蛋白疫苗是在培養的昆蟲細胞中產生的。後來它與佐劑結合以進一步刺激免疫系統。
測試仍處於早期階段,但是,研究人員能夠在動物模型中檢測到針對冠狀病毒的有意義的免疫反應。這可能會在 2021 年底轉化為另一種有效的冠狀病毒疫苗。 此外,研究小組預計,澳大利亞的 COVID 疫苗還將降低傳播率,而不僅僅是疾病。人體測試正在進行中,結果似乎很有希望。
|
|
 |
 |
| 實用資訊 | |
|
|
| 一周點擊熱帖 | 更多>> |
| 一周回復熱帖 |
| 歷史上的今天:回復熱帖 |
| 2020: | 人生需要四種修為,學會你就成功了 | |
| 2020: | 人有四苦 | |
| 2019: | 美國以一站式養老市場蓬勃 | |
| 2019: | 女人在每個年齡都有不同的美麗 | |
| 2017: | 幼兒園事件:底層沒有尊嚴整個社會就是 | |
| 2017: | 什麼?“麻”還成為了營養保健品呢! | |
| 2016: | 每天“喝七八杯水”竟然很傷身 | |
| 2016: | 冬季手冷才是病 手涼手熱都有問題 | |