I 新冠的近親病毒都沒有S1/S2處的furin酶切位點
2020年10月5日,華中科技大學同濟藥學院李華教授、張勇慧教授等領導的科學團隊在Cell子刊iScience上發表了一篇重磅論文:
Furin A Potential Therapeutic Target for COVID-19(Furin,COVID-19的潛在治療靶點)
https://www.cell.com/iscience/fulltext/S2589-0042(20)30834-8?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS2589004220308348%3Fshowall%3Dtrue
論文部分要點包括:
1、在新冠所屬的冠狀病毒β譜系B支系,只有一種病毒具有(S1/S2處的)furin酶切位點,該病毒就是新冠病毒;
2、通過在線軟件搜索發現,所有與新冠病毒S蛋白(spike蛋白,刺突蛋白)同源性(相似度)大於40% 的冠狀病毒都不具有(S1/S2處的)furin酶切位點;
3、新冠S1/S2處(S蛋白S1、S2亞基交界處)特有的furin酶切組合“RRAR”(精氨酸-精氨酸-丙氨酸-精氨酸)在其家族中是獨一無二的,該組合的出現是新冠異於所有近親的獨特插入“PRRA”(脯氨酸-精氨酸-精氨酸-丙氨酸)導致的。
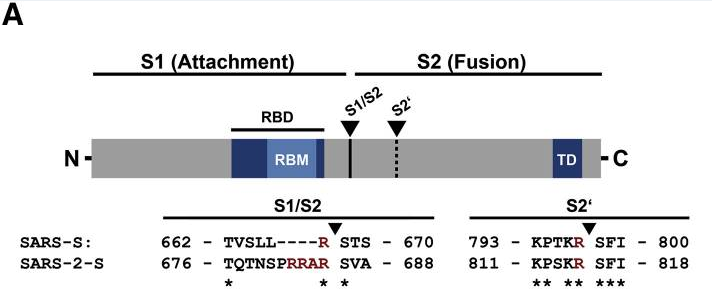
新冠病毒(SARS-2)與SARS病毒S1/S2處氨基酸序列差異對照圖
furin酶切位點指符合furin蛋白酶“RXXR”識別標誌的氨基酸組合。由上圖可見,相比SARS,新冠在S1/S2處多出來四個氨基酸“PRRA”,其中的“RRA”與其後的“R”組成了新冠的furin酶切位點“RRAR”(furin蛋白酶將從最後一個R處對S蛋白進行切割)。這裡涉及兩個四氨基酸組合,一是新冠相對於SARS等近親病毒的獨物插入“PRRA”,二是由此插入產生的新冠furin酶切組合“RRAR”,請大家注意區分。
4、新冠的furin酶切位點不太可能是從MERS、HCoV-HKU1 等病毒進化而來的,從生物信息數據庫目前可用的序列中,我們很難找到其來源,或許還有很多進化的中間序列有待發現。
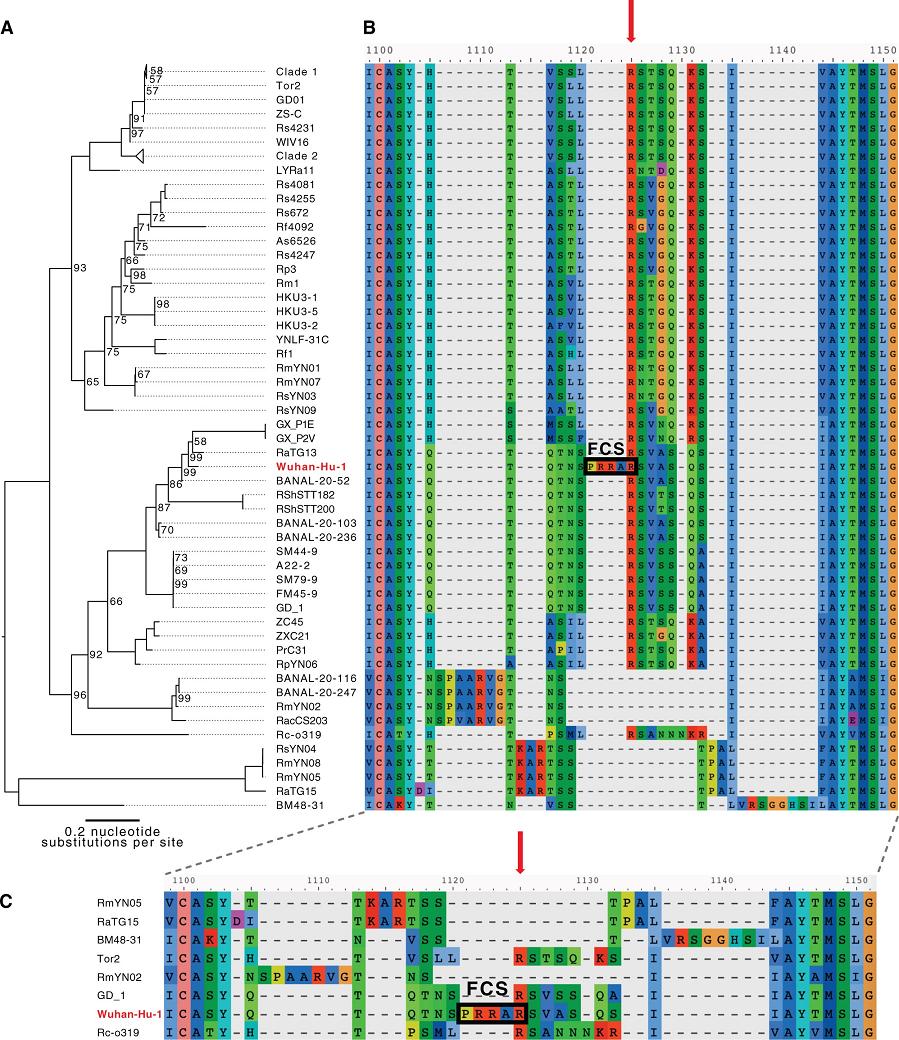
新冠病毒(Wuhan-Hu-1毒株)與進化樹中其它冠狀病毒在S1/S2附近氨基酸序列對照圖
上圖來自其它論文。由圖可見,進化樹中其它病毒在S1/S2處都空缺新冠獨有的“PRRA”,新冠“憑空”多出的這四個氨基酸在圖中非常突兀、刺眼。
很多人認為新冠病毒進化自蝙蝠冠狀病毒,然而,在新冠所屬的β譜系中,沒有一種蝙蝠冠狀病毒具有(S1/S2處的)furin酶切位點(更別說具有新冠特有的RRAR酶切組合);有人認為,新冠病毒的中間宿主是穿山甲,但是,同樣地,沒有一種穿山甲冠狀病毒具有(S1/S2處的)furin酶切位點。
那麼,新冠功能極其強大的furin酶切位點--其特有的“RRAR”furin酶切組合到底有沒有出處?它是從石頭縫裡蹦出來的嗎?它是新冠的首創嗎?它真的毫無出處可尋嗎?
找到“RRAR”的出處,並判斷新冠中“RRAR”來源的自然性或人為性,這就是本文要解決的問題。
II 蝙蝠冠狀病毒RmYN02刺突蛋白中的“P-AA”組合
2020年5月10日,來自山東第一醫科大學、中國科學院北京生命科學研究所、中國科學院西雙版納熱帶植物園、中國科學院武漢病毒研究所、澳大利亞悉尼大學等7所機構的科學家、學者在《細胞》(Cell)旗下子刊《現代生物學》(Current Biology)在線發表了如下論文:
A novel bat coronavirus closely related to SARS-CoV-2 contains natural insertions at the S1/S2 cleavage site of the spike protein
(一種與SARS-CoV-2 密切相關的新型蝙蝠冠狀病毒在刺突蛋白的S1/S2切割位點含有天然插入物)
https://www.cell.com/current-biology/fulltext/S0960-9822(20)30662-X?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS096098222030662X%3Fshowall%3Dtrue
論文指出:
去年(2019年)在雲南勐臘縣的蝙蝠樣本中發現了一種蝙蝠冠狀病毒RmYN02,該病毒S蛋白S1、S2亞基交界處也存在三個插入氨基酸(殘基)PAA。因此,新冠S1、S2交界處的“PRRA”組合在近親中並非獨一無二;RmYN02病毒S1/S2處PAA組合的發現,是新冠病毒相同位置處“PRRA”組合不是“人工插入”,及新冠起源於自然的有力證據。
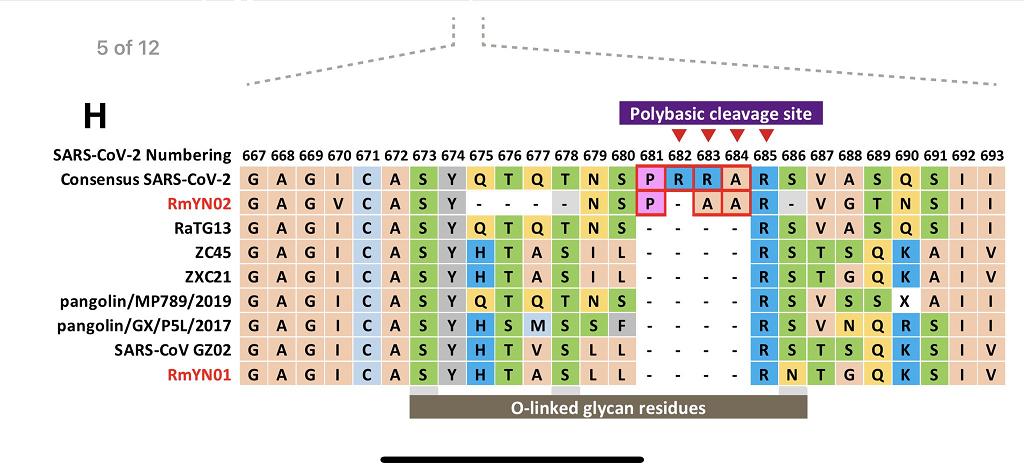
RmYN02與新冠S1/S2附近氨基酸序列對照圖(摘自論文)
關於RmYN02的一些背景說明。RmYN02是與新冠第二相似的病毒,僅次於相似度為96.2%的另一蝙蝠冠狀病毒RaTG13。RmYN02與新冠的全基因組序列一致性為93.3%,二者在最長編碼基因區1ab的一致性達到97.2%。
雖然整體相似度較高,但某些局部的相似度卻較低。二者刺突蛋白(S蛋白)基因序列的相似度僅為71.8%,二者RBD(Receptor Bind Domain,受體結合域,S蛋白S1亞基的一部分,決定冠狀病毒的受體結合能力,細胞進入能力)的相似度更低至62.4%。RmYN02不可能是新冠的直接或較近進化祖先。
上述7所機構的論文靠譜嗎?非常非常不靠譜。為啥?
1、RmYN02的基因序列是新冠疫情發生後才公布的(RaTG13也是如此),如果公布於疫情發生前,將可信、有說服力得多;
2、RmYN02隻有基因序列,沒有病毒毒株(RaTG13也是如此),它的基因序列不是對病毒毒株測序得出的,而是“分析”蝙蝠遺留物(排泄物等)中的RNA片斷,用不完整的RNA殘片結合人為推測“拼裝”、“延展”出來的,其“分析”、“拼裝”過程是不透明和缺乏客觀性的。RmYN02可能根本沒有物理存在過。
3、研究發現,RmYN02的基因序列很可能存在數據造假或數據污染的問題;
4、論文未公開對齊算法,按照多種對齊算法,都得不出RmYN02在S1/S2處有PAA插入的結果。
2021年5月27日,加拿大Youthereum 遺傳學公司的Yuri Deigin,奧地利因斯布魯克大學微生物學系的Rossana Segreto在BioEssays上發表了一篇論文:
SARS-CoV-2′s claimed natural origin is undermined by issues with genome sequences of its relative strains
Coronavirus sequences RaTG13, MP789 and RmYN02 raise multiple questions to be critically addressed by the scientific community
(SARS-CoV-2 聲稱的自然來源受到其相關毒株基因組序列問題的破壞
冠狀病毒序列RaTG13、MP789 和RmYN02 引出了多個需要科學界認真解決的問題)
https://onlinelibrary.wiley.com/doi/full/10.1002/bies.202100015
註:論文發表的時間,恰恰是拜登宣布啟動美國情報機構新冠溯源調查的第二天。
論文對中國科學家、學者在疫情發生後拋出的,用以證明新冠病毒來自自然界的三個病毒RaTG13、MP789 (一種馬來亞穿山甲冠狀病毒,其RBD與新冠病毒高度相似)、RmYN02提出了強烈質疑。
論文對三種病毒都提出了多項質疑。作為質疑之一,論文指出,前述7所機構的RmYN02相關論文未公開對齊算法,二位研究者使用了幾種簡潔、合理的對齊算法,都得不出中國學者對比圖顯示的,RmYN02的“PAA”恰好位於S1/S2位置處的結果。我下面即將展示的對比圖來自其它論文,它比兩位學者論文中的對比圖更直觀、清晰。圖中的Wuhan-Hu-1是復旦張永振團隊測序並最早上傳基因序列到國際生物信息數據庫(約在2020年1月5日)所用的新冠毒株,其序列因測序的極高質量而成為國際公認的新冠病毒基因組參考序列;另外,圖中的FCS即furin酶切位點(Furin Cleavage Site)
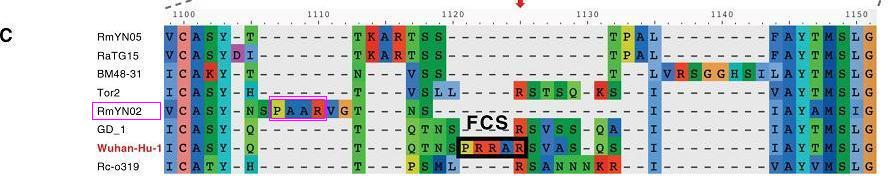
由上圖可見,按常用對齊算法,RmYN02的“PAA”插入根本不在S蛋白S1、S2亞基交界處;在S1/S2處,RmYN02不僅沒有任何新增氨基酸,反而比新冠其它近親病毒缺失了更多的氨基酸。
為勉強證明自然來源論,中國科學家、學者先後輕率地拋出了數個存在很多問題的“證據”,落下了中國捂蓋子的口實。新冠病毒源自中國之外,但新冠疫情的發生並非與中國無關,中國政府確實有捂蓋子的動機;但是,很少有人認識到,中國科學家的所作所為,並不是簡單的自發行為,它們與疫情發生第一年全球病毒學界、科學界的整體行為完全一致,中國科學家更是在追隨、配合全球病毒學界的集體捂蓋子行動。
病毒學界為什麼要集體捂蓋子?如果“新冠病毒是病毒學家設計、製造出來的”這一結論得到公認,那麼,全球病毒學家們的職業活動、收入、生計都將受到嚴重影響。他們的研究行為將受到新出台的法律的極為嚴格的約束,並不得不時刻敞開在全社會的審視、監督之下;他們不能再隨心所欲地進行危險研究、肆意改造病原體,扮演造物主,享受造物主的極致成就感;他們的科研項目、收入來源將大幅萎縮,他們申請研究經費將困難重重;他們還將光環破滅,名聲掃地。。。
親身參與危險病原體功能增益研究的病毒學家們需要捂蓋子;領導病毒學界,積極支持、推動功能增益研究的政府官員們,如弗朗西斯·柯林斯、安東尼·福奇等人需要捂蓋子;在2017年12月19日撤銷奧巴馬功能增益研究暫停令,全面重啟美國危險病原體功能增益研究的川普和共和黨人不僅需要捂蓋子,還需要栽贓嫁禍,製造替罪羊;為了美國的利益,為了美國的聲譽,全球病毒學界的領導者、功能增益研究第一大國--美國的政、科、媒各界都需要捂蓋子,都需要甩鍋動物或製造替罪羊,他們恐懼真相大白,想法設法捂蓋子、撒謊、造謠、構陷才能讓他們心神稍安。
2020年2月19日,國際頂級醫學期刊《柳葉刀》(The Lancet)在線發表了一篇由8個國家(英、德、美、澳、荷蘭、西班牙、馬拉西亞、中國)的27名著名病毒學家、流行病學家聯合簽署的一份聲明:
Statement in support of the scientists, public health professionals, and medical professionals of China combatting COVID-19
支持抗擊COVID-19 的中國科學家、公共衛生專業人員和醫療專業人員的聲明
https://www.thelancet.com/lancet/article/S0140-6736(20)30418-9
表面上,發表這份聲明是為了支持中國;實際上,醉翁之意不在酒,它的真正目的是及時堵口“實驗室來源論”。聲明中說:在這次疫情中相關數據迅速、公開且透明的共享如今正受到關於該疾病起源的謠言和錯誤信息的威脅。“我們在此共同強烈譴責認為該新型冠狀病毒疾病COVID-19並非自然起源的陰謀論。”
這27名頂尖病毒學、流行病學家以其科學權威的身份將“自然來源論”指定為新冠起源的唯一正確可能,將“實驗室來源論”貶斥、誣衊為謠言、錯誤信息和“陰謀論”。他們假裝不知道病毒學界完全有能力設計、製造新冠病毒,假裝不知道美國在疫情發生兩年前的2017年12月19日全面重啟了危險病原體的功能增益改造研究,假裝不知道以美國的科技水平和以往的經驗積累,在兩年的功能增益改造研究中足以製造出跨科屬病毒的集大成者--新冠病毒。疫情發生後。他們不去深入分析、全面探究新冠病毒來源的各種可能性,而是第一時間去堵嘴、禁聲,迫不及待地對質疑者、異議者加以污名、扣帽子。他們為什麼打着科學的幌子反科學,以科學的名義禁止科學討論、辯論? 他們為什麼那麼懼怕“實驗室來源論”?為什麼那麼懼怕有人質疑危險病原體功能增益改造研究?他們是在為誰捂蓋子,他們是在為哪個國家捂蓋子?他們是在為中國病毒學家捂蓋子嗎?他們是在為中國政府捂蓋子嗎?美國國家科學院、工程院、醫學院三大院的院長力挺“野生動物來源論”是為中國捂蓋子嗎?安東尼·福奇和國立衛生院院長弗朗西斯·柯林斯是在為中國一再撒謊、遮掩嗎?美國三大社交平台Twitter、Facebook、Youtube在長達一年半的時間裡無比賣力地刪帖、禁言“實驗室來源論”,他們是在為中國着想,為中國政府效勞嗎?
新冠病毒源自何處,新冠病毒是哪個國家製造的,他們早就心知肚明了。
從新冠病毒產生到新冠病毒出現在武漢,這一過程的曲折程度恐怕超出了絕大多數人的想象。但是,可以充分確定的是,新冠病毒根本不可能是武漢病毒研究所(事故)泄漏的,新冠病毒也根本不是武漢病毒研究所設計、製造的。關於前者,詳盡分析可參見:
武漢病毒研究所是否泄漏了新冠病毒
下文則對兩個問題都給出了簡明分析:
美國之音年終謊言報道(二)
新冠疫情發生後,中美兩國都第一時間積極甩鍋動物(重啟美國危險病原體功能增益研究,積極捏造、構陷,栽贓嫁禍,製造替罪羊的川普和某些共和黨政客除外),但兩者甩鍋的側重點不同,中國側重於:新冠不是(武漢本地)實驗室泄漏的;美國則側重於:新冠不是實驗室製造的。
疫情發生頭一年,中美甩鍋動物的共同目的是,證明新冠疫情不是人為造成的,不是一場人禍。
病毒的首先發現地或首先暴露地不等於病毒的來源地或初始產生地。新冠溯源應該分解為兩個環節的調查、分析:
1、新冠病毒產生自何處;
2、新冠病毒是如何來到或出現在武漢的。
我最近的幾篇文章聚焦的是第一個問題。
III 小鼠肝炎病毒MHV-A59的furin酶切位點與新冠相似
小節I、II已指出,β譜系B支系除新冠外的所有冠狀病毒,β譜系中的所有蝙蝠冠狀病毒,新冠的所有近親病毒(S蛋白相似度>40%)無一具有S1/S2處的酶切位點,無一在S1/S2處具有與新冠相同或相近的氨基酸插入。
把視野擴展到新冠的近親之外,擴展到其它支系,其它譜系,能不能有所發現呢?
除了新冠所在的B支系,冠狀病毒β譜系還有A、C、D三個支系,這三個支系有一些病毒在S1/S2處也有furin酶切位點,其中,最著名的是A支系的小鼠肝炎病毒MHV(Mouse Hepatitis Virus)的幾個株系。在小鼠肝炎病毒MHV的20多個株系(超過25個株系)中,被最研究最多的是毒性(致病力)最強的三個株系:MHV-JHM、MHV-3、MHV-A59,這三種病毒之所以毒性強,就是因為它們在S1/S2處都有furin酶切位點。
先看 MHV-A59。
小鼠肝炎病毒MHV-A59的感染始於呼吸道,而後擴散至肝臟、肺、腦等器官。肝臟是其最主要的感染部位,感染結果是導致重型肝炎;大腦另一個重要感染部位,感染結果是引發腦膜腦炎及各種急、慢性神經性症狀;MHV-A59還能刺激小鼠自身的免疫反應,使急性感染後存活的小鼠患上神經元慢性脫髓鞘病(demyelination)。
MHV-A59在S蛋白的S1/S2處也有furin酶切位點,其furin酶切組合為“RAHR”(新冠的furin酶切組合為“RRAR”);MHV-A59在S1/S2處的完整多元酶切組合為“RRAHR”,除了後四個RAHR組合可被furin蛋白酶識別切割之外,包括第一個“R”在內的每一個精氨酸“R”還可被胰蛋白酶切割。“RRAHR”對應的新冠S1/S2處的五個氨基酸為“PRRAR”,二者都含有符合“RXXR”格式的furin酶切組合,都含有“RRA”組合。見下圖。

新冠與MHV-A59 S蛋白aa(amino acid,氨基酸)序列對照圖。
圖中,Query序列對應新冠S蛋白(Genbank ID:YP_009724390.1),Sbjct(Subject)序列對應MHV-A59 S蛋白(GenBank ID:YP_009824982.1)。Query序列與Sbjct序列之間還有一行,這一行標出了二者相同的氨基酸,並用+號標出了二者不同但性質類似的氨基酸。
新冠病毒可能是MHV-A59自然演化產生的嗎?這是不可能的,它們的差距實在太大了。
新冠的全基因組序列僅有26%與MHV-A59的全基因組序列具有可比對性(即二者74%的序列幾無相似之處),二者26%的可比對部分的一致性僅為66.02%;
新冠S蛋白的aa(amino acid,氨基酸)序列有70%與MHV-A59可比對,二者70%的aa序列可比對部分的一致性僅為36.45%。
雖然S1/S2處的furin酶切位點很相像,雖然同處冠狀病毒的β譜系,但分處B、A兩個支系的新冠和MHV-A59基因結構、親緣關係相去甚遠,它們很可能500萬年前就已經分家了,它們的進化距離相差十個銀河系以上。
furin酶切位點與新冠最相像的病毒還不是MHV-A59。
IV 最毒鼠肝炎病毒MHV-JHM S1/S2處的furin酶切組合也是RRAR
在小鼠肝炎病毒的20多個株系中,有一個株系比MHV-A59毒性強得多。
MHV-JHM是毒性最強的小鼠肝炎株系,具有高度的神經毒性,它引發的強烈腦炎能使小鼠高比例癱瘓、死亡。在MHV各株系中,MHV-JHM毒性最強,被研究的也最多。
在MHV-JHM S1/S2處,我們終於找到了苦苦尋覓的新冠“RRAR”furin酶切組合,見下圖:
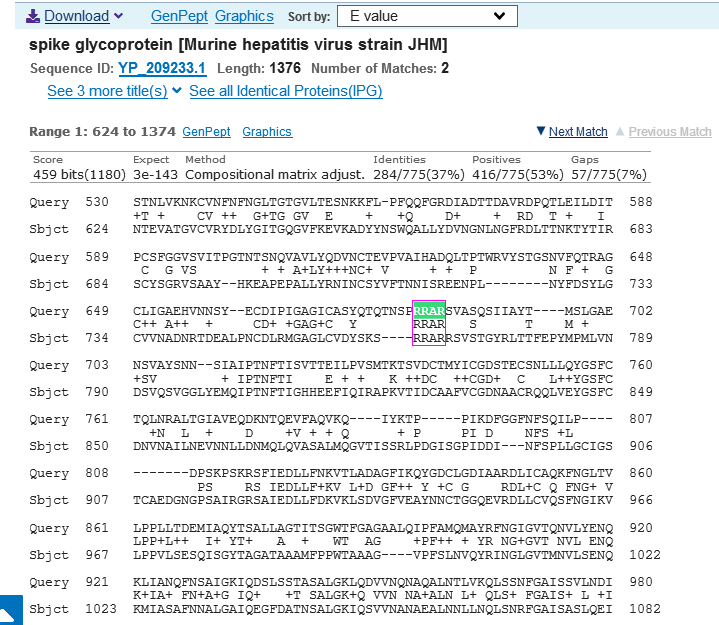
新冠與MHV-JHM S蛋白(GenBank ID:YP_209233.1)aa序列比對圖。Query:新冠;Sbjct:MHV-JHM
MHV-JHM S1/S2處的“RRAR”是該處多元furin酶切組合“RRARR”的一部分(包含兩個furin酶切組合“RRAR”、“RARR”)。MHV-A59的多元酶切組合是“RRAHR”,二者有一個氨基酸差異,A59多元酶切組合的倒數第二個氨基酸是組氨酸(H),而JHM多元furin酶切組合的倒數第二個氨基酸則是精氨酸(R)。後文將說明,這一差異對它們的致病力影響巨大。
毒性顯著強於MHV-A59的另一小鼠肝炎病毒株系是MHV-3,它S1/S2處也有“RRAR”furin酶切組合。見下圖:
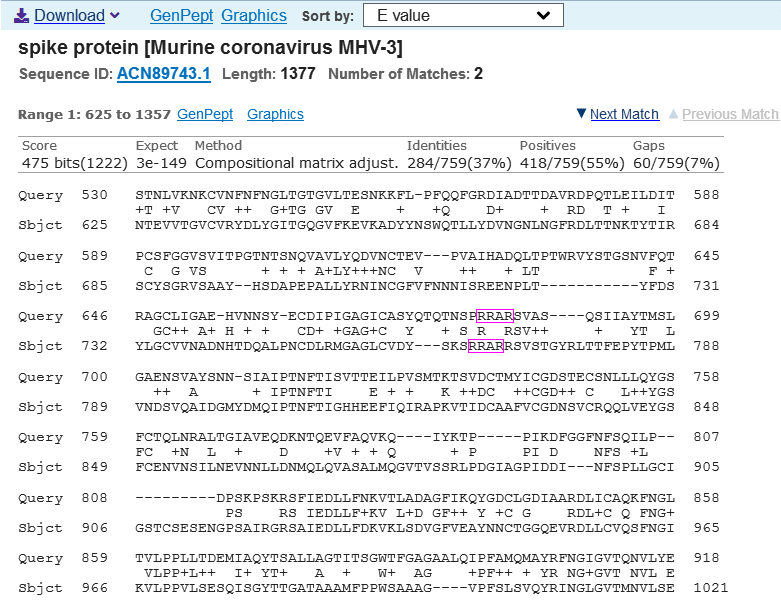
新冠與MHV-3 S蛋白(GenBank ID: ACN89743.1)aa序列比對圖。Query:新冠;Sbjct:MHV-3
MHV-3在S1/S2處的多元furin酶切信號也是“RRARR”,與MHV-JHM相同。
MHV-JHM、MHV-3都有強烈的神經毒性。新冠病毒對人大腦和神經系統的感染、侵犯很可能也與S1/S2處的“RRAR”furin酶切組合有關。
新冠病毒可能是MHV-JHM或MHV-3自然演化產生的嗎?這同樣是不可能的。小鼠肝炎病毒各株系都位於β譜系的A支系,它們與B支系的新冠雖是“鄰居”,但親緣關係非常非常遠,結構差異非常巨大。具體而言,
新冠v.s.MHV-JHM:
新冠的全基因組序列僅有23%與MHV-JHM的全基因組序列具有可比對性(即二者77%的序列幾無相似之處),二者23%的可比對部分的一致性僅為66.79%;
新冠S蛋白aa(amino acid,氨基酸)序列有92%與MHV-JHM 可比對,但可比對部分的一致性僅為36.65%。
新冠v.s.MHV-3:
新冠的全基因組序列僅有24%與MHV-3可比對(即二者76%的序列幾無相似之處),二者24%的可比對部分的一致僅為66.27%;
新冠S蛋白aa序列有91%與MHV-3可比對,但可比對部分的一致性僅為37.42%。
新冠與最毒鼠肝炎病毒MHV-JHM、MHV-3的furin酶切組合相同,這是一個巧合嗎?
在小鼠肝炎病毒的二十多個株系中,被研究最多、知名度最高的就是毒性最強的MHV-JHM(被研究次多的是MHV-A59和MHV-3)。詭異的是,疫情發生後,在本文之前,我從未發現有論文或科學文章明確指出:新冠病毒在相同的位置使用了與MHV-JHM和MHV-3相同的“RRAR”furin酶切組合。
V 某些高毒性貓冠狀病毒S蛋白中也含有“RRAR”組合
貓是鼠的天敵。在貓傳染性腹膜炎病毒 (FIPV,貓冠狀病毒的兩個分支之一,可引發致命的貓傳染性腹膜炎)的某些毒株中,也存在與MHV-JHM、MHV-3相同的,含有“RRAR”的“RRARR”多元furin酶切組合。見下圖:
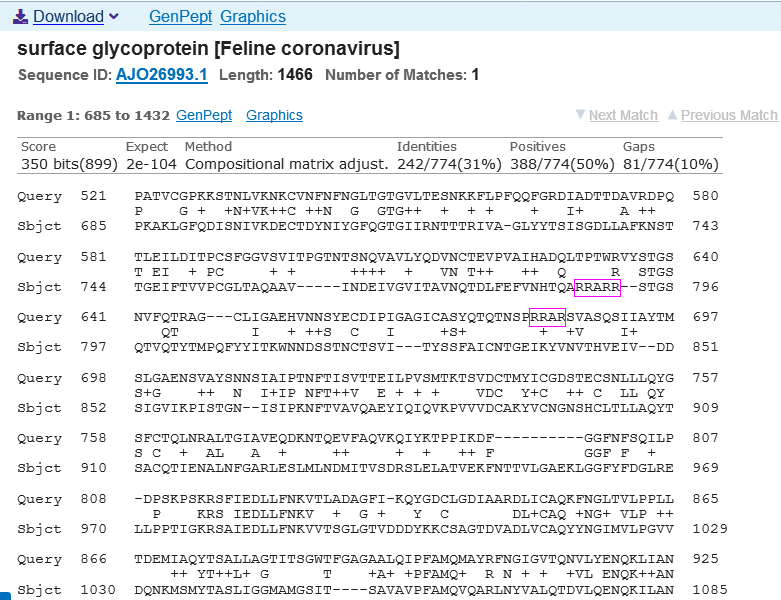
新冠S蛋白、一種FIPV病毒S蛋白(Genbank ID:AJO26993.1 )aa序列比對圖。Query:新冠,Sbjct:FIPV
在上述Blast(一種基因或蛋白比對工具)比對結果中,新冠的“PRRAR”與FIPV的“RRARR”是錯開的,後者的位置比較靠前,似乎位於S1亞基中。我暫時不能確定“RRARR”是位於S蛋白的S1/S2處,還是位於S1/S2之前的S1亞基中。
新冠病毒可能自然演化自貓冠狀病毒嗎?這更不可能了。貓冠狀病毒與新冠病毒不僅不屬於同一支系,而且不屬於同一冠狀病毒譜系。新冠屬於β譜系,而貓冠狀病毒屬於α 譜系。
一些與新冠“血緣”關係遙遠的高毒性冠狀病毒中的“RRAR”furin酶切組合為什麼出現在了新冠之中,這是巧合嗎?很明顯,新冠中的“RRAR”來自對這些高毒性冠狀病毒的人為借鑑。
VI 新冠S1/S2處的furin酶切位點是自然重組引入的嗎?
新冠病毒不可能是MHV-JHM、MHV-3、MHV-A59、貓冠狀病毒等有相同“RRAR”組合或相近furin酶切組合的冠狀病毒自然演化而來的;那麼,其“RRAR”可能是MHV-JHM、MHV-3或貓冠狀病毒與新冠的近親病毒自然重組產生的嗎?
這恐怕也沒有可能。理由如下:
1、MHV-JHM或MHV-3或貓冠狀病毒與新冠病毒的某一近親發生自然重組需要以下條件:雙方感染一個共同的宿主。然而,三種病毒的宿主是小鼠或貓,而新冠近親的宿主是蝙蝠(主要是菊頭蝠),鼠冠狀病毒、貓冠狀病毒感染蝙蝠,或蝙蝠冠狀病毒感染鼠、貓的情況未見報道過,它們感染同一宿主的條件恐怕難以滿足;
2、隨機、無目的的自然重組是粗線條、不精準的。如果新冠S1/S2處的“PRRA”是自然重組引入的,那麼重組時獲得的應當是包含“PRRA”在內的一截氨基酸序列,而不是只獲得了幾個氨基酸。然而,前文列出的所有aa序列比對結果都顯示,在“PRRA”或“RRAR”兩側,新冠與相關病毒的氨基酸序列明顯不同,包括四氨基酸組合在內,沒有一個比對圖中存在長於7個氨基酸的相同序列片斷。這樣的重組相當於是說,我只要你的PRRA或RRAR,其它的統統不要。如此精準、有目的的重組在自然界中極難發生;但在實驗室中,把借鑑自其它病毒的氨基酸組合設計、插入到改造病毒中,則能輕而易舉地促成這種“重組”。
3、2020年1月29日,一組希臘科學家在Elsevier上發表了如下論文:
Full-genome evolutionary analysis of the novel corona virus (2019-nCoV) rejects the hypothesis of emergence as a result of a recent recombination event
2019-nCoV的全基因組進化分析拒絕了(該病毒)因最近的重組事件而出現的假設
https://www.sciencedirect.com/science/article/pii/S1567134820300447
由論文標題即知,希臘科學家的全基因組進化分析表明,新冠病毒不是最近的重組事件產生的。
基於論文可判斷,如果“PRRA”組合是重組得來的,那麼獲得“PRRA”的重組不是最近發生的,而是發生於較早前的某個時間。如果新冠祖先通過自然重組獲得“PRRA”組合已經有一段時間了,那麼,新冠祖先也會將這一組合遺傳給其它後代,也就是新冠的某些近親。但是,文首已經明確指出,新冠的近親病毒無一具有“PRRA”組合。
因此,新冠S1/S2處的“PRRA”組合也不是重組獲得的。
新冠的近親無一自然演化出“PRRA”或“RRAR”;有“RRAR”的鼠、貓冠狀病毒(一百萬年內恐怕)不可能自然演化為新冠;“RRAR”也不是新冠的近親病毒與鼠、貓冠狀病毒重組獲得的。那麼,“PRRA”來自哪裡?只能是實驗室設計、插入的。
VII RRAR是得到業界研究反覆證明的非常優異的furin酶切組合
論文一
1995年12月20日,荷蘭萊頓大學醫學院病毒學系的四位科學家在Elsevier上發表了如下論文:
Mutational Analysis of the Murine Coronavirus Spike Protein: Effect on Cell-to-Cell Fusion
鼠冠狀病毒刺突蛋白的突變分析:對細胞間融合的影響
https://www.sciencedirect.com/science/article/pii/S0042682285700566?via%3Dihub
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7131709/pdf/main.pdf
論文指出:
MHV-A59株系的切割信號為“RRAHR”,MHV-JHM株系的切割信號為“RRARR”,它們的切割信號只有一個氨基酸差異。如果將A59切割信號中的組氨酸(H)替換為精氨酸(R)(替換後,A59切割信號中的furin酶切組合由“RAHR”變為“RARR”,同時,切割信號中增加了另外一個furin酶切組合“RRAR”),那麼,得到的(切割信號與JHM相同的)A59人工變異體S蛋白的水解切割(切割分離S1、S2亞基)效果將顯著提高。這表明,JHM切割信號中的倒數第二個精氨酸R對其S蛋白的切割效果非常重要。
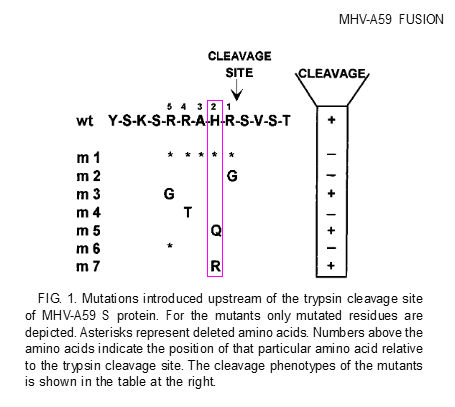
上圖是論文中的配圖。圖中的wt(wild-type)指未改造的MHV-A59,論文設計了7個人工變異體,最下方的m7就是用精氨酸(R)替換組氨酸(H)得到的,用來模擬JHM切割信號的A59變異體。
論文二
1998年2月,三位費城賓夕法尼亞大學的科學家在Journal of Virology發表了如下論文:
The Spike Protein of Murine Coronavirus Mouse Hepatitis Virus Strain A59 Is Not Cleaved in Primary Glial Cells and Primary Hepatocytes
小鼠肝炎病毒MHV-A59 的刺突蛋白在原代神經膠質細胞和原代肝細胞中不會被裂解
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC124642/
論文指出:
1、MHV-3與MHV-JHM共有的furin切割信號“RRARR”可能比MHV-A59的furin切割信號“RRAHR”更好,前二者的S蛋白更容易被細胞內的furin樣蛋白酶切割;
2、MHV-3的S蛋白在原代肝細胞中被切割,但MHV-A59的S蛋白在原代肝細胞中不被切割;
3、在成纖維細胞系中,MHV-3 S蛋白的切割似乎比MHV-A59更完整;
4、如果將MHV-A59的切割信號“RRAHR”突變(人工改造)為MHV-3的切割信號“RRARR”,將導致更完全的切割,(人工)突變體的切割效果與MHV-3的切割效果一致。
論文三
2020年10月5日,華中科技大學同濟藥學院李華教授、張勇慧教授等領導的科學團隊在Cell子刊iScience上發表了如下論文:
Furin A Potential Therapeutic Target for COVID-19(Furin,COVID-19的潛在治療靶點)
https://www.cell.com/iscience/fulltext/S2589-0042(20)30834-8?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS2589004220308348%3Fshowall%3Dtrue
論文指出:新冠S蛋白S1/S2處的“RRAR”基序是一個非常高效的furin酶切組合,它很容易被furin蛋白酶識別和水解,相比經典的furin酶切組合“RVRR”,“RRAR”在furin蛋白酶作用下的水解、裂解效率是“RVRR”的2倍。
註:“RVRR”是土耳其發現的一種H7N1高致病性禽流感病毒株系的furin酶切組合。
新冠是不是事先知道RRAR特別棒,所以特意在S1/S2這一關鍵位置“進化”出了所有近親都沒有的RRAR?
VIII結論
本文結論如下:
1、新冠病毒S1/S2處的furin酶切位點是人為設計、插入的;
2、有人借鑑了最毒鼠冠狀病毒MHV-JHM等高毒性鼠、貓冠狀病毒的結構,將它們S1/S2處的furin酶切組合“RRAR”應用到了新冠病毒中,以賦予新冠病毒強大的致病能力。
3、對新冠病毒與MHV-JHM、MHV-3 S1/S2處酶切組合的明顯關聯,疫情發生至今,病毒學界始終一言不發,一直在集體捂瞞。不捂瞞的話,人們將很快意識到,新冠病毒S1/S2處的“RRAR”是借鑑MHV-JHM、MHV-3等高毒性病毒,人為引入的。
(正文完)
相關文章:
誰設計、製造了新冠病毒(二 上)














