和筆者一起溯源吧,和筆者一起破案吧,我們共同揭示、揭穿那些實驗室設計、製造的病毒,揪出、斬斷隱藏着的邪惡黑手。
SARS-CoV-2溯源是一件非常重要的事情,這件事不能沒有人做,不能不了了之。做這件事的人,應當對真相充滿渴望,應當不加遮掩地向公眾全面袒露信息,應當察真辨偽、堅持不懈;做這件事的人,不應當裝模作樣、敷衍了事、隱匿信息、渾水摸魚、轉移視線、甩鍋嫁禍、掩蓋真相、愚弄公眾。克服巨大困難、付出巨大努力堅持溯源的人,應當得到鼓勵和支持,而不是受到冷漠對待和壓制。
肯請平台,對這些挖掘了大量科學論文,披露了大量第一手SARS-CoV-2研究成果,披露了大量第一手溯源證據、線索、疑點,論據確鑿、充分,邏輯嚴謹、周密,凝聚了作者大量心血,有價值、有說服力,全網獨一無二,可能意義深遠的原創溯源文章,請不要讓它們困處一隅、鮮有人知,請多給予它們一些溫暖和支持,多給予它們一些展示、傳播的機會,讓它們多得到一些討論、交流的機會,或接受批駁、批判的機會吧!
接續:
新冠的跨物種、跨生物界、超生物基因之雜記
I SARS-CoV-2對冠狀病毒基因的繼承、借鑑、模仿、優化、集成(續四)
SARS-CoV-2擁有太多它的“近親”、它的同類無一具有的神奇結構、神奇能力。
SARS-CoV-2的的神奇結構、神奇能力,不僅來自冠狀病毒,來自非冠狀病毒,而且來自微生物、生物、非生物。SARS-CoV-2與非“近親”冠狀病毒,與非冠狀病毒,與致病細菌,與寄生蟲,與人體結構,與人類蛋白、蛋白酶、激素,與低等動物,與植物、與細菌毒素,與動物毒素,與醫療藥劑,與生物醫學專利都存在離奇的結構、能力巧合。
SARS-CoV-2是廣為參照、借鑑、模仿,集眾多跨物種基因、跨生物界基因、超生物基因於一身的基因工程/轉基因集大成者。
這裡所說的結構巧合,包括基因序列(核苷酸序列)巧合、氨基酸序列巧合,以及氨基酸序列對應的多肽的空間構象巧合。
這裡所說的能力巧合,包括感染、致病能力巧合,免疫對抗能力巧合,人體蛋白結合能力巧合,以及其它生理功能、生理特性巧合,如氧化活性巧合、蛋白降解功能巧合等等。這裡所說的免疫對抗能力,包括免疫破壞能力,免疫逃避、免疫屏蔽能力,免疫干擾、免疫抑制能力。免疫對抗能力其實也是致病能力。
只有SARS-CoV-2是人造的嗎?不,已出現的三種嚴重致病冠狀病毒,全都疑點重重。SARS-CoV-2的出現,將他們以前的隱秘罪行也連帶着暴露了。
在SARS-CoV-2的眾多巧合對象中,有一種冠狀病毒。這種冠狀病毒與SARS-CoV-2總體差異巨大、進化距離非常遙遠;兩者的發現地也遠隔重洋、相距萬里。然而,這兩種天差地遠的冠狀病毒,卻如同心有靈犀的靈魂知己,又如同藝出自同門的師兄弟,它們無比默契地聯手創造了多項極其神奇的、極低概率的結構、能力巧合。SARS-CoV-2的這個靈魂知己、同門師兄弟就是MERS-CoV。
SARS-CoV-2與MERS-CoV的結構、能力巧合將分兩部分介紹,本文介紹第一部分。兩篇文章將展示的SARS-CoV-2、MERS-CoV在感染、致病的關鍵位點、關鍵環節的多項離奇、反常巧合將有力地揭示一個驚人的結論:不只SARS-CoV-2是人造的,MERS-CoV也來自實驗室!這兩種病毒的設計思路高度關聯、高度契合、一脈相承,它們極有可能出自同一團隊或同一團伙之手。
MERS-CoV(上)
MERS-CoV,全名為Middle East Respiratory Syndrome Coronavirus,中東呼吸綜合症冠狀病毒。MERS-CoV 2012年9月發現於沙特,是三種嚴重致病冠狀病毒中第二個出現的病毒。MERS-CoV的(短期)致死率(35%)遠高於SARS-CoV-2,但它的傳播能力遠低於SARS-CoV-2。
SARS-CoV-2是β譜系B支系(乙型冠狀病毒屬Sarbe亞屬)冠狀病毒,MERS-CoV 是β譜系C支系(乙型冠狀病毒屬Merbe亞屬),雖然隸屬同一譜系(屬),但兩者差異非常巨大,進化距離非常遙遠。SARS-CoV-2、MERS-CoV全基因組序列(核苷酸序列)僅28%可比對(Blast比對結果中的Query Cover值為28%),可比對部分相似度為67.06%;兩者Spike蛋白aa序列(amino acid sequence,氨基酸序列)76%可比對,可比對部分相似度為僅為34.91%;兩者Spike蛋白決定受體結合能力的RBD(receptor binding domain,受體結合域)部分的aa序列相似度僅為19.1%。然而,神奇的是,RBD相似度如此之低的兩種病毒,不僅都能結合DPP4,都能以DPP4為感染受體,而且,它們的DPP4結合機制、結合細節高度相似!
1、DPP4結合能力、利用能力巧合
DPP4,dipeptidyl peptidase IV,二肽基肽酶4,是一種非常重要的人體絲氨酸蛋白酶兼多功能蛋白。DPP4的生理、病理功能包括血糖控制、代謝調節(如細胞遷移和增殖)、免疫調節、結合其它蛋白/蛋白酶、作為細胞膜表面受體介導病毒、病原體感染等等。
作為一種多功能蛋白,DPP4有多個名稱。與免疫調節功能相對應,DPP4也被稱為白細胞活化抗原CD26或T細胞激活抗原CD26,簡稱CD26(cluster of differentiation 26 ,分化簇26)。注意,CD26就是DPP4。
DPP4能夠結合多種其它人體蛋白質/蛋白酶,如腺苷脫氨酶 (ADA)、纖連蛋白、膠原蛋白、趨化因子受體CXCR4、酪氨酸磷酸酶CD45等。其中最值得注意的是以下結合特性:DPP4能夠以高親和力特異性結合腺苷脫氨酶。
腺苷脫氨酶(ADA)是一種參與嘌呤代謝作用的核酸代謝酶。它的作用是拆解食物組織中的腺苷,移除掉腺苷中的氨基,將腺苷轉化為核苷肌苷。腺苷脫氨酶在人體各種組織中廣泛分布,並與免疫功能有重要關聯。腺苷脫氨酶有兩個常用的英文名稱:Adenosine deaminase(AD)和adenosine aminohydrolase(ADA)。腺苷脫氨酶通常簡稱為ADA。
能夠高親和力特異性結合腺苷脫氨酶,又讓DPP4獲得了另一個名稱:腺苷脫氨酶結合蛋白(adenosine deaminase binding protein,ADBP或adenosine aminohydrolase binding protein ,ADABP),簡稱ADA結合蛋白。DPP4的腺苷脫氨酶(ADA)結合能力,也就是腺苷脫氨酶(ADA)的DPP4結合能力。ADA、DPP4間的相互結合能力對本文後續內容非常重要。
DPP4同樣在眾多人體器官、組織中廣泛分布,包括下呼吸道(支氣管)、肺(特別是肺成纖維細胞)、心臟、胃腸道、肝臟、腎臟(近端腎小管)、胰腺、胸腺、前列腺、淋巴結、胎盤、血漿(及其它組織液)、腦、中樞神經系統、受傷皮膚、肌肉等等;DPP4在各種活化的免疫細胞中也廣泛分布、表達,如CD4(+)和CD8(+)T細胞、B細胞、自然殺傷細胞 (NK)、樹突狀細胞(DC) 和巨噬細胞。
DPP4是MERS-CoV的主要感染受體。以DPP4為感染受體,或具有DPP4結合能力的病毒很罕見(蛋白結合能力是以該蛋白為感染受體的先決條件),在SARS-CoV-2出現前,以DPP4為感染受體或具有DPP4結合能力的冠狀病毒可能只有兩種:2012年出現的MERS-CoV,和發現於2006年的扁顱蝠冠狀病毒HKU4。MERS-CoV更適宜結合人類DPP4,HKU4更適宜結合蝙蝠DPP4;通過結合相應DPP4,MERS-CoV既能感染蝙蝠細胞,也能感染人體細胞,HKU4則只能感染蝙蝠細胞。MERS-CoV和HKU4都屬於β譜系C支系。
筆者閱讀了多篇DPP4研究論文,這些論文提及的以DPP4為感染受體的冠狀病毒只有MERS-CoV和HKU4;這些論文只提及了一種具有DPP4結合能力的非冠狀病毒,令人驚奇的是,這種病毒居然是艾滋病病毒,即人類免疫缺陷病毒(HIV-1)。SARS-CoV-2與HIV-1的巧合、關聯實在太多了!後續文章將一一列舉說明。HIV-1以gp120蛋白結合DPP4。gp120蛋白是HIV-1的包膜蛋白—gp160蛋白的受體結合亞基,gp160蛋白的膜融合亞基是gp41蛋白,gp120蛋白、gp41蛋白在功能上分別對應冠狀病毒Spike蛋白(刺突蛋白)的S1蛋白(S1亞基)、S2蛋白(S2亞基)。HIV-1雖然具有DPP4結合能力,但似乎沒有論文將DPP4稱為HIV-1的感染受體。此外,筆者尚未查閱到HIV-1 gp120蛋白與DPP4的結合細節,因此,不清楚HIV-1的DPP4結合機制,與MERS-CoV或SARS-CoV-2的DPP4結合機制之間是否存在關聯。
### 2024-03-23補充 ###
在具有DPP4結合能力的病毒中,HIV-1能夠結合DPP4,但或許不以DPP4為感染受體;HKU4隻能感染蝙蝠細胞,不能感染人體細胞。因此,在大千世界不計其數的病毒(包括冠狀病毒和非冠狀病毒)中,能以DPP4為受體感染人體細胞的病毒可能僅有兩種,就是SARS-CoV-2和MERS-CoV。
###### end ######
SARS-CoV-2與MERS-CoV的第一組巧合是DPP4結合、利用巧合。這組巧合包括以下3項具體巧合:
1)、SARS-CoV-2、MERS-CoV都具有人類DPP4結合能力;
2)、SARS-CoV-2、MERS-CoV都能以DPP4為受體感染人體細胞。MERS-CoV能以DPP4為受體感染多種人體細胞;SARS-CoV-2 能以DPP4為受體感染某些人體細胞,如腦和脊髓中的皮質星形膠質細胞(cortical astrocytes)。報告SARS-CoV-2 以DPP4為受體感染皮質星形膠質細胞的論文將在本文尾部介紹。
SARS-CoV-2是β譜系B支系(乙型冠狀病毒屬Sarbe亞屬)唯一具有DPP4結合能力的冠狀病毒,同支系的其它冠狀病毒無一具有DPP4結合能力,無一以DPP4為感染受體。
以上兩項巧合已經很反常了,但還不夠神奇,再看它們的第3項DPP4巧合:
3)、SARS-CoV-2、MERS-CoV結合DPP4時所錨掛的DPP4關鍵氨基酸位點相同。下面的論文配圖展示了這一驚人巧合:
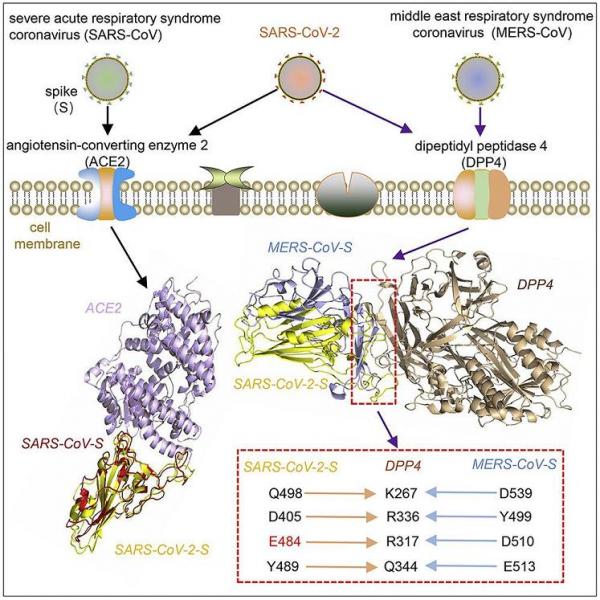
SARS-CoV 、SARS-CoV-2 、MERS-CoV 受體結合能力對照、關聯圖。
由上圖可見,
1)、SARS-CoV-2 兼具SARS-CoV(ACE2)和MERS-CoV(DPP4)的受體結合能力;
2)、SARS-CoV-2 Spike、MERS-CoV Spike 與同一組關鍵DPP4氨基酸(殘基)-(K267、R336、R317、Q344)作用、結合。
第2)點等同於,SARS-CoV-2、MERS-CoV在DPP4中的關鍵氨基酸結合位點相同,再或者說,SARS-CoV-2、MERS-CoV在結合DPP4時,錨掛的DPP4關鍵氨基酸位點相同。
論文依據:
The MERS-CoV Receptor DPP4 as a Candidate Binding Target of the SARS-CoV-2 Spike
MERS-CoV受體DPP4是SARS-CoV-2刺突的候選結合靶點
https://www.cell.com/iscience/fulltext/S2589-0042(20)30345-X
論文原文:
SARS-CoV-2-S/DPP4 binding shares key DPP4 residues with that of MERS-CoV-S/DPP4
Here, bioinformatics approaches combining human-virus protein interaction prediction and protein docking based on crystal structures have revealed the high affinity between human dipeptidylpeptidase 4 (DPP4) and the spike (S) receptor-binding domain of SARS-CoV-2. Intriguingly, the crucial binding residues of DPP4 are identical to those that are bound to the MERS-CoV-S.
Although the homology between SARS-CoV-2-S and MERS-CoV-S RBDs is low (19.1%), they shared identical binding residues of DPP4 at the interfaces (Figure 1C).
(以上內容摘自論文的不同位置,即論文三次強調了同一事實)
相關文章:
萬能”受體適配器--新冠S蛋白 1
前面已經指出,SARS-CoV-2、MERS-CoV差異巨大,進化距離非常遙遠,特別是,二者決定受體結合能力的RBD部分的aa序列相似度僅為19.1%。然而,兩者的RBD不僅都能結合DPP4,而且能錨掛到相同的DPP4位點,這實在是太神奇、太不可思議了!這如同,SARS-CoV-2得到了高人指點:你象MERS-CoV那樣錨掛到這些關鍵氨基酸位點,就能成功結合DPP4了。與其說,這是無目的、隨機性自然變異、自然演化的奇蹟,不如說,SARS-CoV-2參照、模仿了MERS-CoV DPP4結合機制。
第3項巧合仍然不夠神奇。而且,這還只是粗淺的發現;我們要繼續挖掘,下面還有更神奇、更驚人的寶藏。
MERS-CoV的DPP4結合機制也不是原創的。
前面提到,DPP4能夠以高親和力特異性結合人類腺苷脫氨酶(ADA),DPP4因此也被稱為腺苷脫氨酶結合蛋白,或ADA結合蛋白。
DPP4能夠結合ADA,也就是ADA能夠結合DPP4。
MERS-CoV的Spike和ADA都能結合DPP4,二者的DPP4結合機制也存在關聯嗎?
的確如此!二者DPP4結合機制的相似度更高、關聯更緊密:MERS-CoV Spike蛋白與人類ADA二者在結合DPP4時錨掛的DPP4氨基酸位點完全相同、一個不差!
論文依據:
Molecular basis of binding between novel human coronavirus MERS-CoV and its receptor CD26
新型人類冠狀病毒MERS-CoV與其受體CD26結合的分子基礎
https://www.nature.com/articles/nature12328
論文原文:
The features of these residue interactions are very similar to those mediating the interaction between adenosine deaminase (ADA) and CD26 (ref. 23). By a pairwise comparison, we unexpectedly found that all those CD26 residues identified in the virus–receptor interface are also involved in ADA binding, indicating a competition between ADA and the virus for CD26 receptor. As the ADA–CD26 interaction is shown to induce co-stimulatory signals in T cells22, this may indicate a possible manipulation of the host immune system by MERS-CoV through competition for the ADA-recognition site.
這段文字中的關鍵內容是:
By a pairwise comparison, we unexpectedly found that all those CD26 residues identified in the virus–receptor interface are also involved in ADA binding,
直譯:
通過兩兩比較,我們意外地發現病毒-受體(結合)界面中識別出的所有CD26 殘基也參與了ADA 的結合,
意譯:
通過兩兩比較,我們意外地發現,所有參與結合MERS-CoV Spike的CD26 /DPP4殘基,也都參與了與ADA的結合。
再意譯:
結合MERS-CoV Spike的CD26 /DPP4殘基,與結合ADA的CD26 /DPP4殘基完全相同。
再再意譯:
MERS-CoV Spike、ADA二者的DPP4結合位點完全相同;亦即,在結合DPP4時,MERS-CoV Spike、人類ADA二者錨掛的DPP4氨基酸位點完全相同!
依據前述原文所在的論文段落,參與結合MERS-CoV Spike和ADA的DPP4氨基酸位點共14個。從而可知,在結合DPP4時,MERS-CoV Spike、人類ADA二者錨掛的14個DPP4氨基酸位點完全相同、一個不差!
### 2024-03-18補充 ###
人類DPP4共有766個氨基酸位點。MERS-CoV、人類腺苷脫氨酶(ADA)錨掛的14個共同的DPP4氨基酸位點(按照論文依據指出它們時的順序)依次是:1-R336、2-Q286、3-T288、4-R317、5-Q344、6-K267、7-L294、8-Y322、9-A291、10-L294 、11-I295、12-V341、13-I346、14-N229。
MERS-CoV、人類腺苷脫氨酶(ADA)在DPP4 766個氨基酸位點中恰好錨掛了相同的14個氨基酸位點,這是極度不可思議的巧合。
###### end ######
論文還指出,人類DPP4、蝙蝠DPP4二者上述14個位點的氨基酸有12個相同,2個不同。
(美中不足的是,論文沒有提供一個對照圖)
“在結合DPP4時,MERS-CoV Spike、ADA二者錨掛的14個DPP4氨基酸位點完全相同、一個不差!”為什麼會發生如此驚人的巧合?有兩大可能性。
可能性一: MERS-CoV是由一種可結合蝙蝠DPP4的蝙蝠冠狀病毒變異產生的,如HKU4;
可能性二:有高人指點了MERS-CoV,你錨掛到ADA錨掛的那些DPP4位點,就能成功結合DPP4了。
兩對DPP4結合機制巧合小結如下:
SARS-CoV-2 Spike、MERS-CoV Spike在結合DPP4時錨掛的關鍵DPP4位點(4個氨基酸位點)相同;而MERS-CoV Spike、人類ADA在結合DPP4時錨掛的所有DPP4位點(14個氨基酸位點)則完全相同、一個不差。
以上兩對巧合表明:問題不只是SARS-CoV-2參照、模仿了MERS-CoV的DPP4結合機制這麼簡單,SARS-CoV-2、MERS-CoV極有可能都參照、借鑑、模仿了人類腺苷脫氨酶(ADA)的DPP4結合機制!MERS-CoV完全復用了ADA的所有14個DPP4結合位點,SARS-CoV-2則可能作了一些變通,只復用,或至少復用了ADA的4個關鍵DPP4結合位點。
號稱來自動物的SARS-CoV-2參照、模仿了眾多人體元件、蛋白、蛋白酶、激素的結構、能力。
最後,關於SARS-CoV-2的DPP4利用能力,即以DPP4為受體感染人體細胞的能力,作如下說明。
SARS-CoV-2不僅具備DPP4結合能力,而且能夠以DPP4為受體感染某些人體細胞。SARS-CoV-2可通過結合DPP4、CD147/Basigin(BSG,基礎免疫球蛋白)強烈感染人體的皮質星形膠質細胞(cortical astrocytes),損害神經系統,引發多種神經精神症狀。皮質星形膠質細胞是存在於腦和脊髓中的呈星狀的一種神經膠質細胞,可能是大腦中含量最多的細胞類型,具有多種重要功能。
論文依據:
Tropism of SARS-CoV-2 for human cortical astrocytes _ PNAS.htm
SARS-CoV-2 對人皮質星形膠質細胞的(感染)趨向性
https://www.pnas.org/doi/10.1073/pnas.2122236119
論文要點:
1、SARS-CoV-2可強烈感染皮質星形膠質細胞,並在其中強勁複製,造成皮質星形膠質細中廣泛的炎症,細胞因子分泌和先天免疫反應、防禦反應、損傷反應;
2、在皮質星形膠質細胞中沒有檢測到ACE2,這表明SARS-CoV-2通過非ACE2的其它受體途徑來達成對皮質星形膠質細胞的感染;
3、檢測發現,CD147和DPP4在星形膠質細胞中高豐度表達;
4、減少CD147、DPP4的表達豐度或活性都減少了SARS-CoV-2感染;
5、增加CD147、DPP4的表達豐度都增加、促進了SARS-CoV-2感染;
6、這些發現表明,DPP4和CD147足以介導SARS-CoV-2對皮質星形膠質細胞的感染,DPP4可能促進病毒進入,而CD147可能促進病毒複製。
7、GFAP+星形膠質細胞是血腦屏障不可缺少的組成部分,SARS-CoV-2對星形膠質細胞的感染可能使其得以破壞、突破腦血屏障(blood brain barrier),損害大腦和中樞神經系統。
GFAP:glial fibrillary acidic protein,膠質纖維酸性蛋白。GFAP+星形膠質細胞,表達(含有)GFAP的星形膠質細胞。
8、特別值得關注的是,最近有報道稱,腦脊液中含有SARS-CoV-2 抗體的兒童和青少年,即使是無症狀的COVID-19患者,也會出現新的或反覆出現的神經精神後果。一系列與COVID-19相關的神經系統症狀,包括頭暈、癲癇發作和認知困難,可能反映了星形膠質細胞的參與,而星形膠質細胞對大腦整體穩態和功能至關重要。
作一個小結。本文指出了SARS-CoV-2、MERS-CoV、人類腺苷脫氨酶(ADA)之間的一組DPP4相關巧合:
1、SARS-CoV-2 Spike、MERS-CoV Spike都能結合DPP4;
2、SARS-CoV-2、MERS-CoV都能以DPP4為受體感染人體細胞;
3、SARS-CoV-2 Spike、MERS-CoV Spike結合DPP4時錨掛的4個DPP4關鍵氨基酸位點相同;
4、MERS-CoV Spike、人類ADA結合DPP4時錨掛的所有14個DPP4氨基酸位點完全相同、一個不差。
由3、4可知:
SARS-CoV-2 Spike、MERS-CoV Spike、人類ADA結合DPP4時錨掛的4個DPP4關鍵氨基酸位點相同。
SARS-CoV-2、MERS-CoV進化關係非常遙遠,基因組差異非常巨大,特別是二者Spike蛋白RBD部分的氨基酸序列相似度僅為19.1%。以上四項極低概率巧合表明:SARS-CoV-2、MERS-CoV極有可能都參照、借鑑、模仿了人類腺苷脫氨酶(ADA)的DPP4結合機制。
(未完待續)






