巧合太多了,就不再是巧合了。
接續:新冠病毒中的跨物種、跨生物界、超生物基因 1
SARS-CoV-2對冠狀病毒基因的繼承、借鑑、模仿、優化、集成(續一)
WIV1(rs3367)
ACE2結合關鍵氨基酸
SARS-CoV-2 Spike(刺突)蛋白的ACE2結合能力主要由S1亞基RBD(receptor-binding domain,受體結合域)內5個位點上的氨基酸殘基決定,這5個氨基酸殘基稱為ACE2結合關鍵氨基酸。
SARS-CoV-2 的5個ACE2結合關鍵氨基酸參照、借鑑自蝙蝠冠狀病毒WIV1(rs3367)。
SARS-CoV-2的ACE2結合關鍵氨基酸與WIV1(rs3367)的ACE2結合關鍵氨基酸存在顯著的參照、借鑑關係:二種病毒的5個ACE2結合關鍵氨基酸有3個相同,另有一對理化性質高度相似。
SARS-CoV-2、WIV1(rs3367)的第2、第4、第5關鍵氨基酸同為苯丙氨酸、天冬酰胺(亦稱天門冬酰胺)、酪氨酸。如下表所示。
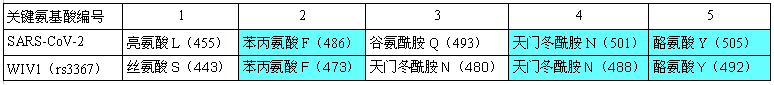
SARS-CoV-2、WIV1(rs3367)ACE2結合關鍵氨基酸對照表
F、N、Y依次是苯丙氨酸、天冬酰胺、酪氨酸的單字母縮寫。表中括號內的數字是相應氨基酸在Spike蛋白aa序列(amino
acid
sequence,氨基酸序列)中的序號/位置,比如,2-苯丙氨酸F(486)表示SARS-CoV-2的第2個ACE2結合關鍵氨基酸是一個苯丙氨酸,它是SARS-CoV-2
Spike蛋白的第486個氨基酸。
下圖比對了12種冠狀病毒Spike蛋白RBD的aa序列片斷。

5種人類致病冠狀病毒、7種蝙蝠冠狀病毒RBD局部區域aa序列比對
圖中5種人類致病冠狀病毒是:HCoV-NL63、HCoV-OC43、MERS-CoV、SARS-CoV-2、SARS-CoV。SARS-CoV Tor2是一個SARS-CoV流行病毒株,收集於Canada Toronto,全基因組序列上傳時間是april,2003。
SARS-CoV-2、rs3367的5個ACE2結合關鍵氨基酸在圖中以紫色方框標出。圖中除rs3367外的其它10種冠狀病毒與SARS-CoV-2至多只有1個相同ACE2結合關鍵氨基酸。
SARS-CoV-2、WIV1(rs3367)的5個ACE2結合關鍵氨基酸除了有3個相同外,還有1對高度相似。
SARS-CoV-2的第3個ACE2結合關鍵氨基酸是穀氨酰胺Q(也叫麩酰胺酸),WIV1(rs3367)的第3個ACE2結合關鍵氨基酸是天門冬酰胺N,雖然並不相同,但非常巧合的是,穀氨酰胺、天門冬酰胺這兩種氨基酸高度相似,它們的6項物理、化學屬性(分子結構、親水性、分子量、等電點、羧基解離常數、氨基解離常數)要麼相同,要麼非常相似、接近。如下表所示。
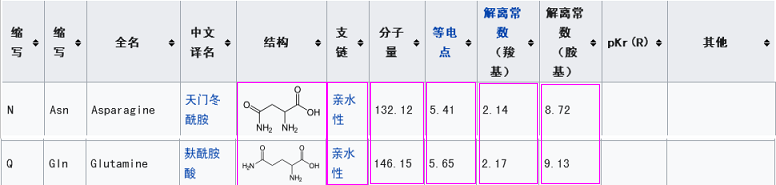
天門冬酰胺(N)、穀氨酰胺(Q)物理、化學屬性對照
上述6項理、化屬性同時高度相似的情況在氨基酸之間非常難得。這是無目的、隨機性自然變異的偶然巧合,還是人為設計的結果呢?
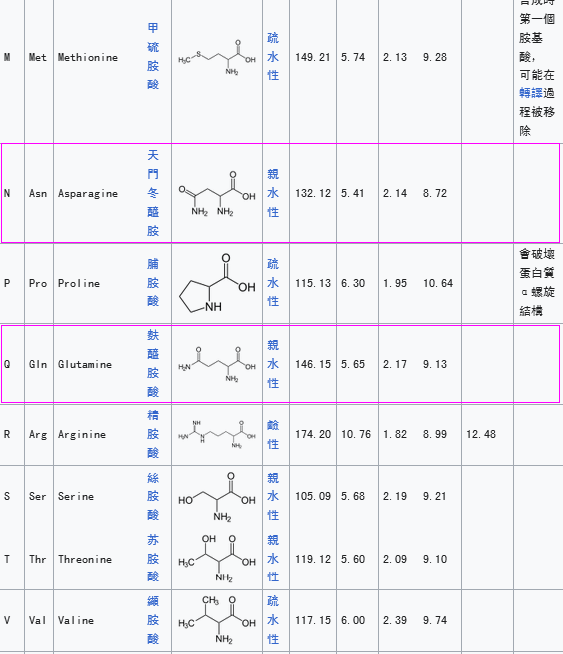
部分氨基酸物理、化學屬性對照表
有論文指出,SARS-CoV-2、WIV1(rs3367)RBD的三維結構也非常相似,二者RBD與ACE2結合形成的複合體的空間構象同樣非常相似,複合體中RBD、ACE2間關鍵氨基酸的接觸情況依然非常一致。
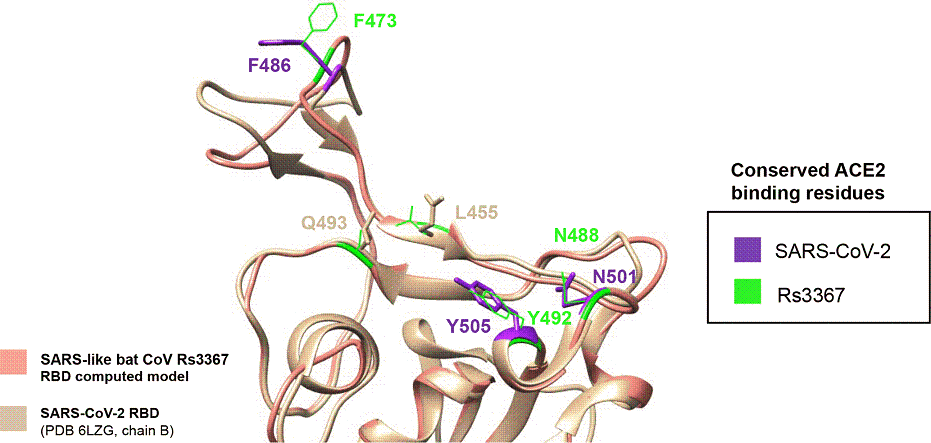
rs3367、SARS-CoV-2的RBD 3D結構模型對比
由上圖可見,橙紅色的rs3367 RBD 3D模型與褚灰色的SARS-CoV-2 RBD 3D模型高度相似、高度吻合;圖中還標示了rs3367、SARS-CoV-2的3對相同ACE2結合氨基酸,就是前面所指出的F486~F473、N501~N488、Y505~Y492。
hACE2結合能力
SARS-CoV-2、WIV1(rs3367)的Spike蛋白都具有強大的hACE2(human ACE2,人類ACE2)結合能力。
號稱來自動物的SARS-CoV-2的最早分離株(2019年12月在武漢分離得到的Wuhan-Hu-1等病毒株)未經任何人體適應性變異就已具備了極佳的hACE2結合能力,hACE2是SARS-CoV-2 Spike的最佳結合對象,SARS-CoV-2 Spike的hACE2結合親和力強於其與所有已對照物種ACE2的結合親和力;SARS-CoV-2未經任何人體適應性變異,自現身之初就以人類為最佳感染、致病對象,SARS-CoV-2對人體細胞、對人體的感染、致病能力強於所有已知動物物種,致病後果重於所有已知動物物種。
如果SARS-CoV-2是動物來源的,那麼,從動物宿主轉移到人類宿主之初,它更適合感染的,不是人類,而是它的動物來源宿主;如果SARS-CoV-2是動物來源的,那麼,它需要一個人體適應過程,它的刺突蛋白需要適應性變異以獲得更佳的人類ACE2結合能力,在獲得更理想的人類感染、致病能力前,它還需要經歷其它變異來充分適應人體組織、細胞。
WIV1(rs3367)Spike也具有極佳的hACE2結合、利用能力,這一點在Ralph S. Baric(拉爾夫·巴里克)團隊March 14, 2016發表的PNAS嵌合病毒論文中得到了揭示和證明。該論文實驗表明,WIV1、WIV1-MA15能感染實驗小鼠,並在小鼠氣道、肺中有效複製,不過,它們只能使小鼠產生輕度症狀;但是,當用表達hACE2的轉基因小鼠替代普通實驗小鼠後,WIV1、WIV1-MA15在小鼠肺中的複製滴度提高了100倍,部分轉基因小鼠體重減輕超過10%,病毒在轉基因小鼠大腦中的複製更為強勁(與肺中相比),使部分轉基因小鼠患上了致命的腦炎。
WIV1-MA15是用WIV1的Spike與SARS-CoV MA15的Spike外部分製作的嵌合病毒(將WIV1-Spike的基因序列,與SARS-CoV MA15 Spike外部分的基因序列拼接成一個完整的基因序列,再基於拼接所得基因序列使用反向遺傳平台合成、復活WIV1-MA15),SARS-CoV MA15是Ralph S. Baric等人實驗室培育的SARS-CoV小鼠適應性變異體。SARS-CoV能感染小鼠細胞,但不會使小鼠產生臨床疾病症狀,SARS-CoV MA15則可使小鼠嚴重致病並100%致死。反向遺傳平台功能強大,可只基於基因序列合成、復活冠狀病毒;它將冠狀病毒的基因編輯、基因改造簡化為基因序列的設計與編輯,可簡捷、靈活、高效、無痕跡地改造冠狀病毒。基因序列是一串文本字符串。
跨物種感染能力
SARS-CoV-2、WIV1(rs3367)都具有強大的跨物種ACE2結合能力及跨物種感染(/細胞進入)能力,而且它們的宿主範圍可能高度重合。
SARS-CoV-2的跨物種ACE2結合能力、跨物種感染能力極為驚人,已報告的SARS-CoV-2可感染物種約有30種左右,包括但不限於:人類、靈長類動物(如大猩猩、非洲綠猴、恆河猴、食蟹獼猴、狒狒、黑長尾猴和狨猴)、穿山甲、狗、豬、兔子、家貓、老虎、獅子、雪豹、麝香貓、某些鼠類(如倉鼠、田鼠)、某些鼬類或貂類(如雪貂、水貂、水獺、黃鼠狼等等)、北美鹿(如白尾鹿)、貉、樹鼩、果蝠等等。
由於相比SARS-CoV-2,對WIV1(rs3367)的研究要有限得多,而且WIV1(rs3367)的致病效果微弱而不明顯,因此,已報告的WIV1(rs3367)可感染物種少於SARS-CoV-2。由疫情前的有關論文可知,WIV1(rs3367)至少具有11種/類動物的ACE2結合能力和細胞進入(感染)能力,其中的9種/類也是SARS-CoV-2的可感染物種,它們是:人類、非洲綠猴、恆河猴、果子狸、貉、雪貂、水鼬(即水貂)、貓、果蝠。例外物種是老鼠/小鼠、菊頭蝠(等蝙蝠)。WIV1(rs3367)可感染老鼠/小鼠,以及菊頭蝠等眾多蝙蝠,但SARS-CoV-2不能感染老鼠/小鼠,不能感染菊頭蝠等眾多蝙蝠(SARS-CoV-2可感染倉鼠、田鼠、果蝠)。菊頭蝠是眾多蝙蝠冠狀病毒的宿主,然而,號稱來自蝙蝠的SARS-CoV-2不能結合菊頭蝠ACE2,不能進入/感染菊頭蝠等眾多蝙蝠的細胞。
WIV1(rs3367)雖然具有強大的跨物種ACE2結合能力,以及強大的跨物種細胞進入能力,但它自身毒力(致病能力)微弱,至多只能使某些小型被感染物種(如實驗室小鼠)產生輕度疾病症狀;雖然能夠強力結合hACE2,並具備人體細胞進入能力,但WIV1(rs3367)不是一種人類致病冠狀病毒,它不能使人體產生臨床疾病症狀;雖然能在表達hACE2的轉基因小鼠體內強烈複製,但WIV1(rs3367)應該不能在人體細胞內有效複製,不能在人體中持續存在。這種情況類似於WIV1(rs3367)對埃及果福的感染。
on 19 December 2018,Ralph S. Baric團隊、國家過敏和傳染病研究所(所長是安東尼·福奇Anthony Fauci)的兩個下屬機構聯合發表了的一篇研究WIV1對埃及果福感染、致病能力的MDPI論文,論文實驗表明:
1)、WIV1能有效結合、利用埃及果福(Egyptian fruit bat,Rousettus aegyptiacus)的ACE2進入果蝠細胞,能夠感染果蝠的鼻甲、咽部、氣管、肺、腎、胃、腸等眾多組織、器官,使這些組織、器官產生不同程度的內在免疫反應;
2)、但是,12隻實驗果蝠都沒有表現出明顯的臨床疾病跡象(如呼吸窘迫、厭食或嗜睡),未檢測到果蝠的體重減輕或體溫變化;
3)、感染後第3天,只在果蝠咽部和鼻甲骨檢測到WIV1的RNA,在其它器官、組織中已檢測不到WIV1的RNA,WIV1已經從果蝠的大多數器官、組織中消失了。
論文認為,WIV1雖然能夠感染果蝠的眾多組織、器官,但它在果蝠組織、器官內缺乏有效的複製、繁衍(因而將從果福體內自動消失)。
論文還做了兩組轉基因BHK細胞(Baby Hamster Syrian Kidney cells,敘利亞幼倉鼠腎細胞)體外感染實驗,實驗結果表明:WIV1能有效感染表達hACE2的轉基因BHK細胞,以及表達果蝠ACE2 的轉基因BHK細胞;與果福體內感染實驗不同的是,WIV1在這兩種轉基因BHK細胞中都能健壯地持續複製。
其它信息
WIV1、rs3367發現於雲南同一山洞,是一對“孿生”蝙蝠冠狀病毒,二者全基因組序列一致度為99.92%,二者決定物種感染能力及宿主範圍的Spike蛋白S1亞基(受體結合基因)的aa序列完全相同。2013年4月8日,武漢病毒研究所將rs3367的全基因組序列、WIV1的spike蛋白aa序列上傳至NCBI(National Center for Biotechnology Information,美國國家生物技術信息中心)的GenBank生物信息數據庫,2013年7月8日,WIV1的全基因組序列也上傳至GenBank國際共享(武漢病毒研究所受美國政府機構資助為美國搜集、鑑定冠狀病毒)。
雲南同一山洞還發現了另一對“孿生”蝙蝠冠狀病毒:WIV16、Rs4874,這對病毒全基因組序列一致度為99.93%。它們與WIV1、rs3367也高度相似,WIV1與WIV16的全基因組序列一致度為97.54%。這二對四個“至親”病毒的5個ACE2結合關鍵氨基酸完全相同。
在疫情發生前報告的冠狀病毒中(不計疫情發生後報告的某些穿山甲冠狀病毒、某些蝙蝠冠狀病毒),可能只有上述四個病毒與SARS-CoV-2有3個(含)以上的相同ACE2結合關鍵氨基酸;甚至,其它冠狀病毒與SARS-CoV-2可能至多只有1個相同ACE2結合關鍵氨基酸,筆者未看到過其它與SARS-CoV-2有2個(含)以上相同ACE2結合關鍵氨基酸的冠狀病毒。
上一篇文章指出,SARS-CoV-2的病毒骨架主要來自CoVZC45(/CoVZXC21)、SARS-CoV,這兩/三種病毒與SARS-CoV-2都只有一個相同的ACE2結合關鍵氨基酸:第5關鍵氨基酸--酪氨酸Y。見下表:
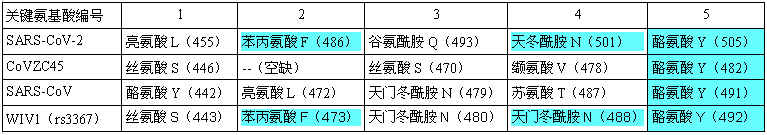
SARS-CoV-2、CoVZC45、SARS-CoV、WIV1的ACE2結合關鍵氨基酸對照表
SARS-CoV-2、SARS-CoV、CoVZC45/CoVZXC21、WIV1(rs3367)都是乙型冠狀病毒屬(Betacoronavirus)B亞屬(Sarbecovirus)冠狀病毒,該亞屬(subgenera)也稱作冠狀病毒β譜系(β-CoVs)B支系。
雖然處於同譜系同支系,但SARS-CoV-2與WIV1(rs3367)全基因組序列相似度僅為82.13%,Spike蛋白aa序列相似度僅為77.70 %,二者沒有直接或接近的進化淵源。
問題
SARS-CoV-2與WIV1(rs3367)ACE2結合關鍵氨基酸的高度關聯,是自然變異、自然重組產生的嗎?是自然進化/自然演化的巧合,還是人為借鑑、人為設計的結果?
相關文章:
誰設計、製造了新冠病毒(三 下)
連繫新冠病毒與Ralph S. Baric的雙紐帶(下)
(未完待續)











